Kakšna formula ima jabolčno kislino in kako jo dobite?
Drugo ime za jabolčno kislino je hidroksintarična. Je član razreda hidroksi dikarboksilne kisline. Spojino je najprej 1785 leta pridobil Karl Scheele (švedski kemik) iz nezrelih jabolk (ki je določil svoje ime). Tudi v naravi najdemo v grozdju, barberi, pepelu, malini itd. Snov se v obliki soli, imenovanih malati, nahaja v tobaku. Največja vsebnost hidroksiciklične kisline skupaj s citronsko kislino pri nezrelih zelenih jabolkih doseže 1,2%.

Jabolčna kislina: formula
Ta kemijska spojina ima naslednjo formulo:
HOOC-CH2-CH (OH) -COOH ali C4H302 (OH) 3
V normalnih pogojih je jabolčna kislina brezbarvni kristalinični prah, ki se dobro raztopi v alkoholu (v 100 ml - 35,9 g) in v vodi (v 100 ml - 144 g). Molekularna teža spojine, ki so enake 134,1 g / mol.
Ad
Spodnja slika prikazuje prostorsko strukturo molekule jabolčne kisline. Atomi ogljika so označeni s črno, kisik v rdeči, vodik v beli barvi.
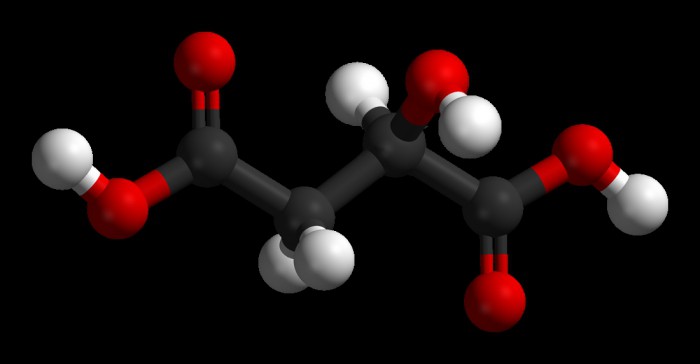
Malična kislina obstaja v obliki racemata (optično neaktivna spojina) in dveh stereoizomerov. Slednje so takšne spojine v molekulah, med katerimi je med atomi enaka sekvenca kemijskih vezi, vendar obstajajo razlike v njihovi razporeditvi v prostoru glede na druge. To vprašanje podrobno obravnava stereokemijo. V jabolčni kislini obstajata dva stereoizomera, pri čemer je bil P. Walden prvi, ki je leta 1896 pokazal, da so možna medsebojna konverzija enantiomerov. Proučevanje tega pojava je služilo kot osnova za kasnejše oblikovanje teorije reakcije tako imenovane nukleofilne substitucije na atomu ogljika (nasičenega).
Ad
Pridobivanje
Snov je pridobljena na dva načina: naravna in kemična. Prva ponuja ekstrakcijo sadja in jagodičja. Sintetična jabolčna kislina je pridobljena z več reakcijami:
1. Hidracija maleinske ali fumarne kisline. Predpogoj je temperatura 100-150 ° C. Reakcijska enačba je naslednja:
HOOCCH = CHCOOH + H20 → NOEP-CH2-CH (OH) -COOH
2. Hidroliza bromo- ali kloro-jantarne kisline. Malično kislino ekstrahiramo z uporabo etra. Uporablja rastlinski material.
Jabolčna kislina. Reakcije interakcij

1. Oksidacija žveplove koncentrirane kisline (H2SO4) z nastankom kumalinske kisline. Reakcija poteka v dveh fazah:
HOOC-CH2-CH (OH) -COOH + H2SO4 → HOOC-CH2-CHO + HCOOH
Rezultat je aldehid malonic in mravljične kisline. Ta spojina se razgradi in oblikuje ogljikov monoksid in voda:
HCOOH → CO + H2O
Aldehid malonska kislina se takoj pretvori v kumalinsko kislino.
2. Interakcija z klorovodikovo kislino :
HOOC-CH2-CH (OH) -COOH + HCl → HOOC-CH2-CHCl-COOH
Nastala snov se imenuje 2-kloroantin.
3. Jabolčna kislina je dovzetna za oksidacijo (zlasti pri uporabi KMnO4): t
HOOC-CH2-CH (OH) -COOH + KMnO4 → HOOC-CH2-CO-COOH
Nastala kislina se imenuje 2-okso-jantarna kislina (oksil-ocetna kislina).
4. Medsebojno delovanje z acetil kloridom, da se tvori 2-acetoksisukcinska kislina: t
HOOC-CH2-CH (OH) -COOH + CH3COCl → HOOC-CH2-CH (OCOCH3) -COOH
S postopnim segrevanjem se jabolčna kislina razgradi in tvori serijo vmesnih proizvodov. Pri temperaturi 100 ° C se pojavi nastanek anhidridov (podobni so laktidom). S povečanjem na 140-150 ° C se pretvorijo v fumarno kislino. Pri hitrem povišanju temperature na 180 ° C dobimo anhidrid maleinske kisline.
Ad
Če povzamemo vse podatke, lahko rečemo, da so kemijske lastnosti jabolčne kisline enake kemičnim lastnostim drugih hidroksi kislin.
Biološka vloga
Jabolčna kislina je vključena v Krebsov cikel. Predstavlja glavno stopnjo v dihanju vseh celic, ki uporabljajo kisik, in je vmesna vez med glikolizo in električno transportno verigo. Glavna vloga cikla trikarboksilne kisline (Krebs) je sinteza reduciranih koencimov FAD * H 2 in NAD * H. Nato se uporabljajo za proizvodnjo ATP, ADP in fosfatov. Hidroksidna kislina se tvori s hidracijo s fumarno. Njena poznejša oksidacija z NAD + zaključi Krebsov cikel. Katalizirajoči encim je malat dehidrogenaza.

Področja uporabe
Dobljena komercialna jabolčna kislina se zelo pogosto uporablja:
- V živilski industriji je znana pod oznako E296. Snov, ki se uporablja kot konzervans. ojačevalec okusa in regulator kislosti. Glavna uporaba: gazirane pijače, sadni sokovi, slaščice, vino, konzervirana hrana. Treba je poudariti, da v majhnih količinah jabolčna kislina pozitivno vpliva na telo.
- V kozmetologiji. Oxycytic kislina ima antioksidativno, beljenje, piling in vlažilne lastnosti, ki omogoča, da se uporablja kot del anti-celulita in sredstva za beljenje kože, pilingov. Poleg tega se doda zobnim pastam in izdelkom za nego ust.
- V farmakologiji se za pripravo izkašljevalcev in odvajalnikov uporablja jabolčna kislina (formula je navedena zgoraj).