Najmočnejša kislina. Formula najmočnejše kisline
O tem, katera kislina je najmočnejša, je trdila več kot ena generacija kemikov. V različnih časih je ta naslov prejel dušik, žveplo, klorovodikovo kislino. Nekateri so verjeli, da spojine ne morejo biti močnejše od fluorovodikove kisline. Nedavno so bile pridobljene nove spojine z močnimi kislinskimi lastnostmi. Morda je med njimi najmočnejša kislina na svetu? Prispevek obravnava značilnosti najmočnejših obstojnih kislin našega časa in daje njihove kratke kemijske lastnosti.
Koncept kisline 
Kemija je natančna kvantitativna znanost. Naslov »Najmočnejša kislina« je treba smiselno pripisati eni ali drugi snovi. Kaj je lahko glavni kazalnik, ki označuje moč katere koli povezave?
Najprej se spomnimo klasične definicije kisline. V bistvu se ta beseda uporablja za kompleksne kemijske spojine, ki so sestavljene iz vodikovega in kislega ostanka. Število vodikovih atomov v spojini je odvisno od valence kislega ostanka. V molekuli klorovodikove kisline je na primer le en vodikov atom; in žveplova kislina že ima dva H + atoma.
Kislinske lastnosti
Vse kisline imajo določene kemijske lastnosti, ki se lahko imenujejo skupne za ta razred kemičnih spojin.
- Sposobnost interakcije s kovinami ob sprostitvi vodika.
- Sposobnost interakcije z bazami, pri čemer poudarjajo soli.
- Možnost spreminjanja barve indikatorjev - na primer, da povzroči rdečico lakmusovega papirja.

V vseh zgoraj omenjenih lastnostih se kaže drugačno "spretnost" katerekoli znane kisline - sposobnost darovati atom vodika, ki jo nadomesti z atomom druge kemikalije ali molekule spojine. Prav ta sposobnost je značilna za "moč" kisline in stopnjo njene interakcije z drugimi kemijskimi elementi.
Voda in kislina
Prisotnost vode bistveno zmanjša sposobnost kisline za sproščanje atomov vodika. To je zato, ker vodik lahko oblikuje svoje kemične vezi med molekulami kisline in vode, zato je njena sposobnost, da se loči od baze, manjša od sposobnosti nerazredčenih kislin.
Superacid
Beseda "superacid" je bila v kemijski slovar uvedena leta 1927, z rahlo roko slavnega kemika Jamesa Conanta.
Standard trdnosti te kemične spojine je koncentrirano žveplovo kislino. Kemična snov ali katera koli mešanica, ki presega kislost koncentrirane žveplove kisline, se imenuje superkiselina. Vrednost superkisline je odvisna od njene sposobnosti, da da pozitivno električni naboj iz katerega koli razloga. Za osnovni parameter za določanje kislosti je bil sprejet ustrezen kazalnik H 2 SO 4 . Med močnimi kislinami so snovi s precej nenavadnimi imeni in lastnostmi.
Znane močne kisline
Najbolj znane kisline iz poteka anorganske kemije so hidrojodične (HI), bromovodik (HBr), klorovodik (HCl), žveplo (H 2 SO 4 ) in dušikove (HNO 3 ) kisline. Vsi imajo visok indeks kislosti in lahko reagirajo z večino kovin in baz. V tej seriji je najmočnejša kislina zmes dušikove in klorovodikove kisline, imenovane "aqua regia". Formula najmočnejše kisline v tej seriji je HNO3 + 3 HCl. Ta spojina lahko raztopi celo plemenite kovine, kot so zlato in platina.

Nenavadno je, da fluorovodikova kislina, ki je spojina vodika z najmočnejšim halogenom - fluorom, ni bila vključena v kandidate za naziv "Najmočnejša kislina v kemiji". Edina značilnost te snovi je sposobnost raztapljanja stekla. Zato je takšna kislina shranjena v polietilenskem vsebniku.
Močne organske kisline
Kandidati za naziv "Najmočnejša kislina v organski kemiji" - mravlja in ocetna kisline. Mravljinčna kislina je najmočnejši v homolognem območju omejevalnih kislin. Ime je dobilo zaradi dejstva, da je nekaj vsebovano v izločkih mravljev.

Ocetna kislina je nekoliko šibkejša od mravljične kisline, vendar je njen spekter porazdelitve veliko širši. Pogosto ga najdemo v sokovih rastlin in nastanejo med oksidacijo različnih organskih snovi.
Nedavni razvoj na področju kemije je omogočil sintezo nove snovi, ki lahko konkurira tradicionalnim organskim snovem. Trifluorometansulfonska kislina ima indeks kislosti višji kot žveplova kislina. Hkrati je CF3SO3H stabilna higroskopična tekočina z določenimi fizikalno-kemijskimi lastnostmi v normalnih pogojih. Danes lahko temu sestavku dodelite naslov »Najmočnejša organska kislina«.
Mnogi menijo, da stopnja kislosti ne more biti bistveno višja od stopnje žveplove kisline. Nedavno pa so znanstveniki sintetizirali številne snovi, katerih parametri kislosti so več tisočkrat višji od vrednosti žveplove kisline. Spojine, dobljene z interakcijo protonskih kislin z Lewisovimi kislinami, imajo nenormalno visoke vrednosti kislosti. V znanstvenem svetu se imenujejo: kompleksne protonske kisline.
Čarobna kislina
Da V redu Čarobna kislina. To se imenuje. Magična kislina je mešanica fluorida vodika ali fluor sulfonske kisline z antimonovim pentafluoridom. Kemična formula te spojine je prikazana na sliki: 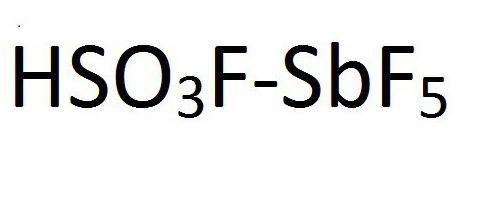
To čudno ime čarobna kislina, ki jo je dobil na božični zabavi kemikov, ki se je zgodila v zgodnjih šestdesetih letih. Član raziskovalne skupine, J. Olaha, je pokazal smešen trik, ki je raztapljal voščeno svečo v tej čudoviti tekočini. To je ena najmočnejših kislin nove generacije, toda snov, ki jo presega po moči in kislosti, je že sintetizirana.
Najmočnejša kislina na svetu
Karborna kislina je karboranska kislina, ki je daleč najmočnejša spojina na svetu. Formula najmočnejše kisline izgleda takole: H (CHB11Cl11).
Ta pošast je nastala leta 2005 na Kalifornijski univerzi v tesnem sodelovanju z Novosibirskim inštitutom za katalizo SB RAS.
Sama ideja sinteze je nastala v mislih znanstvenikov, skupaj s sanjami o novih molekulah in atomih brez primere. Nova kislina je milijonkrat močnejša od žveplove, medtem ko je popolnoma neagresivna in najmočnejša kislina se lahko enostavno shrani v steklenici. Vendar se sčasoma steklo še vedno raztopi in s povečanjem temperature se hitrost te reakcije znatno poveča. 
Ta izjemna mehkoba je posledica visoke stabilnosti nove spojine. Kot vse kemikalije, povezane s kislinami, se karboranska kislina hitro odzove in se odreče svojemu edinemu protonu. Osnova kisline je tako stabilna, da kemijska reakcija ne gre dlje.
Kemijske lastnosti karboranske kisline
Nova kislina je odličen protonski donor H + . To je tisto, kar določa moč te snovi. Raztopina karboranske kisline vsebuje več vodikovih ionov kot katera koli druga kislina na svetu. V kemijski reakciji SbF 5 - antimonov pentafluorid, veže ion fluora. Istočasno se sproščajo novi in novi atomi vodika. Zato je karboranska kislina najmočnejša na svetu - suspenzija protonov v njegovi raztopini je 2 × 10 19 -krat večja od žveplove kisline.
Vendar je kislinska baza te spojine izjemno stabilna. Molekula te snovi je sestavljena iz enajstih atomov broma in enakega števila atomov klora. V vesolju ti delci tvorijo kompleksno, geometrijsko pravilno sliko, ki se imenuje ikozaeder. Ta razporeditev atomov je najbolj stabilna, kar pojasnjuje stabilnost karboranske kisline. 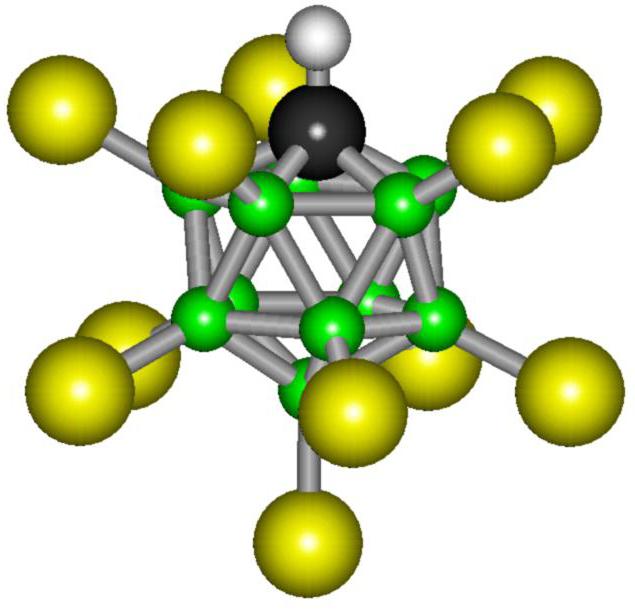
Vrednost karboranske kisline
Najmočnejša kislina na svetu je ustvarjalcem prinesla zaslužene nagrade in priznanja v znanstvenem svetu. Čeprav vse lastnosti nove snovi niso popolnoma razumljive, je že postalo jasno, da pomen tega odkritja presega laboratorije in raziskovalne inštitute. Karborna kislina se lahko uporablja kot močan katalizator v različnih industrijskih reakcijah. Poleg tega lahko nova kislina komunicira z najbolj trdovratnimi kemikalijami - inertnimi plini. Trenutno poteka delo, ki omogoča možnost vstopa v reakcijo ksenona.
Nedvomno bodo neverjetne lastnosti novih kislin našli uporabo na različnih področjih znanosti in tehnologije.