Kemijska vez - koncept in klasifikacija
Vsaka interakcija med atomi je možna le, če obstaja kemijska vez. Takšna vez je vzrok za nastanek stabilnega poliatomskega sistema - molekularni ion, molekula, kristalne rešetke. Močna kemijska vez zahteva veliko energije za prekinitev, zato je osnovna količina za merjenje moči vezi.
Pogoji za kemijsko vezavo
Oblikovanje kemijske vezi vedno spremlja sproščanje energije. Ta proces nastane zaradi zmanjšanja potencialne energije sistema medsebojno delujočih delcev - molekul, ionov, atomov. Potencialna energija nastali sistem interakcijskih elementov je vedno manjši od energije nevezanih izhodnih delcev. Tako je osnova za nastanek kemijske vezi v sistemu zmanjšanje potencialne energije njenih elementov.
Ad
Narava kemijske interakcije
Kemična vezava je posledica interakcije elektromagnetnih polj, ki nastajajo okoli elektronov in atomskih jeder tistih snovi, ki sodelujejo pri nastajanju nove molekule ali kristala. Po odkritju teorije o strukturi atoma je narava te interakcije postala bolj dostopna za študij. 
Prvič se je v angleškem fiziku G. Deviju pojavila ideja o električni naravi kemičnega vezanja, ki je predlagala, da se molekule oblikujejo zaradi električne privlačnosti nasprotno nabitih delcev. Ta ideja je zanimala švedskega kemika in naturalista I.Ya. Berzelius, ki je razvil elektrokemijsko teorijo kemičnih vezav.
Prva teorija, ki je pojasnjevala procese kemijske interakcije snovi, je bila nepopolna in sčasoma jo je bilo treba opustiti.
Teorija Butlerov
Uspešnejši poskus razlage narave kemične vezi snovi je opravil ruski znanstvenik A. M. Butlerov. Temelj njegove teorije je ta znanstvenik postavil takšne predpostavke:
- Atomi v povezanem stanju so med seboj povezani v določenem vrstnem redu. Sprememba v tem vrstnem redu je vzrok za nastanek nove snovi.
- Atome vežejo valenčni zakoni.
- Lastnosti snovi so odvisne od vrstnega reda atomov spojin v molekuli snovi. Različni vrstni red lokacij povzroči spremembo kemijskih lastnosti snovi.
- Atomi med seboj najbolj vplivajo drug na drugega.
Butlerova teorija je razložila lastnosti kemikalij ne le po njihovi sestavi, ampak tudi po razporeditvi atomov. Tak notranji nalog A.M. Butlerov je imenoval "kemijsko strukturo". 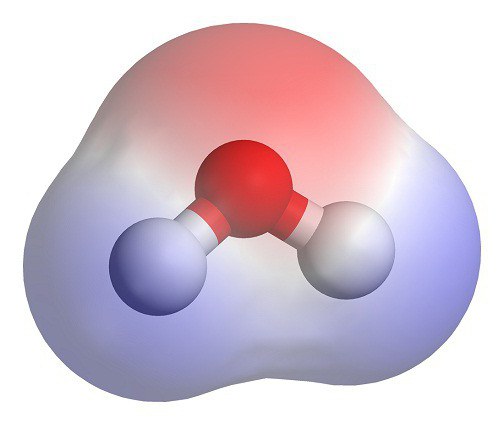
Teorija ruskega znanstvenika je omogočila, da se stvari uvrščajo v razvrstitev snovi in omogočila možnost določitve strukture molekul glede na njihove kemijske lastnosti. Teorija je odgovorila tudi na vprašanje, zakaj imajo molekule z enakim številom atomov različne kemijske lastnosti?
Ad
Predpogoji za ustvarjanje teorij kemijskih vezi
Butlerov se v svoji teoriji kemijske strukture ni dotaknil vprašanja, kaj je kemijska vez. Za to je bilo torej premalo podatkov o notranji strukturi snovi. Šele po odprtju planetni model atoma Ameriški znanstvenik Lewis je začel razvijati hipotezo, da kemična vez nastane z nastajanjem elektronskega para, ki hkrati pripada dvema atomoma. Nato je ta ideja postala temelj za razvoj teorije kovalentnih vezi.
Kovalentna kemijska vez
Stabilna kemična spojina se lahko oblikuje, ko se elektronski oblaki dveh sosednjih atomov prekrivata. Rezultat tega medsebojnega preseka je naraščajoča elektronska gostota v medzvočnem prostoru. Jedra atomov, kot je dobro znano, so pozitivno nabita in se zato poskušajo čim bolj približati negativno nabitemu elektronskemu oblaku. Ta privlačnost je veliko močnejša od odbojne sile med dvema pozitivno nabitima jedroma, zato je ta odnos stabilen.
Ad
Kemične vezi so prvič opravili kemiki Geytler in London. Obravnavali so razmerje med dvema atomoma vodika. Najenostavnejša vizualna predstavitev lahko izgleda takole: 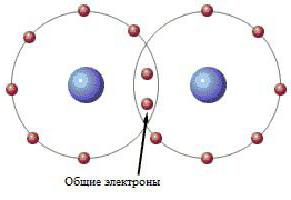
Kot lahko vidimo, elektronski par zavzema kvantno mesto v obeh atomih vodika. Ta dvosmerna postavitev elektrona se imenuje kovalentna kemijska vez. Kovalentna vez značilne za molekule enostavnih snovi in njihovih spojin iz nekovin. Snovi, ki nastanejo zaradi kovalentne vezave, običajno ne izvajajo električnega toka ali so polprevodniki.
Jonska vez
V primeru medsebojnega električnega privlačenja dveh nasprotno nabitih ionov nastane kemijska vez ionskega tipa. Ioni so lahko preprosti, sestavljeni iz enega atoma snovi. V spojinah tega tipa so preprosti ioni najpogosteje pozitivno nabite kovinski atomi skupin 1, 2, ki so izgubili svoj elektron. Nastajanje negativnih ionov je neločljivo povezano z atomi značilnih nekovin in bazami njihovih kislin. Zato je med tipičnimi ionskimi spojinami veliko halogenidov alkalijske kovine na primer CsF, NaCl in drugi. 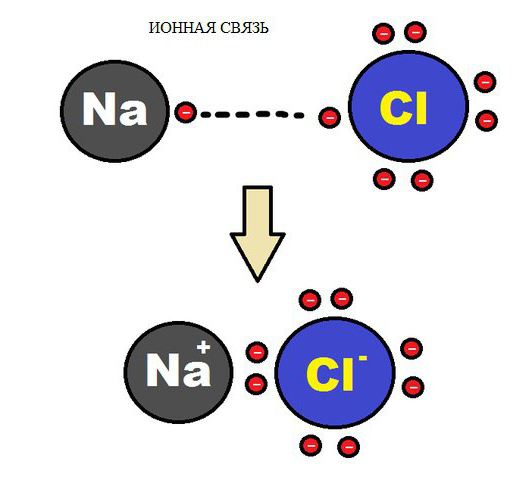
Za razliko od kovalentne vezi ion ni nasičen: različno število nasprotno nabitih ionov se lahko pridruži ionu ali skupini ionov. Število pritrjenih delcev je omejeno le z linearnimi dimenzijami interakcijskih ionov in s pogojem, pod katerim morajo biti privlačne sile nasprotno nabitih ionov večje od odbojnih sil enako nabitih delcev, ki sodelujejo v ionski spojini.
Ad
Vodikova vez
Še pred nastankom teorije kemijske strukture je bilo eksperimentalno ugotovljeno, da imajo vodikove spojine z različnimi ne-kovinami nekoliko nenavadne lastnosti. Na primer, vrelišče vodikovega fluorida in vode je veliko večje od pričakovanega. 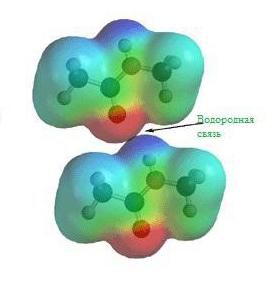
Te in druge lastnosti vodikovih spojin lahko razložimo s sposobnostjo H + atoma, da tvori drugo kemijsko vez. Ta vrsta spojine se imenuje »vodikova vez«. Vzroki vodikove vezi so zakoreninjeni v lastnostih elektrostatičnih sil. Na primer, v molekuli vodikovega fluorida je skupni oblak elektronov tako premaknjen proti fluoru, da je prostor okoli atoma te snovi nasičen z negativnim električnim poljem. Okoli vodikovega atoma, brez svojega edinega elektrona, je polje veliko šibkejše in ima pozitiven naboj. Posledica tega je dodatno razmerje med pozitivnimi polji elektronskih oblakov H + in negativnim F - .
Ad
Kemična vez kovin
Atomi vseh kovin se nahajajo v prostoru na določen način. Razporeditev kovinskih atomov se imenuje kristalna rešetka. V tem primeru elektroni različnih atomov med seboj slabo komunicirajo in tvorijo skupni elektronski oblak. Ta vrsta interakcije med atomi in elektroni se imenuje "kovinska vez". 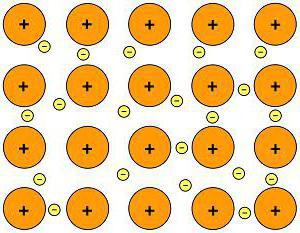 Prosto gibanje elektronov v kovinah lahko pojasni fizikalne lastnosti kovinskih snovi: električno prevodnost, toplotno prevodnost, trdnost, taljivost in druge.
Prosto gibanje elektronov v kovinah lahko pojasni fizikalne lastnosti kovinskih snovi: električno prevodnost, toplotno prevodnost, trdnost, taljivost in druge.