Ioni so nabiti atomi in atomske skupine. Koncept ionskih reakcij in naboj ionov
Prvič je bil izraz "ion" uveden leta 1834, v katerem je zasluga Michaela Faradaya. Po študiju učinka električnega toka na raztopine soli, alkalij in kislin je prišel do zaključka, da vsebujejo delce, ki imajo določeno napolnjenost. Faradayovi kationi se imenujejo ioni, ki se v električnem polju premikajo na katodo, ki ima negativen naboj. Anioni so negativno nabiti neelementni ionski delci, ki se v električnem polju premikajo proti plus-anodi.
Ta terminologija se sedaj uporablja, delci pa se še proučujejo, kar nam omogoča, da razmislimo o kemijski reakciji, ki je posledica elektrostatične interakcije. Po tem principu poteka veliko reakcij, ki omogočajo razumevanje njihovega poteka in izbiranje katalizatorjev in inhibitorjev za pospešitev njihovega poteka in zaviranje sinteze. Prav tako je postalo znano, da so mnoge snovi, zlasti v raztopinah, vedno v obliki ionov.
Nomenklatura in klasifikacija ionov
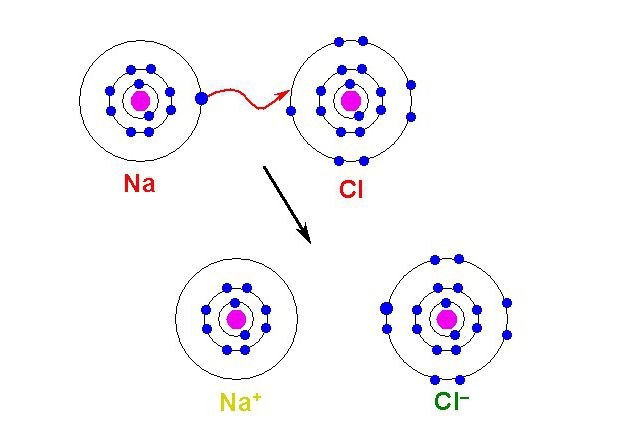
Ioni so nabiti atomi ali skupina atomov, ki so izgubili ali pridobili elektrone med kemijsko reakcijo. Sestavljajo zunanje plasti atoma in se lahko izgubijo zaradi nizke sile gravitacije jedra. Nato je rezultat odstranitve elektrona pozitiven ion. Tudi, če ima atom močan jedrski naboj in ozko elektronsko lupino, je jedro akceptor dodatnih elektronov. Posledično se tvori negativni ionski delec.
Ioni sami niso samo atomi s presežkom ali nezadostno elektronsko lupino. Lahko je skupina atomov. V naravi so najpogosteje prisotni skupinski ioni, ki so prisotni v raztopinah, bioloških tekočinah organizmov in v morski vodi. Obstaja veliko število vrst ionov, katerih imena so precej tradicionalna. Kationi so ionski delci, ki so pozitivno nabiti in negativno nabiti ioni so anioni. Odvisno od sestave se imenujejo drugače. Na primer natrijev kation, cezijev kation in drugi. Anioni se imenujejo drugače, saj so najpogosteje sestavljeni iz več atomov: sulfatnega aniona, ortofosfatnega aniona in drugih.
Mehanizem za tvorbo ionov
Kemični elementi v spojinah so redko električno nevtralni. To pomeni, da skoraj nikoli niso v stanju atomov. V izobraževanju kovalentna vez, kar velja za najpogostejše, imajo atomi tudi določeno polnitev in elektronska gostota se premika vzdolž vezi znotraj molekule. Vendar se ionski naboj tukaj ne tvori, ker je energija kovalentne vezi manjša od ionizacijske energije. Zato kljub različni elektronegativnosti nekateri atomi ne morejo povsem pritegniti elektronov zunanje plasti drugih.
Pri ionskih reakcijah, kjer je razlika v elektronegativnosti med atomi dovolj velika, lahko en atom vzame elektrone zunanje plasti iz drugega atoma. Potem je ustvarjena povezava močno polarizirana in lomljena. Energija, porabljena za to, ki ustvarja ionski naboj, se imenuje ionizacijska energija. Za vsak atom je drugačen in je naveden v standardnih tabelah.
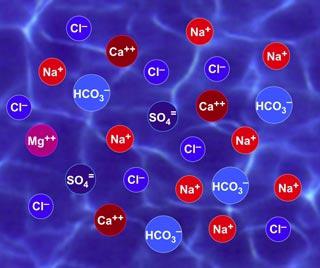
Ionizacija je mogoča le v primeru, ko je atom ali skupina atomov sposobna darovati elektrone ali jih sprejeti. Najpogosteje to opazimo v raztopini in kristalih soli. Kristalna rešetka vsebuje tudi skoraj nepremične naelektrene delce, brez kinetična energija. In ker v kristalu ni možnosti za gibanje, se reakcija ionov najpogosteje pojavlja v raztopinah.
Ioni v fiziki in kemiji
Fiziki in kemiki aktivno preučujejo ione iz več razlogov. Prvič, ti delci so prisotni v vseh znanih agregatna stanja snovi. Drugič, energijo ločevanja elektronov od atoma lahko izmerimo, da bi jo uporabili v praktičnih dejavnostih. Tretjič, v kristalih in raztopinah se ioni obnašajo drugače. In četrtič, ioni omogočajo vodenje električnega toka in fizikalno-kemijske lastnosti raztopin so odvisne od koncentracije ionov.
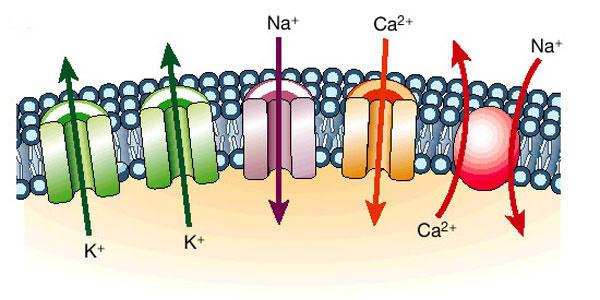
Ionske reakcije v raztopini
Natančneje je treba razmisliti o samih raztopinah in kristalih. V kristalih soli obstajajo ločeno locirani pozitivni ioni, npr. Natrijevi kationi in negativni, klorov anioni. Kristalna struktura je neverjetna: zaradi sil elektrostatične privlačnosti in odbojnosti so ioni usmerjeni na poseben način. V primeru. T natrijev klorid tvorijo ti diamantno kristalno rešetko. Tukaj je vsak natrijev kation obdan s 6 kloridnimi anioni. Vsak kloridni anion obkroža 6 klorovih anionov. Zaradi tega je preprosto sol in v hladni in vroči vodi se raztopi skoraj pri enaki hitrosti.

V raztopini tudi ni trdne molekule natrijevega klorida. Vsak od ionov je obdan z dipoli vode in kaotično se giblje po debelini. Prisotnost nabojev in elektrostatičnih interakcij vodi do dejstva, da se raztopine slane vode zamrznejo pri temperaturi, ki je nekoliko nižja od nič, in vre pri temperaturi nad 100 stopinj. Poleg tega, če v raztopini obstajajo druge snovi, ki lahko vstopijo v kemično vez, se reakcija ne zgodi s sodelovanjem molekul, temveč z ioni. To je ustvarilo doktrino uprizoritve kemijske reakcije.
Izdelki, ki jih dobimo na koncu, se ne tvorijo takoj med interakcijo, ampak se postopoma sintetizirajo iz vmesnih proizvodov. Študija ionov je omogočila razumevanje, da reakcija poteka natančno po načelih elektrostatičnih interakcij. Njihov rezultat je sinteza ionov, ki elektrostatično vplivajo na druge ione, kar ustvarja končni ravnotežni reakcijski produkt.
Povzetek
Tak delec kot ion je električno nabitega atom ali skupina atomov, ki se pridobi med izgubo ali pridobitvijo elektronov. Najpreprostejši ion je vodik: če izgubi en elektron, je le jedro z nabojem +1. Povzroča kislo okolje raztopin in medijev, kar je pomembno za delovanje bioloških sistemov in organizmov.
Ioni imajo lahko pozitivne in negativne naboje. Zaradi tega v raztopinah vsak delec vstopa v elektrostatično interakcijo z dipoli vode, kar ustvarja tudi pogoje za življenje in prenos signalov s celicami. Poleg tega se ionska tehnologija še naprej razvija. Na primer, ustvarjeni so bili ionski motorji, ki so že opremili 7 vesoljskih misij NASA.