Skupno stanje snovi. Sprememba stanja snovi
Vse snovi lahko obstajajo v eni od štirih vrst. Vsak od njih je določeno agregatno stanje snovi. V naravi Zemlje je le ena predstavljena v treh od njih hkrati. To je voda. Je lahko videti in izhlapeti, stali se in strdi. To je para, voda in led. Znanstveniki so se naučili spreminjati agregacijo snovi. Največja težava za njih je le plazma. Ta pogoj zahteva posebne pogoje.

Kaj je to, od česa je odvisno in kako je značilno?
Če se je telo preselilo v drugo agregatno stanje snovi, to ne pomeni, da se je pojavilo nekaj drugega. Snov ostaja enaka. Če ima tekočina vodne molekule, bodo enake s paro z ledom. Samo njihova lokacija, hitrost gibanja in sile medsebojnega delovanja se bodo spremenile.
Ad
Pri proučevanju teme »Agregatne države (8. razred)« so upoštevane le tri. To je tekoči plin in trdno. Njihove manifestacije so odvisne od fizičnih pogojev okolja. Značilnosti teh stanj so predstavljene v tabeli.
| Ime agregacijskega stanja | trdno telo | tekočine | plina |
| Njegove lastnosti | ohranja obliko z volumnom | ima konstanten volumen, ima obliko plovila | nima stalne prostornine in oblike |
| Ureditev molekul | v mrežnih točkah | nenavadno | kaotično |
| Razdalja med njimi | primerljive z velikostjo molekul | približno enako velikosti molekul | bistveno večji od njihove velikosti |
| Kako se molekule premikajo | lebdite okoli rešetke | ne premikajte se od mesta ravnotežja, ampak včasih naredite velike skoke | naključno s priložnostnimi trki |
| Kako delujejo | močno privlači | močno privlači drug drugega | ne pritegnejo, se ob udarcu pojavijo odbojne sile |
Prvo stanje: trdno
Njegova temeljna razlika je, da imajo molekule strogo določen prostor. Ko govorijo o trdnem agregacijskem stanju, se pogosto sklicujejo na kristale. V njih je mrežna struktura simetrična in strogo periodična. Zato je vedno ohranjeno, kako daleč se telo ne bi širilo. Oscilacijsko gibanje molekul snovi ni dovolj, da bi uničilo to mrežo.
Vendar pa obstajajo tudi amorfna telesa. Pomanjkata strogo strukturo v razporeditvi atomov. Lahko so kjerkoli. Toda ta prostor je tako stabilen kot v kristalinskem telesu. Razlika med amorfnimi in kristaliničnimi snovmi je v tem, da nimajo specifičnega tališča (strjevanja), za njih pa je značilna pretočnost. Živahni primeri teh snovi: steklo in plastika.
Ad
Drugo stanje: tekočina
To agregativno stanje snovi je križišče med trdno snovjo in plinom. Zato združuje nekatere lastnosti prvega in drugega. Razdalja med delci in njihova interakcija je podobna tisti, ki je bila pri kristalih. Toda lokacija in premik bliže plinu. Zato tekočina ne ohranja oblike, ampak se razprostira preko posode, v katero se vlije.
Tretja država: plin
Za znanost, imenovano "fizika", agregatno stanje v obliki plina ni na zadnjem mestu. Konec koncev, raziskuje svet okoli sebe in zrak v njem je zelo pogost.
Posebnosti tega stanja so, da so sile interakcije med molekulami praktično odsotne. To pojasnjuje njihovo prosto gibanje. Zaradi tega plinasta snov zapolni celotno količino, ki ji je dana. In v tem stanju lahko prenesete vse, morate samo povečati temperaturo na želeno vrednost.
Ad
Četrto stanje: plazma
To agregatno stanje snovi je plin, ki je v celoti ali delno ioniziran. To pomeni, da je število negativno in pozitivno nabitih delcev v njem skoraj enako. To se zgodi, ko se plin segreje. Potem pride do ostrega pospeševanja procesa toplotne ionizacije. Leži v tem, da so molekule razdeljene na atome. Slednji se nato spremenijo v ione.

V okviru vesolja je takšno stanje zelo pogosto. Ker vsebuje vse zvezde in okolje med njimi. V mejah zemeljske površine se zgodi zelo redko. Razen ionosfere in sončnega vetra je plazma možna le med nevihto. V bliskavici nastajajo taki pogoji, v katerih plini ozračja preidejo v četrto stanje snovi.
Vendar to ne pomeni, da plazma ni ustvarjena v laboratoriju. Prva stvar, ki je bila sposobna razmnoževati, je odvajanje plina. Zdaj plazma napolni fluorescentne luči in neon oglaševanje.

Kako poteka prehod med državami?
Če želite to narediti, morate ustvariti nekatere pogoje: konstanten tlak in določeno temperaturo. V tem primeru spremembo agregatnih stanj snovi spremlja sproščanje ali absorpcija energije. Poleg tega se ta prehod ne dogaja s svetlobno hitrostjo, temveč zahteva določeno časovno obdobje. Ves ta čas morajo biti pogoji nespremenjeni. Prehod poteka z istočasnim obstojem snovi na dva načina, ki vzdržujeta toplotno ravnovesje.
Ad
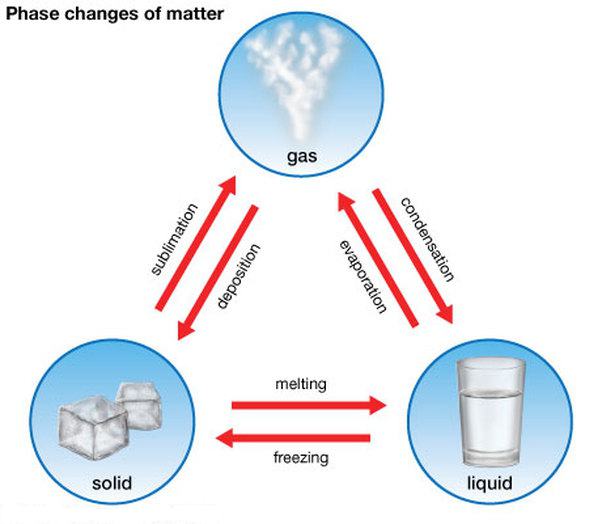
Prve tri snovi snovi lahko gredo ena v drugo. Obstajajo neposredni in obratni procesi. Imajo naslednja imena:
- taljenje (od trdnega do tekočega) in kristalizacije , kot je taljenje ledu in utrjevalne vode;
- izhlapevanje (od tekočega v plinasto) in kondenziranje , primer je izhlapevanje vode in njena proizvodnja iz pare;
- sublimacija (od trdnega v plinasto) in desublimacija , na primer izhlapevanje suhe arome za prvo in zmrzovanje na steklu do drugega.
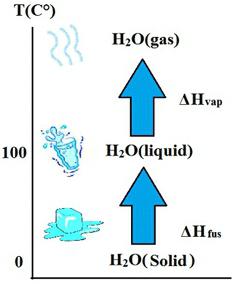
Fizika taljenja in kristalizacije
Če se trdna snov segreje, potem se pri določeni temperaturi, imenovani tališče določene snovi, začne sprememba agregatnega stanja, imenovana taljenje. Ta proces prihaja z absorpcijo energije, ki se imenuje količina toplote in je označena s črko Q. Da bi jo izračunali, morate poznati specifično toploto fuzije , ki jo označujemo z λ . Formula vsebuje naslednji izraz:
Q = λ * m , kjer je m masa snovi, ki sodeluje pri taljenju.
Če pride do obratnega procesa, to je kristalizacije tekočine, se pogoji ponovijo. Edina razlika je, da se energija sprosti, v formuli pa se pojavi znak minus.
Fizika izhlapevanja in kondenzacije
S stalnim segrevanjem snovi se bo postopoma približevala temperaturi, pri kateri se bo začela intenzivna izhlapevanja. Ta proces se imenuje uparjanje. Ponovno je značilna absorpcija energije. Samo za njegov izračun je potrebno poznati specifično toploto uparjanja r . Formula bo:
Q = r * m .
Obratni proces ali kondenzacija se pojavi s sprostitvijo istega toplote. Zato se v formuli ponovno pojavi minus.