Stopnja in konstanta hidrolize
Če upoštevamo dve glavni veji kemijske znanosti, anorganske in organske kemije, se izkaže, da v njih ne boste našli preveč točk stika. Vendar pa obstaja en proces na resnično globalni ravni, ki združuje anorganske in organske snovi. To je proces hidrolize.
Voda je univerzalno topilo
Hidroliza je interakcija snovi z vodo, v kateri sestavni deli kemičnih spojin tvorijo reakcijske produkte z vodikovimi ioni in hidroksilnimi skupinami molekul H 2 O. Ker je 79% planeta in do 80% mase vseh živih organizmov voda, postane jasno, da je reakcija hidroliza pokriva vse manifestacije naravnih procesov, začenši z uničevanjem kamnin in konča s presnovo na vseh sedmih stopnjah organiziranosti žive snovi, od molekularne do biosferične.
Ad

Matematični jezik hidrolize
Bolj ko je kemijski proces zapleten, večje je število formul in izračunov. Za obe vrsti izmenjevalnih reakcij snovi z vodo, tako v organski kot anorganski kemiji, se uporabljajo matematične vrednosti - to je stopnja in konstanta hidrolize, označena kot α g in K g. Njihove vrednosti se izračunavajo in uporabljajo v tehnoloških postopkih organske sinteze, na primer pri sladkorju škrob, hidroliza lesa, umiljenje maščob.
Kakšna je stopnja hidrolize
Čim hitreje snov reagira z vodo, več hidroliziranih molekul bo v takšni raztopini. Razmerje med njihovim številom in skupnim številom delcev kemijske spojine v raztopini se imenuje stopnja hidrolize. V anorganski kemiji je običajno označen kot h, v organskem α g . Izraža se v delih enote ali v odstotkih. Na primer, če se 2 mol snovi raztopi v vodi in hidrolizira 0,01 mol, potem je h = 0,01 / 2 = 0,005 ali 0,5%.
Ad

Konstanta hidrolize
Ta vrednost kaže na sposobnost snovi za hidrolizo. Višja kot je, hitreje so molekule raztopine v interakciji z vodikovimi ioni in hidroksilnimi skupinami vode. Označen je kot K g , izraz za konstanto hidrolize lahko predstavimo s formulo:
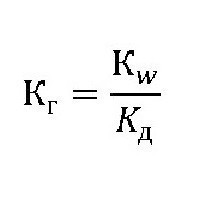
kjer je: K w ionski produkt vode [H + ] * [OH-];
K d - disociacijska konstanta (cepitev) raztopine.
Za organske spojine stopnja in konstanta hidrolize sta povezani s formulo:
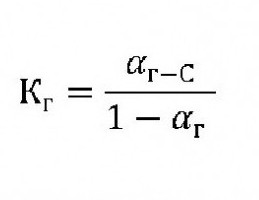
kjer:
K g - stalna hidroliza.
C je koncentracija ionov v topilu.
α g - stopnja hidrolize.
Značilnosti hidrolize organskih spojin
Reakcije izmenjave z vodo v beljakovinah, ogljikovih hidratih in maščobah so večstopenjske in težavne. Zato je konstanta hidrolize, katere formula je:
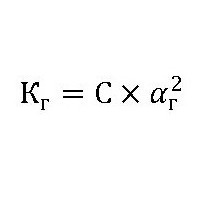
kjer je: S koncentracija raztopljene snovi (mol / l).
α g - stopnja hidrolize je odvisna tudi od narave katalizatorja (encima), njegove aktivnosti in temperature raztopine.
Na primer, v tehnološkem procesu izmenjave celuloznih reakcij z vodo, strokovnjaki izračunajo vse parametre, med katerimi so glavna konstanta hidrolize in konstanta hitrosti hidrolize. Za slednjo vrednost se takšne komponente uvedejo kot: α– relativna aktivnost katalizatorja, N - njena normalnost, tj. Koncentracija, b - sposobnost hidroliziranja celuloze in λ - indikator, ki označuje odvisnost hitrosti reakcije od temperature vode: k = α * N * b * λ
Ad

Inženirji kemijskih procesov pri reakcijah hidrolize maščob upoštevajo njegovo reverzibilnost. Za premik ravnotežja v desno, v smeri tvorbe želenih produktov, npr. Glicerola, se v industrijski sintezi uporabi alkalija. V tem primeru se hidroliza maščob odvija skoraj do konca: natrijevega hidroksida ali kalijeve pretvorite polibazične karboksilne kisline, ki nastanejo v soli in tako preprečijo prehod obrnjene reakcije tvorbe maščobe. Podobna metoda se uporablja, kadar voda razgrajuje estre v reakciji saponifikacije. S povečanjem koncentracije hidroksidnih ionov in redčenjem reakcijske zmesi povečata stopnjo hidrolize α in s tem donos reakcijskih produktov alkoholov in organskih kislin.
Razgradnja anorganskih snovi v vodi
Iz praktičnega pomena so reakcije hidrolize kemičnih spojin, ki spadajo v razred soli. Znano je, da so produkti izmenjave med kislinami in bazami. Torej bo njihova hidroliza odvisna od tega, kateri hidroksidi in kisline tvorijo soli. In tukaj bo ključni koncept teorije elektrolitske disociacije o moči elektrolitov. Konstanta in stopnja hidroliza soli odvisno od sestave ionov, ki tvorijo njihove molekule.
Ad

Zakaj je pH soli drugačen
Poskusi kažejo, da so lahko raztopine različnih soli kisle (pH <7), nevtralne (pH = 7) ali alkalne (pH> 7), čeprav v molekulah ni vodikovih ali hidroksilnih ionov. Razlago teh protislovij je treba iskati v procesu njihove reakcije z vodo:
Sol + voda <=> kislina + baza.
To ravnotežje ustreza konstanti hidrolize:
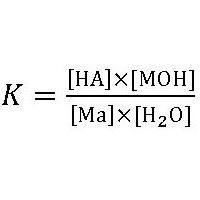
kjer je: ON kislina,
PWS - Fundacija
MA je sol.
Glede na to, da je koncentracija vode v razredčenih raztopinah konstantna, bo konstanta hidrolize: 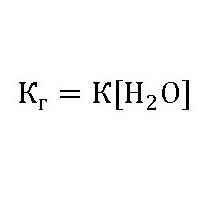 Poenostavimo prvo formulo in dobimo vrednost:
Poenostavimo prvo formulo in dobimo vrednost: 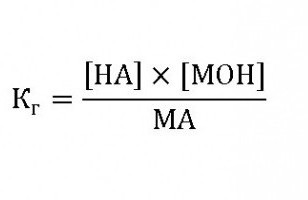 To je stalna hidroliza soli - Kg. Njegova vrednost označuje sposobnost razgradnje snovi z vodo, večja je, hitrejša (pri isti temperaturi in koncentraciji soli) reakcija. Ker je konstanta hidrolize, katere formula je Kg = [OH] × [MA], koncentracija hidroksilnih ionov:
To je stalna hidroliza soli - Kg. Njegova vrednost označuje sposobnost razgradnje snovi z vodo, večja je, hitrejša (pri isti temperaturi in koncentraciji soli) reakcija. Ker je konstanta hidrolize, katere formula je Kg = [OH] × [MA], koncentracija hidroksilnih ionov: 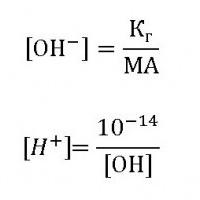 Za večino soli je hidroliza reverzibilni proces. Na vrednost α vplivajo temperatura in koncentracija raztopine soli. Višja sta oba parametra, večja je stopnja in konstanta hidrolize. To je posledica dejstva, da se pri segrevanju Cn + in Son- no močno povečata. Povečanje koncentracije vode, kot je razvidno iz enačbe hidrolize, premakne ravnotežje v desno. Vendar pa je bilo v dejanskih kemijskih procesih dokazano, da h soli, ki jih tvori šibka kislina in baza, niso odvisne od razredčitve raztopine.
Za večino soli je hidroliza reverzibilni proces. Na vrednost α vplivajo temperatura in koncentracija raztopine soli. Višja sta oba parametra, večja je stopnja in konstanta hidrolize. To je posledica dejstva, da se pri segrevanju Cn + in Son- no močno povečata. Povečanje koncentracije vode, kot je razvidno iz enačbe hidrolize, premakne ravnotežje v desno. Vendar pa je bilo v dejanskih kemijskih procesih dokazano, da h soli, ki jih tvori šibka kislina in baza, niso odvisne od razredčitve raztopine.

Stopnja hidrolize in TED
V luči teorije elektrolitska disociacija ravnotežje procesa hidrolize je odvisno od že znane vrednosti h ali αg - stopnje hidrolize. Če sol šibke kisline razpade z vodo, na primer Na2CO3 ali K2S, potem 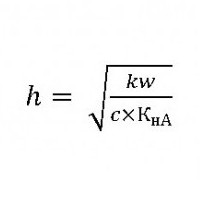 Reakcijske raztopine takšnih soli bodo alkalne. Določi se lahko z uporabo brezbarvnega indikatorja fenolftaleina, ki s prebitkom hidroksilnih ionov postane rdeč. Vijoličen lakmus v alkalni raztopini dobi modro barvo, metil oranž pa postane rumena. Natrijev karbonat, kot močan elektrolit, ko se raztopi v vodi, se popolnoma razgradi v kovinske katione in anione kislega ostanka. Prav slednji medsebojno delujejo z vodikovimi ioni in hidroksokrupi.
Reakcijske raztopine takšnih soli bodo alkalne. Določi se lahko z uporabo brezbarvnega indikatorja fenolftaleina, ki s prebitkom hidroksilnih ionov postane rdeč. Vijoličen lakmus v alkalni raztopini dobi modro barvo, metil oranž pa postane rumena. Natrijev karbonat, kot močan elektrolit, ko se raztopi v vodi, se popolnoma razgradi v kovinske katione in anione kislega ostanka. Prav slednji medsebojno delujejo z vodikovimi ioni in hidroksokrupi.

Natrijevi kationi ne morejo vezati iona OH– v molekule natrijevega hidroksida, ker je močan elektrolit in nikoli ni prisoten kot molekula v raztopini. Hkrati se karbonatni ioni vežejo na H +, da tvorijo šibek elektrolit - karbonsko kislino - dokler se v raztopini ne vzpostavi ravnovesje.
Med hidrolizo soli šibkih baz AlCl3, FeSO4: 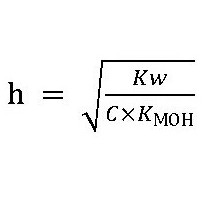 Reakcija raztopin takšnih soli bo kisla, pH je manjši od 7. V tem primeru nastane šibek elektrolit Al (OH) 3. Del vodikovih ionov, medtem ko ostane prost, povzroči zakisljevanje raztopine: lakmusov indikator to zmanjša tako, da spremeni vijolično barvo v rdečo. Posledično se ionsko ravnotežje disociacije vode premakne in nastane presežek vodikovih ionov.
Reakcija raztopin takšnih soli bo kisla, pH je manjši od 7. V tem primeru nastane šibek elektrolit Al (OH) 3. Del vodikovih ionov, medtem ko ostane prost, povzroči zakisljevanje raztopine: lakmusov indikator to zmanjša tako, da spremeni vijolično barvo v rdečo. Posledično se ionsko ravnotežje disociacije vode premakne in nastane presežek vodikovih ionov.
 Če soli šibke baze in šibke kisline (NH4) CH3COO, NH4CN vstopijo v reakcijo izmenjave z vodo, potem
Če soli šibke baze in šibke kisline (NH4) CH3COO, NH4CN vstopijo v reakcijo izmenjave z vodo, potem 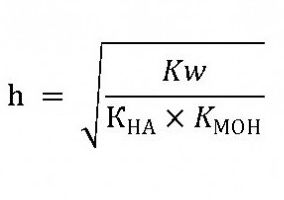 Raztopine takih soli se hidrolizirajo posebej enostavno in njihov pH bo odvisen od stopnje disociacije tako kisline kot baze. Če je koncentracija ionov H + večja, bo pH nižji od 7. Pri presežku hidroksida bo pH večji od 7, pri približno enaki količini pa bo raztopina postala nevtralna. Tako pride do hidrolize soli, kadar so njihovi ioni, ki nastanejo kot posledica elektrolitske disociacije, načini za tvorbo šibke vode (nizko disociirani elektroliti).
Raztopine takih soli se hidrolizirajo posebej enostavno in njihov pH bo odvisen od stopnje disociacije tako kisline kot baze. Če je koncentracija ionov H + večja, bo pH nižji od 7. Pri presežku hidroksida bo pH večji od 7, pri približno enaki količini pa bo raztopina postala nevtralna. Tako pride do hidrolize soli, kadar so njihovi ioni, ki nastanejo kot posledica elektrolitske disociacije, načini za tvorbo šibke vode (nizko disociirani elektroliti).
Dodamo tudi naslednje: 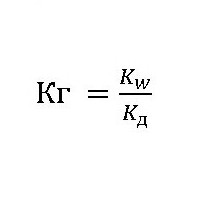 Konstanta hidrolize soli, določena s to formulo, kaže, da je Ostwaldov zakon, ki ima obliko:
Konstanta hidrolize soli, določena s to formulo, kaže, da je Ostwaldov zakon, ki ima obliko:
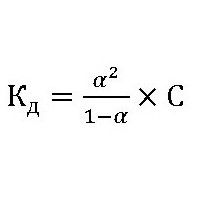 ne le za elektrolitsko disociacijo, temveč tudi za proces razgradnje snovi z vodo. Če sol nastane z močno bazo in močno kislino, se v vodnih raztopinah ne hidrolizira, saj se ne pojavi nastanek šibkega elektrolita. To pomeni, da so štiri vrste ionov stalno prisotne v raztopini v prostem stanju: to so kationi kovine in vodika ter anioni hidroksilnih skupin in kislih ostankov. Za raztopine takšnih soli je nemogoče napisati skrajšano ionsko enačbo in celotna reakcija se zmanjša na tvorbo vodnih molekul.
ne le za elektrolitsko disociacijo, temveč tudi za proces razgradnje snovi z vodo. Če sol nastane z močno bazo in močno kislino, se v vodnih raztopinah ne hidrolizira, saj se ne pojavi nastanek šibkega elektrolita. To pomeni, da so štiri vrste ionov stalno prisotne v raztopini v prostem stanju: to so kationi kovine in vodika ter anioni hidroksilnih skupin in kislih ostankov. Za raztopine takšnih soli je nemogoče napisati skrajšano ionsko enačbo in celotna reakcija se zmanjša na tvorbo vodnih molekul.
Izračun amonijevega klorida v hidrolizi
Za določitev te vrednosti s šibko osnovo in močno kislino uporabite razmerje: 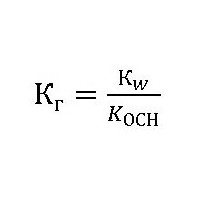 Kw - proizvod vode;
Kw - proizvod vode;
COSN je konstanta disociacije baze NH4OH, ki nastane med hidrolizo.
Nato bo stalna hidroliza amonijevega klorida enaka: 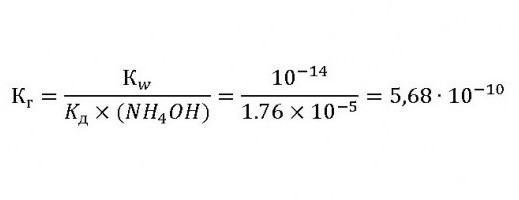
To dokazuje, da je pri hidrolizaciji raztopina te soli kisla.