Peptidno spajanje je osnova za primarno strukturo proteina. Karakterizacija in tvorba peptidnih vezi
Peptidna vez je močna povezava med fragmenti dveh aminokislin, ki sta osnova za tvorbo linearnih struktur proteinov in peptide. V takšnih molekulah se vsaka aminokislina (razen terminalnih) kombinira s prejšnjo in naslednjo.
Glede na število povezav lahko peptidne vezi ustvarijo dipeptide (sestavljene iz dveh aminokislin), tripeptide (od treh), tetrapeptide, pentapeptide itd. Kratke verige (od 10 do 50 monomerov) se imenujejo oligopeptidi, dolge pa - polipeptidi in proteini ( molska masa več kot 10 tisoč.
Značilnosti peptidne vezi
Peptidna vez je kovalentna kemijska spojina med prvim ogljikovim atomom ene aminokisline in dušikovim atomom drugega, ki je rezultat interakcije alfa-karboksilne skupine (COOH) z alfa-amino skupino (NH2). Ko se to zgodi, se nukleofilna substitucija OH-hidroksila na amino skupini, iz katere je ločen vodik. Tako nastane ena CN vez in vodna molekula.
Ad
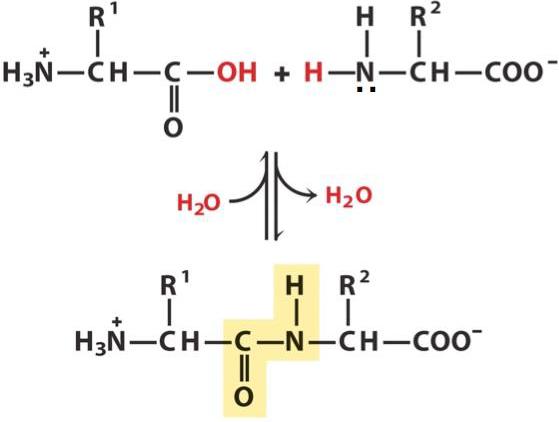
Ker se med reakcijo izgubijo nekatere komponente (OH skupine in vodikov atom), se peptidne enote ne imenujejo več aminokisline, temveč aminokislinski ostanki. Zaradi dejstva, da slednje vsebujejo vsaka 2 ogljikova atoma, v peptidni verigi poteka izmenjava vezi C-C in CN, ki tvorijo peptidno ogrodje. Na straneh so aminokislinski radikali. Razdalja med atomi ogljika in dušika se giblje od 0,132 do 0,127 nm, kar kaže na neomejeno vez.
Peptidna vez je zelo močna oblika kemijske interakcije. Pod standardnimi biokemičnimi pogoji, ki ustrezajo celičnemu okolju, ni podvržen samouničenju.
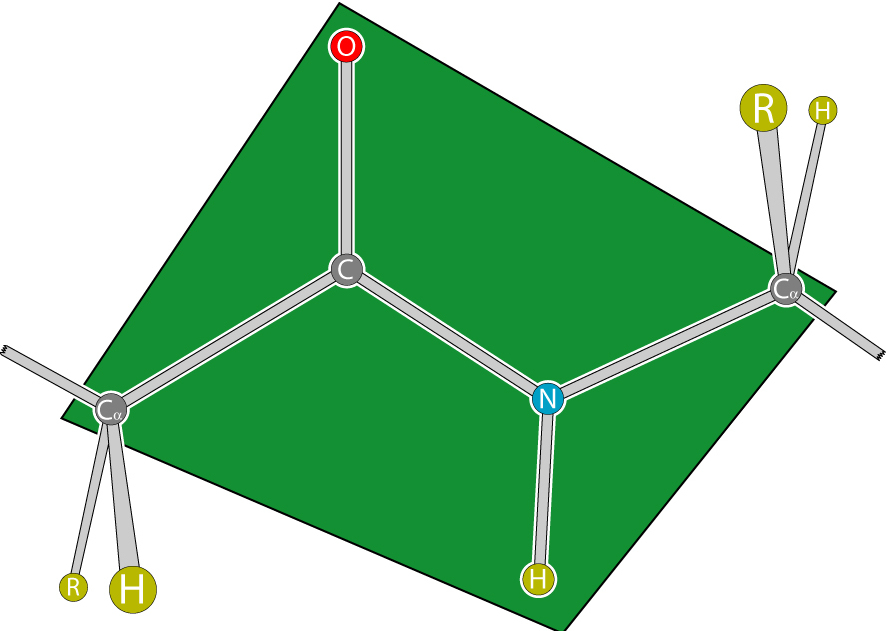
Za peptidno vez proteinov in peptidov je značilna lastnost koplanarnosti, saj so vsi atomi, ki sodelujejo pri njeni tvorbi (C, N, O in H), v isti ravnini. Ta pojav je pojasnjen s togostjo (t.j. nemožnostjo vrtenja elementov okoli vezi), ki je posledica resonančne stabilizacije. V aminokislinski verigi med ravninami peptidnih skupin spadajo α-ogljikovi atomi, povezani z radikali.
Ad
Vrste konfiguracij
Glede na položaj alfa-ogljikovih atomov glede na peptidno vez, lahko slednja ima dve konfiguraciji:
- "cis" (na eni strani);
- "trance" (iz različnih strani).
Trans oblika je bolj odporna. Včasih so konfiguracije označene z lokacijo radikalov, ki ne spreminjajo bistva, saj so povezani z alfa-ogljikovimi atomi.
Pojav resonance
Posebnost peptidne vezi je, da je 40% dvojna in je lahko v treh oblikah:
- Ketol (0,132 nm) - CN-vez je stabiliziran in popolnoma en.
- Prehodna ali mezomerno - vmesna oblika ima delno nedoločeno.
- Enol (0.127 nm) - peptidna vez postane popolnoma dvojna, spojina C - O pa popolnoma enojna. V tem primeru kisik dobi delno negativen naboj in atom vodika - delno pozitiven.
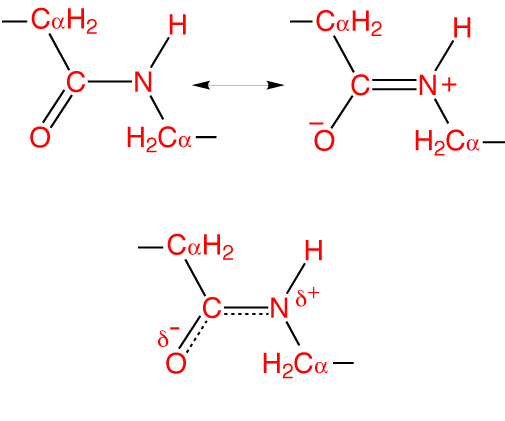
Ta lastnost se imenuje resonančni učinek in jo razlagamo s delokalizacijo kovalentne vezi med atomi ogljika in dušika. V tem primeru hibridne sp 2 orbitale tvorijo elektronski oblak, ki se širi na atom kisika.
Nastanek peptidne vezi
Oblikovanje peptidne vezi je tipična reakcija polikondenzacije, ki je termodinamično neugodna. V naravnih pogojih se ravnotežje premakne proti prostim aminokislinam, zato je za sintezo potreben katalizator, ki aktivira ali spreminja karboksilno skupino za lažje vzdrževanje hidroksila.
V živi celici nastane peptidna vez v centru za sintezo beljakovin, kjer specifični encimi delujejo kot katalizator, ki delajo s porabo energije visokoenergetskih vezi.