Kalcijev karbid: lastnosti in uporaba. Pridobivanje acetilena
Karbidi so skupina anorganskih ogljikovih spojin s kovinami, pa tudi s silicijem ali borom (ker ti elementi kažejo kovinske lastnosti). Kalcijev karbid je ena izmed najbolj zahtevnih snovi te skupine. O lastnostih in uporabi spojine preberite spodaj.
Prejemanje zgodovine
Kalcijev karbid je spojina, ki se pogosto uporablja v sodobni industriji. Leta 1862 je nemški kemik Friedrich Weler prvič sintetiziral molekulo te snovi. Pridobivanje kalcijevega karbida je potekal na naslednji način. Znanstvenik je pripravil kalcijevo talino s cinkom in jo nato ogreval s premogom. Rezultat je karbid. Kemična formula spojine je CaC2. Industrijsko metodo proizvodnje karbidov je predlagal znanstvenik Moissan leta 1892. Druga imena snovi so kalcijev acetilid ali kalcijev karbonat. Kristalna rešetka spojine je naslednja:
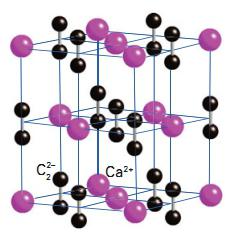
Fizične lastnosti
Glede na njegove fizikalne lastnosti je kalcijev karbid kristalinična snov s tališčem 2300 o C. Ta številka velja samo za čiste spojine. Karbide, ki vsebujejo nečistoče, lahko imajo druge talilne točke. Glavno agregatno stanje snovi je trdno in barva se spreminja od sive do rjave.
Kemijske lastnosti
Kalcijev karbid dobro absorbira vodo. Ta postopek spremlja reakcija kemične razgradnje. Pomembno je, da ima karbidni prah dražljiv učinek na sluznice, kožo in dihal. Zato je treba pri delu s spojino uporabiti plinske maske ali protiprašne respiratorje. Kalcijev karbid v stiku z kisikom pri visoki temperaturi kalcijev karbonat. Reakcija z dušikom vodi do sinteze kalcijevega cianamida. Tudi pri visokih temperaturah kalcijev karbid reagira s klorom, fosforjem, arzenom. Še vedno pa je ena najpomembnejših lastnosti spojine razgradnja z vodo.

Pridobivanje
Proizvodnja kalcijevega karbida je naslednja. Mešani so živo apno in predhodno zdrobljen koks. Nastala zmes se tali v električnih pečeh. Koks in kalcijev oksid se vzamejo v enakih masnih deležih. Postopek poteka pri temperaturi 1900 o C. Talina zapusti peč in se nato vlije v posebne oblike. Nato že strjeni kalcijev karbid zdrobimo in razvrstimo glede na velikost kosov. Granule snovi so razdeljene v štiri frakcije v skladu z njihovimi velikostmi: 25 × 80, 15 × 25, 8 × 15, 2 × 8, ki jih določa GOST 1460-56. Tehnični kalcijev karbid po svoji sestavi vsebuje 75-80% glavne snovi. Delež nečistoč, kot so ogljik, apno in drugi, predstavlja do 25% skupne mase mešanice. Poleg tega sulfid in kalcijev fosfid, ki ju vsebuje tehnični karbid, povzročata precej neprijeten vonj. Predstavljajte si reakcijo pridobivanja CaC 2 : CaO + 3C → CaC 2 + CO ↑. Nastajanje kalcijevega acetilida spremlja absorpcija toplote. Zato je logično domnevati, da reakcija njenega razkroja, nasprotno, gre z sproščanjem energije.

Prevoz in skladiščenje
Ker se vlaga takoj razgradi s sproščanjem velikih količin toplote in nastajanjem eksplozivnega acetilenskega plina, je treba snov shraniti v hermetično zaprtih sodih ali pločevinkah. Ne smemo pozabiti, da je acetilen lažji od zraka in se lahko kopiči v zgornjih predelih prostora. Ta plin, poleg narkotičnega delovanja, ima tudi sposobnost samovžiga. Zato je potrebno skrbno uporabljati kalcijev karbid. Posebno pozornost namenjamo pakiranju v proizvodnji. Končna snov se postavi v posebne bobne (posoda, ki spominja na pločevinke). Takšna embalaža zahteva skrbno odpiranje. Uporabiti je treba orodje, ki ne vodi do nastajanja isker (kladivo ali posebni nož). V primeru karbida na koži ali sluznicah, morate prizadeto območje takoj sprati z vodo in ga obdelati z vazelinom ali maščobno kremo. Prevoz priključka se izvaja samo s pokritim vrste prevoza. Dobava karbida v zraku je prepovedana. Prostori, kjer je shranjen CaC 2 , morajo biti dobro prezračeni. Prav tako ni dovoljeno shranjevati karbida skupaj z drugimi kemikalijami. To lahko vodi do neželenih in morda nevarnih reakcij. Rok uporabnosti karbida je šest mesecev.

Uporaba
Obseg kalcijevega karbida je zelo širok. Najprej je to industrijska sinteza. Kalcijev karbid se uporablja za proizvodnjo sintetične gume, ocetne kisline, acetona, etilena, vinilklorida, stirena. Prav tako se uporablja pri pripravi kalcijevega cianamida. Ta snov je dragocena za uporabo pri sintezi različnih gnojil in cianidnih snovi. V kmetijstvu vsak agronom pozna takšno ime kot regulator karbid-karbamid. Uporablja se za uravnavanje rasti rastlin. Za pridobitev je uporabljen tudi kalcijev karbid. Poleg tega se ta spojina uporablja pri proizvodnji kalcijevega cianamida. Ta reakcija temelji na segrevanju kalcijevega karbida z dušikom. Izterjava alkalijske kovine tudi brez uporabe snovi, ki smo jo opisali. Kalcijev karbid se uporablja v procesu varjenja s plinom. Na primer, karbidne svetilke se pogosto uporabljajo. Načelo njihovega dela temelji na interakciji v posebni posodi s karbidom z vodo in izgorevanjem na izhodu iz aparature končne reakcijske snovi - acetilena. Poglejte fotografijo karbidne svetilke.

Proizvodnja acetilena
Ena od najpomembnejših aplikacij kalcijevega karbida je njegova uporaba pri proizvodnji acetilena. Za to odkritje je zaslužen tudi nemški kemik Friedrich Vehler. Osnova tega industrijskega procesa je reakcija razgradnje karbida pod vplivom vode. CaC2 + 2H2O → C2H2 + Ca (OH) 2 ↓. Na izhodu se tvori plin acetilen in hidrirano apno, oborila. Proces spremlja sproščanje velike količine toplote. Količina plina na izhodu je odvisna od tega, kako čist kalcijev karbid se uporablja za reakcijo. Tako nastali acetilen ima lahko drugačen volumen - 1 kg začetne snovi lahko da 235 do 290 litrov plina. Kar zadeva hitrost reakcije, je odvisna tako od majhnega odstotka nečistoč v kalcijevem karbidu kot tudi od temperature vode ter njene čistosti. Če upoštevamo teoretično reakcijo proizvodnje acetilena iz karbida, potem je za 1 kg karbida dovolj 560 ml vode. Vendar se v praksi količina vode za reakcijo poveča. Na 1 kg kalcijevega karbida v pogojih industrijske sinteze je potrebno od 5 do 20 litrov vode. Ta količina je potrebna za zagotovitev boljšega hlajenja acetilena in za zagotovitev optimalne varnosti med delovanjem. Spodaj je nemški kemik Friedrich Veler.

Laboratorijske izkušnje z acetilenom
Številni pouk kemije v šoli pozna reakcijo interakcije karbidne vode. Običajno nam ta izkušnja omogoča, da prikažemo reakcijo za pridobitev acetilena, pa tudi njegove fizikalne in kemijske lastnosti. Hkrati se proces razvijanja plina odvija precej močno, tako da se cevka, ki izloča acetilen iz bučke z aktivnimi snovmi, postavi v posodo z vodo. To zagotavlja manj aktivno in hitro premikanje plina. Poleg tega lahko v laboratoriju uporabite drug način, da ne preveč silovite reakcije razgradnje takšnih spojin kot karbid. Acetilen v tem primeru gre enakomerno in mirno. Če želite to narediti, namesto vode, morate vzeti nasičeno raztopino soli. Tudi v laboratoriju je treba pri izvedbi te reakcije v karbid, ki se nahaja v volumetrični bučki, previdno dodati vodo in ne obratno.