Aldehidi in ketoni. Formula, priprava, uporaba
Med organskimi spojinami, ki vsebujejo kisik, sta izjemno pomembna dva razreda snovi, ki se vedno preučujeta skupaj za podobnost v strukturi in manifestiranih lastnostih. To so aldehidi in ketoni. Prav te molekule so osnova mnogih kemičnih sintez in njihova struktura je dovolj zanimiva, da jo je mogoče preučevati. Poglejmo podrobneje, kaj so ti razredi spojin.

Aldehidi in ketoni: splošne značilnosti
Z vidika kemije bi moral razred aldehidov vključevati organske molekule, ki vsebujejo kisik v funkcionalni skupini -СON, imenovani karbonil. Splošna formula v tem primeru bo izgledala takole: R-COH. Po svoji naravi so lahko tako omejevalne kot nenasičene. Med njimi so tudi aromatični predstavniki, skupaj z alifatskimi. Število ogljikovih atomov v radikalni verigi se spreminja v precej širokih mejah, od enega (formaldehid ali metan) do več deset.
Ketoni vsebujejo tudi karbonilno skupino -CO, vendar ni vezana na vodikov kation, ampak na drugačen radikal, ki je drugačen ali enak tistemu, ki vstopa v verigo. Splošna formula je naslednja: R-CO-R. Očitno je, da so aldehidi in ketoni podobni v prisotnosti funkcionalne skupine te sestave.
Ketoni so lahko tudi omejevalni in nenasičeni, manifestirane lastnosti pa so podobne tesno povezanemu razredu. Obstaja več primerov, ki ponazarjajo sestavo molekul in odražajo sprejete označbe formul obravnavanih snovi.
- Aldehidi: metanal-HCl, butanal-CH3-CH2-CH2-COH, fenilocetni - C6H5-CH2-COH.
- Ketoni: aceton ali dimetil keton - CH3-CO-CH3, metil etil keton - CH3-CO-C2H5 in drugi.
Očitno je, da se ime teh spojin oblikuje na dva načina:
- po racionalni nomenklaturi glede na radikale in pripone razreda -al (za aldehide) in -on (za ketone);
- zgodovinsko gledano.
Če podate splošno formulo za oba razreda snovi, bo postalo jasno, da so to izomeri drug drugega: C n H 2n O. Za sebe so značilne naslednje vrste izomerizma:
- za ketone, strukturo ogljikovodikove verige radikala in položaj skupine -CO;
- za aldehide - le razporeditev atomov v verigi.

Za razlikovanje med predstavniki obeh razredov uporabite kvalitativne reakcije večina, ki nam omogoča identifikacijo aldehida. Ker je kemijska aktivnost teh snovi nekoliko višja zaradi prisotnosti vodikovega kationa.
Molekularna struktura
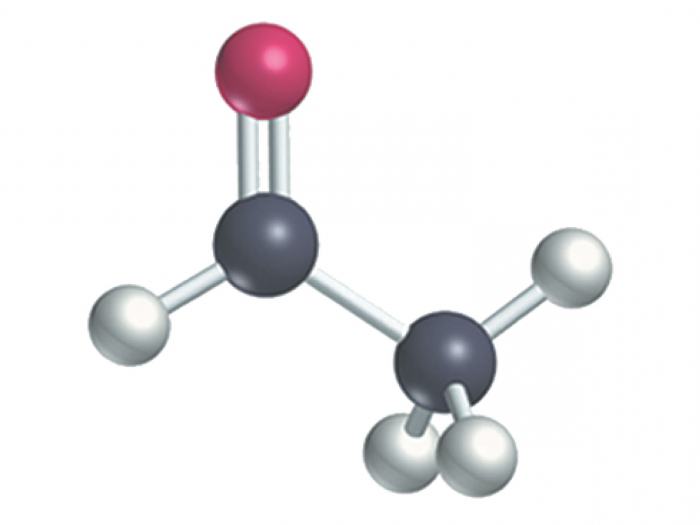
Razmislite, kako izgledajo aldehidi in ketoni v prostoru. Struktura njihovih molekul se lahko odraža v več točkah.
- Ogljikov atom, ki je neposredno vključen v funkcionalno skupino, ima sp 2 hibridizacijo, ki omogoča, da ima del molekule ravno prostorsko obliko.
- V tem primeru je polarnost C = O vezi močna. Kot bolj elektronegativen, kisik prevzame večino svoje gostote, koncentrira delno negativen naboj na sebe.
- V aldehidih je OH vez tudi zelo polarizirana, zaradi česar je vodikov atom mobilen.
Posledično se izkaže, da takšna struktura molekul omogoča, da se obravnavane spojine oksidirajo in zmanjšajo. Formula aldehida in ketona z redistribuirano elektronsko gostoto omogoča napovedovanje reakcijskih produktov, v katerih te snovi sodelujejo.
Zgodovina odkrivanja in študija
Kot mnogi organske spojine šele v 19. stoletju so ljudje uspeli izolirati in proučevati aldehide in ketone, ko so se vitalistični pogledi popolnoma razpadli in postalo jasno, da se te spojine lahko oblikujejo s sintetičnimi, umetnimi sredstvi, brez sodelovanja živih bitij.
Vendar je leta 1661 R. Boyleju uspelo dobiti aceton (dimetil keton), ko je kalcijev acetat izpostavil segrevanju. Vendar ni mogel podrobno preučiti te snovi in jo poimenovati, določiti sistematični položaj med drugim. Šele leta 1852 je Williamson končal to zadevo, nato se je začela zgodovina podrobnega razvoja in kopičenja znanja o karbonilnih spojinah.

Fizične lastnosti
Upoštevajte fizikalne lastnosti aldehidov in ketonov. Začnimo s prvim.
- Glede na stanje agregacije je prvi predstavnik metan, naslednjih enajst je tekočin, več kot 12 atomov ogljika je del trdnih aldehidov normalne strukture.
- Vrelišče: odvisno od števila atomov C, bolj kot so, višje je. Poleg tega je veja razvejana, nižja je temperatura.
- Za tekoče aldehide so indeksi viskoznosti, gostote in loma odvisni tudi od števila atomov. Več jih je, zato so višje.
- Plinasti in tekoči aldehidi se zelo dobro raztopijo v vodi, vendar trdne snovi tega praktično ne morejo storiti.
- Vonj predstavnikov je zelo prijeten, pogosto so to arome cvetja, parfuma, sadja. Samo tisti aldehidi, v katerih je število ogljikovih atomov 1-5, so močno in neprijetno dišeče tekočine.
Če določite lastnosti ketonov, lahko izberete tudi glavne.
- Agregatna stanja: nižji predstavniki so tekočine, bolj masivni so trdne spojine.
- Vonj je oster, neprijeten za vse predstavnike.
- Topnost v vodi je dobra za nižje, odlična je za vse v organskih topilih.
- Hlapne snovi, ta kazalnik presega tiste iz kislin, alkoholov.
- Vrelišče in tališče sta odvisna od strukture molekule, močno se razlikuje glede na število ogljikovih atomov v verigi.
To so glavne lastnosti obravnavanih spojin, ki spadajo v skupino fizikalnih.
Kemijske lastnosti
Najpomembnejša stvar, s katero reagirajo aldehidi in ketoni, so kemijske lastnosti teh spojin. Zato jih smatramo nujno. Najprej se ukvarjamo z aldehidi.
- Oksidacija v ustrezne karboksilne kisline. Splošni pogled na reakcijsko enačbo: R-COH + [O] = R-COOH. Aromatični predstavniki še lažje vstopajo v takšne interakcije in so tudi sposobni oblikovati estre industrijskega pomena. Kot oksidanti se uporabljajo: kisik, Tollensov reagent, bakrov (II) hidroksid in drugi.
- Aldehidi se kažejo kot močna redukcijska sredstva, medtem ko se spreminjajo v omejevalne enodolne alkohole.
- Interakcija z alkoholi za tvorbo produktov acetalov in hemiacetalov.
- Posebne reakcije - polikondenzacija. Tako nastanejo fenolformaldehidne smole, ki so pomembne za kemično industrijo.
- Več posebnih reakcij z naslednjimi reagenti:
- vodno-alkoholne baze;
- Grignardov reagent;
- hidrosulfiti in drugi.
Kakovosten odziv na ta razred snovi je reakcija "srebrnega ogledala". Posledično tvori kovinsko reducirano srebro in ustrezno karboksilno kislino. Zahteva raztopino amoniaka iz srebrovega oksida ali reagenta Tollins.
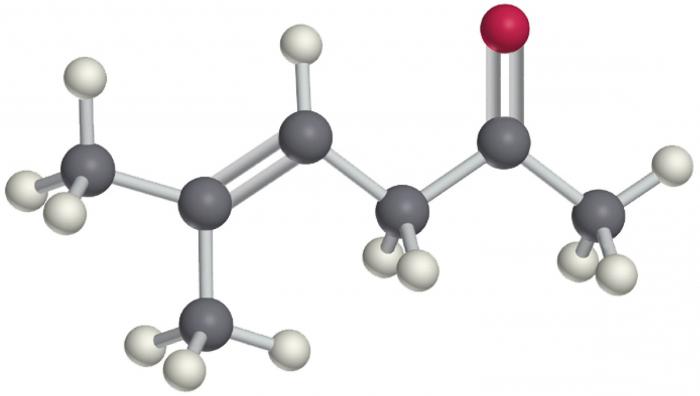
Kemijske lastnosti ketonov
Alkoholi, aldehidi, ketoni so po svojih lastnostih podobni, ker vse vsebujejo kisik. Vendar pa že v fazi oksidacije postane jasno, da so alkoholi najbolj aktivne in lahko občutljive spojine. Ketoni so najtežje oksidirati.
- Oksidativne lastnosti. Posledično nastanejo sekundarni alkoholi.
- Hidrogeniranje vodi tudi do zgoraj navedenih izdelkov.
- Keto-enolna tavtomerija je posebna specifična lastnost ketonov, da vzamejo beta obliko.
- Reakcije aldolne kondenzacije z nastankom beta-ketospirtov.
- Tudi ketoni lahko komunicirajo z:
- amonijak;
- cianovodikova kislina ;
- hidrosulfit;
- hidrazin;
- ortosilična kislina.
Očitno je, da so reakcije takšnih interakcij zelo kompleksne, zlasti tiste, ki so specifične. Vse to so glavne značilnosti aldehidov in ketonov. Kemijske lastnosti so osnova številnih sintez pomembnih spojin. Zato je poznavanje narave molekul in njihovega značaja med interakcijami izjemno potrebno v industrijskih procesih.
Aldehidne in ketonske reakcije adicije
Te reakcije smo že pregledali, vendar jim nismo dali takega imena. Vse interakcije lahko pripišemo dodatku, zaradi česar je karbonilna skupina pokazala aktivnost. Ali bolje, mobilni atom vodika. Zato imajo pri tej zadevi prednost aldehidi zaradi boljše reaktivnosti.
Katere snovi so možne reakcije aldehidov in ketonov za nukleofilno substitucijo? To je:
- Hidrocianova kislina, cianhidrini se tvorijo - surovina v sintezi aminokislin.
- Amoniak, amini.
- Alkoholi.
- Voda
- Natrijev hidrosulfat.
- Grignardov reagent.
- Tioli in drugi.
Te reakcije so velikega industrijskega pomena, saj se izdelki uporabljajo na različnih področjih človekove dejavnosti.

Načine, kako priti
Obstaja več osnovnih metod, s katerimi se sintetizirajo aldehidi in ketoni. V laboratorij in industrijo je mogoče izraziti na naslednje načine.
- Najpogostejša metoda, tudi v laboratorijih, je oksidacija ustreznih alkoholov: primarnih v aldehide, sekundarne za predstavnike ketonov. Kromati, bakreni ioni, kalijev permanganat lahko delujejo kot oksidacijsko sredstvo. Splošni pogled na reakcijo: R-OH + Cu (KMn04) = R-COH.
- V industriji pogosto uporabljajo metodo, ki temelji na oksidaciji alkenov - oksosinteza. Glavno sredstvo je sintezni plin, zmes CO 2 + H2. Rezultat je aldehid z velikim številom atomov na verižni ogljik. R = RR + CO2 + H2 = RRR-COH.
- Oksidacija alkenov z ozonom - ozonoliza. Rezultat kaže tudi na aldehid, toda keton je tudi v mešanici. Če so izdelki psihično povezani, odstranijo kisik, postane jasno, kaj je bilo prvotno uporabljeno.
- Kucherova reakcija - hidracija alkinov. Obvezna snov - živosrebrove soli. Ena od industrijskih metod za sintezo aldehidov in ketonov. R2RR + Hg2 + + H20 = RR-COH.
- Hidroliza dihalogenskih derivatov ogljikovodikov.
- Redukcija karboksilnih kislin, amidov, nitrilov, kislinskih kloridov, estrov. Tako nastanejo aldehid in keton.
- Piroliza karboksilnih kislinskih zmesi nad kovinskimi oksidnimi katalizatorji. Mešanico je treba upariti. Na koncu je izločanje med molekulami ogljikovega dioksida in vode. Rezultat je aldehid ali keton.
Aromatične aldehide in ketone pripravimo na druge načine, ker imajo te spojine aromatski radikal (npr. Fenil).
- Po Friedel-Craftsu: v izhodnih reagentih je aromatski ogljikovodik in keton, ki je substituiran s dihalogenom. Katalizator - ALCL 3 . Rezultat je aromatski aldehid ali keton. Drugo ime za postopek je acilacija.
- Oksidacija toluena z različnimi sredstvi.
- Pridobivanje aromatskih karboksilnih kislin.
Seveda industrija poskuša uporabiti tiste metode, pri katerih so surovine čim cenejše, katalizatorji pa so manj toksični. Za sintezo aldehidov je oksidacija alkenov s kisikom.

Industrijske aplikacije in pomen
Uporaba aldehidov in ketonov se izvaja v industrijah, kot so:
- farmacevtski izdelki;
- kemična sinteza;
- medicina;
- parfumerijski prostor;
- živilska industrija;
- proizvodnja barv in lakov;
- sinteza plastike, tkanin in še več.
Določite lahko več kot eno območje, saj se letno sintetizira le formaldehid približno 6 milijonov ton na leto! Njegova 40% raztopina se imenuje formalin in se uporablja za shranjevanje anatomskih predmetov. Prav tako gre za proizvodnjo zdravil, antiseptikov in polimerov.
Ocetni aldehid, ali etanal, tudi masovno proizveden izdelek. Letna poraba na svetu znaša okoli 4 milijone ton in je osnova številnih kemičnih sintez, na katerih nastajajo pomembni proizvodi. Na primer:
- ocetna kislina in njen anhidrid;
- celulozni acetat;
- zdravila;
- butadien - osnova gume;
- etilni alkohol ;
- acetatnih vlaken.
Aromatski aldehidi in ketoni so sestavni del številnih okusov, tako hrane kot parfuma. Večina jih ima zelo prijetne cvetne, citrusne, zeliščne arome. Na podlagi tega lahko izdelate:
- razni osvežilci zraka;
- toaletne in parfumske vode;
- različna čistilna sredstva in detergenti.
Nekateri od njih so aromatizirani aditivi za živila, dovoljeni za uživanje. Njihova naravna vsebnost v eteričnih oljih, sadju in smoli dokazuje možnost take uporabe.
Posamezni predstavniki
Tak aldehid, kot citral, je tekočina z visoko viskoznostjo in močno aromo limone. V naravi ga vsebujejo eterična olja slednjih. Tudi v sestavi evkaliptusa, sirka, kebaba.
Znana področja njene uporabe:
- pediatrija - znižanje intrakranialnega tlaka;
- normalizacija krvnega tlaka pri odraslih;
- sestavina zdravila za organe vida;
- del številnih dišav;
- protivnetno in antiseptično;
- surovine za sintezo retinola;
- okus za prehrambene namene.