Voda in njene fizikalne in kemijske lastnosti. Struktura vode
Najpomembnejša snov našega planeta, edinstvena po svojih lastnostih in sestavi, je seveda voda. Konec koncev, zahvaljujoč ji, da je življenje na Zemlji, medtem ko ni na drugih objektih sončnega sistema, znanega danes. Trdna, tekoča, v obliki pare - je potrebna in pomembna za vse. Voda in njene lastnosti so predmet študija celotne znanstvene discipline - hidrologije.
Količina vode na planetu
Če upoštevamo kazalnik količine tega oksida v vseh agregativnih stanjih, potem je to približno 75% celotne mase na planetu. Pri tem je treba upoštevati vezano vodo v organske spojine živih bitij, mineralov in drugih elementov.

Če upoštevate le tekoče in trdno stanje vode, se bo stopnja znižala na 70,8%. Razmislite, kako so ti odstotki porazdeljeni, ki vsebujejo zadevno snov.
- Solna voda v oceanih in morjih, slanih jezer na Zemlji 360 milijonov km 2 .
- Sveža voda je porazdeljena neenakomerno: v ledenikih Grenlandije, Arktike in Antarktike je obdan z ledom v višini 16,3 milijona km 2 .
- V svežih rekah, močvirjih in jezerih je koncentriranih 5,3 milijona km 2 vodikovega oksida.
- Podzemna voda je 100 milijonov m 3 .
Zato astronavti iz oddaljenega vesolja vidijo Zemljo v obliki modre krogle z občasnimi lisami zemlje. Pomembni elementi znanosti so voda in njene lastnosti, poznavanje značilnosti strukture. Poleg tega človeštvo v zadnjem času začenja občutiti pomanjkanje sveže vode. Morda bo takšno znanje pomagalo pri reševanju tega problema.
Sestava vode in struktura molekule
Če upoštevamo te kazalnike, bodo lastnosti, ki jih ta neverjetna snov manifestira, takoj postale jasne. Tako je vodna molekula sestavljena iz dveh vodikovih atomov in enega kisikovega atoma, zato ima empirično formulo H 2 O. Poleg tega imajo elektroni obeh elementov pomembno vlogo pri konstrukciji same molekule. Poglejmo, kakšna je struktura vode in njenih lastnosti.
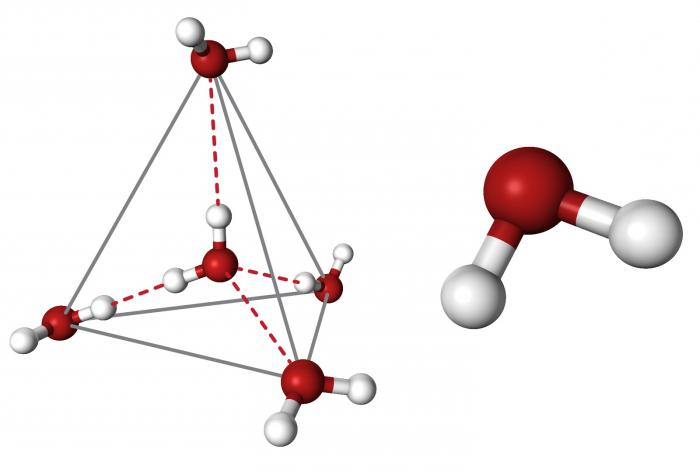
Očitno je, da je vsaka molekula usmerjena okoli druge in skupaj tvorijo skupno kristalno mrežo. Zanimivo je, da je oksid zgrajen v obliki tetraedra - atoma kisika v središču in dva para njenih elektronov in dva atoma vodika okoli sta asimetrično. Če narišete črto skozi središča jedra atomov atomov in jih povežete, potem dobite točno tetraedrično geometrijsko obliko.
Kot med središčem kisikovega atoma in jedri vodikov je 104,5 ° C. Vezava je O-H = 0,0957 nm. Prisotnost elektronskih parov kisika, pa tudi njegova večja elektronska afiniteta v primerjavi z vodikom, zagotavlja nastanek negativno nabitega polja v molekuli. V nasprotju z njo jedra vodikov tvorijo pozitivno nabit del spojine. Tako se izkaže, da je molekula vode dipol. To določa, kaj je voda, njene fizikalne lastnosti pa so odvisne tudi od strukture molekule. Za žive stvari te značilnosti igrajo pomembno vlogo.
Osnovne fizikalne lastnosti
Ti se običajno pripisujejo kristalni rešetki, vrelišču in tališču, posebnim individualnim značilnostim. Vse in razmislite.
- Struktura kristalne rešetke vodikovega oksida je odvisna od agregatnega stanja. Lahko je trdna - ledena, tekoča - glavna voda v normalnih pogojih, plinasta - para, ko se temperatura vode dvigne nad 100 ° C. Led oblikuje lepe vzorce kristalov. Žar je na splošno ohlapen, vendar je sklep zelo močan, gostota je nizka. To si lahko ogledate na primeru snežink ali zmrzali na steklu. V navadni vodi rešetka nima stalne oblike, se spreminja in prehaja iz ene države v drugo.
- Molekula vode v vesolju ima pravilno obliko krogle. Vendar pa se pod dejanjem gravitacije zemlje izkrivlja in v tekočem stanju ima obliko plovila.
- Dejstvo, da je struktura vodikovega oksida dipol, določa naslednje lastnosti: visoka toplotna prevodnost in toplotna zmogljivost, ki ju je mogoče zaslediti v hitrem segrevanju in dolgem ohlajanju snovi, sposobnost usmerjanja okoli sebe tako ionov kot posameznih elektronov, spojin. Zaradi tega je voda univerzalno topilo (polarno in nevtralno).
- Sestava vode in struktura molekule pojasnjujeta sposobnost te spojine, da tvori več vodikovih vezi, vključno z drugimi spojinami, ki imajo osamljene elektronske pare (amoniak, alkohol in druge).
- Vrelišče tekoče vode je 100 ° C, kristalizacija poteka pri + 4 ° C. Led je pod tem indikatorjem. Če povečate pritisk, potem vrelišče vode dramatično povečala. Pri visokih atmosferah se lahko v njem tali svinec, hkrati pa tudi ne vre (nad 300 ° C).
- Lastnosti vode so zelo pomembne za živa bitja. Na primer, ena najpomembnejših je površinska napetost. To je tvorba najtanjšega zaščitnega filma na površini vodikovega oksida. Gre za vodo v tekočem stanju. Zelo težko ga je mehansko razbiti. Znanstveniki so ugotovili, da je potrebna sila 100 ton. Kako jo opaziti? Film je viden, ko voda počasi kaplja iz pipe. Vidimo lahko, da je kot v nekakšni lupini, ki se razteza do določene meje in teže in izstopa v obliki okrogle kapljice, rahlo popačene zaradi gravitacije. Zaradi površinske napetosti se lahko na površini vode nahaja veliko predmetov. Na njih se lahko prosto gibljejo žuželke s posebnimi napravami.
- Voda in njene lastnosti so nenormalne in edinstvene. Z organoleptičnimi lastnostmi te spojine je brezbarvna tekočina brez okusa in vonja. To, kar imenujemo okus vode, so minerali, raztopljeni v njem, in druge sestavine.
- Prevodnost vodikovega oksida v tekočem stanju je odvisna od tega, koliko in kakšne soli so v njej raztopljene. Destilirana voda ne vsebujejo nečistoč električni tok ne drži.
Led je posebno stanje vode. V strukturi tega stanja so njene molekule med seboj povezane z vodikovimi vezmi in tvorijo lepo kristalno mrežo. Ampak to je precej nestabilen in lahko zlahka razpok, taline, da je, deformirati. Med molekulami se ohranja veliko praznin, katerih dimenzije presegajo velikost samih delcev. Zaradi tega je gostota ledu manjša od gostote tekočega vodikovega oksida.

To je zelo pomembno za reke, jezera in druga sladkovodna telesa. V zimskem obdobju voda v njih ne zmrzne popolnoma, temveč se pokrije le z gosto skorjo lažjega ledu, ki plava navzgor. Če ta lastnost ni bila značilna za trdno stanje vodikovega oksida, bi se rezervoarji zamrznili. Življenje pod vodo bi bilo nemogoče.
Poleg tega je trdno stanje vode zelo pomembno kot vir ogromne količine sveže pitne vode. To so ledeniki.
Posebno lastnost vode lahko imenujemo fenomen trojne točke. To je stanje, v katerem lahko hkrati obstajata led, para in tekočina. To zahteva pogoje, kot so:
- visok tlak - 610 Pa;
- temperatura 0,01 ° C.
Indeks transparentnosti vode je odvisen od nečistoč. Tekočina je lahko popolnoma prozorna, opalescentna, motna. Valovi rumene in rdeče barve se absorbirajo, vijolične žarke prodrejo globoko.

Kemijske lastnosti
Voda in njene lastnosti so pomembno orodje za razumevanje mnogih življenjskih procesov. Zato se zelo dobro preučujejo. Torej, hidrokemija se zanima za vodo in njene kemijske lastnosti. Med njimi so: t
- Trdnost To je lastnost, ki se pojasni s prisotnostjo kalcijevih in magnezijevih soli, njihovih ionov v raztopini. Razdeljen je na konstanto (soli imenovanih kovin: kloridi, sulfati, sulfiti, nitrati), začasne (bikarbonati), ki se izloči z vrenjem. V Rusiji je voda mehkejša pred uporabo s kemičnimi sredstvi za boljšo kakovost.
- Mineralizacija. Lastnost na osnovi dipolnega momenta vodikovega oksida. Zaradi svoje prisotnosti so molekule sposobne pritrditi na sebe številne druge snovi, ione in jih obdržati. Tako nastajajo družabniki, klatrati in druga združenja.
- Lastnosti redoksa. Kot univerzalno topilo, katalizator, asociant, voda lahko komunicira z mnogimi enostavnimi in kompleksnimi spojinami. Pri nekaterih deluje kot oksidant, pri drugih - obratno. Kako reagent reagira s halogeni, solmi, nekaterimi manj aktivnimi kovinami, z mnogimi organske snovi. Najnovejše transformacije preučujejo organsko kemijo. Voda in njene lastnosti, zlasti kemične, kažejo, da je vsestranska in edinstvena. Kot oksidant reagira z aktivnimi kovinami, nekaterimi binarnimi solmi, številnimi organskimi spojinami, ogljikom, metanom. Na splošno kemijske reakcije, ki vključujejo to snov, zahtevajo izbiro določenih pogojev. Od njih bo odvisen izid reakcije.
- Biokemijske lastnosti. Voda je sestavni del vseh biokemičnih procesov v telesu, saj je topilo, katalizator in medij.
- Interakcija s plini z nastankom klatratov. Redna tekoča voda lahko absorbira celo neaktivne kemične pline in jih razporedi v votline med molekulami notranje strukture. Takšne spojine se imenujejo klatrati.
- Pri mnogih kovinah vodikov oksid tvori kristalinične hidrate, v katerih je nespremenjen. Na primer, bakrov sulfat (CuSO4 * 5H2O), kot tudi navadni hidrati (NaOH * H20 in drugi).
- Za vodo so značilne reakcije spojine, v katerih nastajajo nove vrste snovi (kisline, baze, baze). Niso redoks.
- Elektroliza. Pod vplivom električnega toka se molekula razgradi v sestavljene pline - vodik in kisik. Eden od načinov, kako jih pridobiti v laboratoriju in industriji.
Z vidika Lewisove teorije je voda šibka kislina in šibka baza hkrati (amfolit). To pomeni, lahko rečemo o nekakšni amfoterni v kemijskih lastnostih.

Voda in njene koristne lastnosti za živa bitja
Težko je preceniti pomen, ki ga ima vodikov oksid za vsa živa bitja. Navsezadnje je voda zelo vir življenja. Znano je, da brez nje oseba ne bi mogla preživeti teden dni. Voda, njene lastnosti in vrednost so preprosto ogromne.
- Je univerzalna, ki je sposobna raztapljati tako organske kot anorganske spojine, topilo, ki deluje v živih sistemih. Zato je voda vir in medij za pretok vseh katalitičnih biokemičnih transformacij, z oblikovanjem kompleksnih vitalnih kompleksnih spojin.
- Sposobnost tvorbe vodikovih vezi je ta snov univerzalna pri ohranjanju temperatur brez spreminjanja agregatnega stanja. Če se to ne bi zgodilo, bi se pri najmanjšem zmanjšanju stopinj spremenilo v led v živih bitijih, kar bi povzročilo celično smrt.
- Za ljudi je voda vir vseh osnovnih gospodinjskih izdelkov in potreb: kuhanje, pranje, čiščenje, kopanje, kopanje in plavanje itd.
- Industrijski obrati (kemična, tekstilna, strojna, prehrambena, rafinerija nafte in drugi) ne bi mogli opravljati svojega dela brez sodelovanja vodikovega oksida.
- Od antičnih časov je veljalo, da je voda vir zdravja. Uporabljen je bil in se danes uporablja kot terapevtska snov.
- Rastline ga uporabljajo kot glavni vir prehrane, zaradi česar proizvajajo kisik - plin, ki na našem planetu ustvarja življenje.
Razlogi, zakaj je voda najbolj razširjena, pomembna in nujna snov za vse žive in umetno ustvarjene predmete, je več deset. Prinesli smo samo najbolj očitne, glavne.

Hidrološki krog vode
Z drugimi besedami, gre za njegovo kroženje v naravi. Zelo pomemben proces, ki vam omogoča nenehno obnavljanje izginjajočih zalog vode. Kako gre?
Glavni udeleženci so trije: podtalnica (ali podzemna voda), površinska voda in oceani. Pomembno je tudi kondenziranje ozračja in izjemne padavine. Aktivni udeleženci v procesu so tudi rastline (predvsem drevesa), ki lahko dnevno absorbirajo veliko količino vode.
Torej je postopek naslednji. Podzemna voda zapolnjuje podzemne kapilare in jate na površje in svetovni ocean. Nato rastline absorbirajo površinske vode in jih prepeljejo v okolje. Izhlapevanje se pojavi tudi iz velikih območij oceanov, morij, rek, jezer in drugih vodnih teles. Kaj v vodi naredi voda? Kondenzirala in prelila nazaj kot padavine (dež, sneg, toča).
Če se ti procesi ne bi zgodili, bi se zaloge vode, zlasti sveže vode, dolgo iztekle. Zato ljudje veliko pozornosti namenjajo zaščiti in normalnemu hidrološkemu ciklu.
Koncept težke vode
V naravi obstaja vodikov oksid kot mešanica izotopologa. To je posledica dejstva, da vodik tvori tri vrste izotopov: protium 1 N, devterij 2 N, tritij 3 N. Kisik prav tako ne zaostaja in tvori tri stabilne oblike: 16 O, 17 O, 18 O. to ni samo običajna propijska voda, ki ima sestavo H 2 O ( 1 H in 16 O), temveč tudi devterij in tritij.

Obenem je devterij ( 2 N) stabilen v strukturi in obliki, ki je vključen v skoraj vse naravne vode, vendar v majhnih količinah. Da se imenuje težka. Nekoliko se razlikuje od običajnega ali preprostega za vse kazalnike.
Za težko vodo in njene lastnosti je značilno več točk.
- Kristalizira pri temperaturi 3,82 ° C.
- Vrelišče opazimo pri 101,42 ° C.
- Gostota je 1,1059 g / cm3.
- Kot topilo nekajkrat slabše od lahke vode.
- Ima kemijsko formulo D 2 O.
Pri izvajanju poskusov, ki kažejo učinek takšne vode na žive sisteme, je bilo ugotovljeno, da lahko v njem živijo le določene vrste bakterij. Kolonijam je bilo potrebno nekaj časa za prilagoditev in prilagoditev. Toda po prilagoditvi so popolnoma obnovili vse vitalne funkcije (reprodukcijo, prehrano). Poleg tega je jeklo zelo odporno na sevanje. Poskusi na žabah in ribah niso dali pozitivnega rezultata.
Sodobna področja uporabe devterija in težka voda, ki jo tvorijo, so atomska in jedrska energetika. V laboratorijskih pogojih se taka voda lahko dobi z navadno elektrolizo - nastane kot stranski produkt. Deuterij se oblikuje s ponovljenimi destilacijami vodika v posebnih napravah. Njegova uporaba temelji na sposobnosti upočasnjevanja nevtronskih sintez in protonskih reakcij. Prav izredno težke vode in vodikove izotope tvorijo jedrska in vodikova bomba.
Poskusi uporabe deuterijeve vode v majhnih količinah so pokazali, da se ne zadržujejo dolgo - popolni zaključek je opazen po dveh tednih. Uporabite ga kot vir vlage za življenje je nemogoče, vendar tehnična vrednost je preprosto ogromna.
Talino vodo in njeno uporabo
Lastnosti takšne vode so ljudje že od antičnih časov opredelili kot zdravilne. Že dolgo je opaziti, da ko se sneg stopi, živali poskušajo piti vodo iz nastalih luž. Kasneje sta bila temeljito raziskana njegova struktura in biološki učinki na človeško telo.

Melt water, njeni znaki in lastnosti so v sredini med normalno svetlobo in ledu. Znotraj se ne oblikujejo samo z molekulami, temveč s skupino grozdov, ki jih tvorijo kristali in plin. To pomeni, da sta vodik in kisik znotraj praznin med strukturnimi deli kristala. Na splošno je struktura taline vode podobna strukturi ledu - struktura je ohranjena. Fizikalne lastnosti takega vodikovega oksida se rahlo razlikujejo v primerjavi z običajnimi. Biološki učinki na telo pa so odlični.
Ko je voda zamrznjena s prvo frakcijo, se težji del spremeni v led - to so izotopi, soli in nečistoče devterija. Zato je treba to jedro odstraniti. Ostalo pa je čista, strukturirana in zdrava voda. Kakšen je učinek na telo? Znanstveniki Donetsk Research Institute so imenovali naslednje vrste izboljšav:
- Pospeševanje obnovitvenih procesov.
- Krepitev imunitete.
- Pri otrocih se po vdihavanju s takšno vodo pojavi okrevanje in zdravljenje prehladov, kašelj, rinitis in tako naprej.
- Izboljšano dihanje, laringealne in sluznice.
- Splošna blaginja osebe, aktivnost se povečuje.
Danes obstajajo številni podporniki zdravljenja s talino vode, ki pišejo svoje pozitivne ocene. Vendar pa obstajajo znanstveniki, vključno z zdravniki, ki teh stališč ne podpirajo. Verjamejo, da taka voda ne bo škodila, vendar je malo koristi.
Energetika
Zakaj se lahko lastnosti vode spreminjajo in obnavljajo, ko se selijo v drugačno agregatno stanje? Odgovor na to vprašanje je naslednji: ta povezava ima svoj lasten pomnilnik informacij, ki beleži vse spremembe in vodi v obnovo strukture in lastnosti ob pravem času. Bioenergetsko polje, skozi katerega prehaja del vode (ki prihaja iz vesolja), nosi močan naboj energije. Ta vzorec se pogosto uporablja pri zdravljenju. Vendar pa z medicinskega vidika ne more vsaka voda imeti koristen učinek, vključno z informacijami.
Strukturirana voda - kaj je to?
To je taka voda, ki ima nekoliko drugačno strukturo molekul, lokacijo kristalnih mrež (kot je opaziti v ledu), vendar je še vedno tekoča (odmrzovanje se nanaša tudi na ta tip). V tem primeru sestava vode in njene lastnosti niso znanstveno drugačne od tistih, ki so značilne za navadni vodikov oksid. Zato strukturirana voda ne more imeti tako širokega terapevtskega učinka, ki se pripisuje njenim ezoteričnim in zagovornikom alternativne medicine.