Sekundarna struktura proteina in njegova prostorska organizacija. Oblikovanje sekundarne strukture proteina.
V telesu je vloga beljakovin zelo velika. Hkrati se lahko takšno ime nosi samo, ko pridobi vnaprej določeno strukturo. Do te točke je to polipeptid, samo aminokislinska veriga, ki ne more izvajati svojih lastnih funkcij. Na splošno je prostorska struktura proteinov (primarna, sekundarna, terciarna in domena) njihova tridimenzionalna struktura. In najpomembnejše za telo sekundarne, terciarne in domenske strukture.
Pogoji za proučevanje strukture proteinov
Med metodami proučevanja strukture kemikalij ima posebno vlogo rentgenska kristalografija. Z njim lahko dobimo informacije o zaporedju atomov v molekularnih spojinah in njihovi prostorski organizaciji. Preprosto povedano, rentgensko sliko lahko naredimo za posamezno molekulo, ki je postala mogoča v tridesetih letih 20. stoletja.
Ad
Takrat so raziskovalci ugotovili, da številni proteini nimajo le linearne strukture, temveč jih je mogoče razvrstiti tudi v spirale, zapletke in domene. Kot rezultat izvajanja množice znanstvenih poskusov se je izkazalo, da je sekundarna struktura proteina končna oblika za strukturne beljakovine in intermediat za encime in imunoglobuline. To pomeni, da morajo snovi, ki imajo na koncu terciarno ali kvartarno strukturo, v fazi njihovega "zorenja", prestati tudi fazo spiralne tvorbe, ki je značilna za sekundarno strukturo.
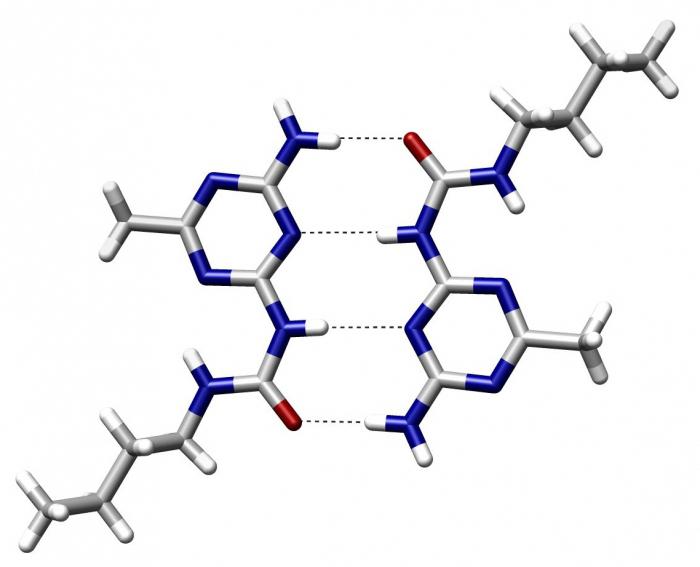
Nastanek sekundarne proteinske strukture
Takoj, ko je sinteza polipeptida na ribosomih končana v grobi mreži celične endoplazme, sekundarna struktura beljakovin. Sam polipeptid je dolga molekula, ki zavzema veliko prostora in je neprimerna za transport in izvajanje inherentnih funkcij. Da bi zmanjšali njegovo velikost in ji dali posebne lastnosti, se razvije sekundarna struktura. To se zgodi z nastankom alfa-spirale in beta-plasti. Na ta način dobimo protein sekundarne strukture, ki se bo v prihodnosti spremenil v terciarno ali kvartarno ali pa bo uporabljen v tej obliki.
Ad
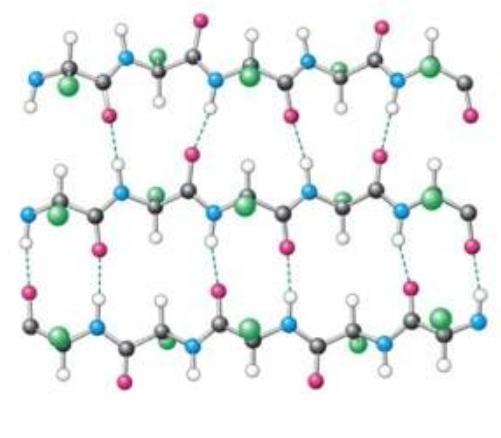
Sekundarna organizacija
Kot so pokazale številne študije, je sekundarna struktura beljakovine bodisi alfa heliks, bodisi beta sloj, ali izmenjava odsekov s temi elementi. Poleg tega je sekundarna struktura način zavijanja in spiralne tvorbe proteinske molekule. To je kaotičen proces, ki nastane zaradi vodikovih vezi, ki se pojavijo med polarnimi regijami aminokislinskih ostankov v polipeptidu.
Alfa spiralna sekundarna struktura
Ker v biosintezo polipeptidov sodelujejo samo L-aminokisline, se nastanek sekundarne strukture proteina začne z zasukanjem v smeri urinega kazalca (desni zavoj). Za vsak spiralni zavoj so strogo 3,6 aminokislinskih ostankov, razdalja vzdolž spiralne osi pa je 0,54 nm. To so skupne lastnosti za sekundarno strukturo proteina, ki ni odvisna od vrste aminokislin, ki sodelujejo pri sintezi.
Ugotovili smo, da ni celotna polipeptidna veriga popolnoma spiralizirana. Njegova struktura vsebuje linearne odseke. Še posebej se molekula pepsin proteina spiralizira le za 30%, lizozim za 42% in hemoglobin za 75%. To pomeni, da sekundarna struktura proteina ni strogo spiralna, temveč kombinacija njenih odsekov z linearnimi ali večplastnimi.
Ad
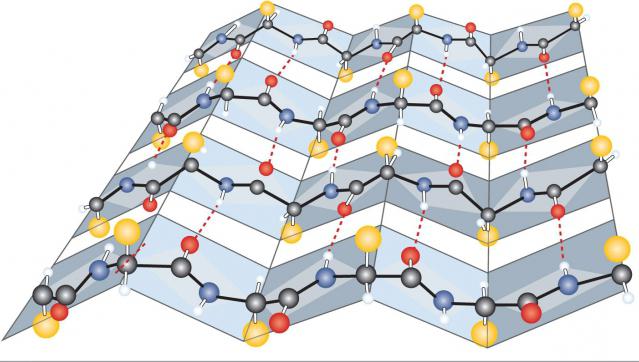
Sekundarna struktura beta sloja
Druga vrsta strukturne organizacije snovi je beta sloj, ki je sestavljen iz dveh ali več pramenov polipeptida, ki je povezan z vodikovo vezjo. Slednje se pojavlja med prostimi CO NH2 skupinami. Strukturni (mišični) proteini so tako združeni.
Struktura proteinov te vrste je naslednja: en pramen polipeptida z oznako končnih odsekov A-B je vzporeden z drugim. Edina omejitev je, da se druga molekula nahaja antiparalelno in je označena kot BA. Tako nastane beta-plast, ki lahko sestoji iz poljubnega števila polipeptidnih verig, povezanih z mnogimi vodikovimi vezmi.
Vodikova vez
Sekundarna struktura proteina je vez, ki temelji na večpolnih interakcijah atomov z različnimi faktorji elektronegativnosti. 4 elementi imajo največjo sposobnost tvoriti takšno vez: fluor, kisik, dušik in vodik. V beljakovinah je vse, razen fluorida. Zato se lahko tvori in oblikuje vodikova povezava, ki omogoča povezavo polipeptidnih verig v beta slojih in alfa vijačnici.
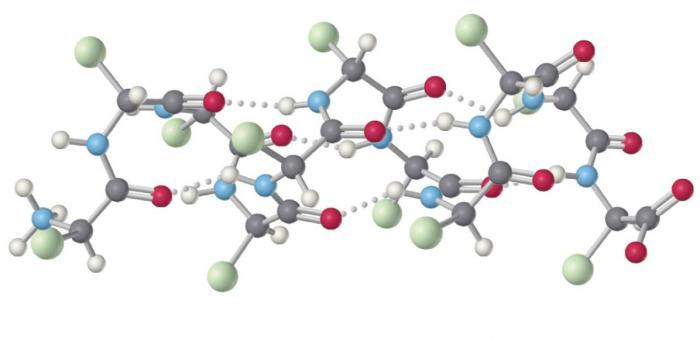
Najlažji način za pojasnitev nastanka vodikove vezi je primer vode, ki je dipol. Kisik nosi močan negativen naboj in zaradi visoke polarizacije O-H vezi velja vodik za pozitivno. V tem stanju so molekule prisotne v nekem okolju. In mnogi med njimi se dotaknejo in trčijo. Nato kisik iz prve molekule vode privlači vodik iz drugega. In tako na verigi.
Ad
Podobni procesi se pojavljajo v beljakovinah: elektronegativna peptidna vez kisika privlači vodik iz katerega koli dela drugega aminokislinskega ostanka in tako tvori vodikovo vez. To je šibka polarna konjugacija, za prelom je potrebno porabiti približno 6,3 kJ energije.
Za primerjavo, najšibkejši kovalentna vez beljakovin potrebuje 84 kJ energije, da ga razbije. Najmočnejša kovalentna vez zahteva 8400 kJ. Vendar je količina vodikovih vezi v beljakovinski molekuli tako velika, da njihova celotna energija omogoča molekuli, da obstaja v agresivnih pogojih in ohrani njeno prostorsko strukturo. Zaradi tega obstajajo beljakovine. Struktura proteinov te vrste zagotavlja moč, ki je potrebna za delovanje mišic, kosti in vezi. Torej je velik pomen sekundarne strukture beljakovin za telo.