Drugi zakon termodinamike. Razlaga, teoretična in praktična utemeljitev
V fiziki, ker je to natančna znanost, se večina dogm dokazuje empirično. Tako je nastal drugi zakon termodinamike, ki se trenutno preučuje v vsaki šoli. Nepovratni toplotni procesi - tako pravi. Treba je omeniti, da je v začetnih fazah študije takšna razlaga veliko bolj razumljiva.
Splošni pogledi
Fizično načelo, ki omejuje smer različnih procesov v. T termodinamični sistemi je drugi zakon termodinamike. Opredelitev tega izraza je nastala v 19. stoletju, najprej Rudolf Clausis, nato pa William Thomson (Lord Kelvin). V skladu z dvema postulatoma v svetu ne more obstajati nekakšen perpetualni stroj druge vrste. Ni in ne bo takšne naprave, ki bi toploto, ki prihaja iz vseh stvari, živih bitij in pojavov, v energijo za svoje stalno delo. Na podlagi tega je bilo izvedeno pravilo, da učinkovitost ne more biti enaka eni. To lahko primerjamo z delovanjem hladilnika, kjer bo temperatura, recimo, enaka absolutna nič. V takih pogojih je krožna izmenjava toplote izključena. 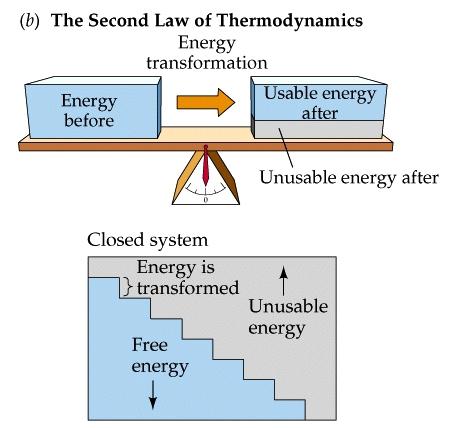
Formulacija Rudolph Clausis
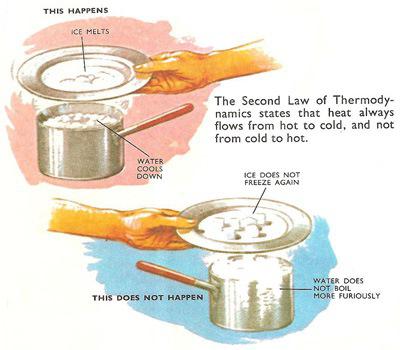
Prvi je izrazil drugo pravo termodinamike R. Clausis - nemški fizik in matematik. Po njegovem mnenju krožni proces, v katerem se rezultat doseže s prenosom toplote iz manj ogrevanega telesa na bolj ogreto, ni mogoč. Z drugimi besedami, temperatura v celoti ali deloma lahko prosto prehaja iz toplejšega telesa v hladnejšo, vendar se ta proces ne more zgoditi v nasprotni smeri. To nam jasno kaže odsotnost cikličnosti, začaran krog. Takšni koncepti so za termodinamiko nesprejemljivi. Toplota se preprosto zamenja med telesi in kot rezultat teh ukrepov se ne proizvaja presežna energija. 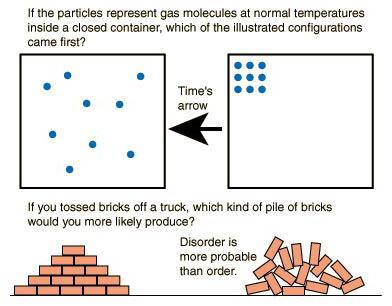
Postulat, ki ga je izpeljal Lord Kelvin
Podobna definicija drugega zakona termodinamike je prejela v spisih Thomsona - britanskega fizika in mehanike. Teoretično se sliši takole: "Cikličen proces, ki je edini rezultat, ki ga lahko dosežemo s hlajenjem toplega telesa ali rezervoarja, je nemogoč." Da bi razumeli to razlago bolj jasno, si predstavimo nek stroj (ne more obstajati po termodinamskem postulatu). Občasno ohlaja rezervoar s stalno vročo vodo in od te toplotne energije. Zaradi te energije stroj dvigne različne tovore, kot je gradbeni žerjav. V tem primeru ni motorja, elektrarn in drugih mehanskih polnil. V smislu empirične fizike je to nemogoče. 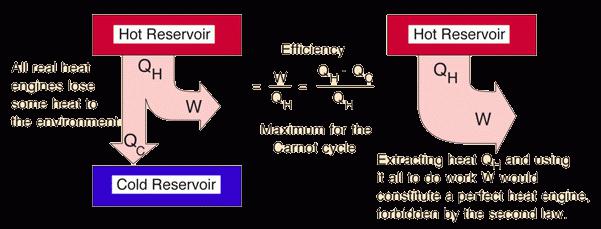
Kaj je običajno?
Zdaj bomo preučili, kako sta ti dve interpretaciji združeni in na kateri načeloma temelji drugi zakon termodinamike. Entropija je merilo kaosa, ki se povečuje v procesu izmenjave toplote. Da je povezovalni element za opis Clausisa in Kelvina. Toda nazaj. Drugi zakon termodinamike pravi, da ko se toplota izmenjuje, energija upada (zato pridobivanje dela sploh ni mogoče), hkrati pa se poveča tudi merilo kaosa. Ta proces je nepovraten in se pogosto imenuje spontan. V termodinamiki se entropija nenehno množi, vendar je njeno uničenje nemogoče. Zato tudi 100 odstotkov energije, ki je v katerem koli telesu, ni mogoče pretvoriti v delo. 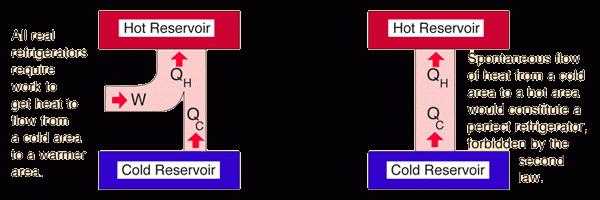
Kaj je merilo kaosa?
Koncept entropije je bil najprej oblikovan v ustih Clausisa. Uporabljen je bil za določitev merila nepovratnega procesa disipacije energije. To je bila nekakšna razlika v odstopanju realnega procesa od ideala. Entropija v zaprtih sistemih, kjer se vsi procesi odvijajo ciklično, ima konstantno vrednost. Če je proces nepovraten (kar neposredno zadeva termodinamiko), ima entropija vedno pozitiven pomen. Prav tako je treba omeniti, da je merilo kaosa ustvarjeno z vsemi procesi, ki se pojavljajo v vesolju. S stalnimi kazalci prostornine in energije telesa ali rezervoarja se entropija stalno povečuje. Če se te številke redno spreminjajo, se lahko merilo kaosa zmanjša zaradi opravljenega dela, vendar je njegovo popolno uničenje nemogoče. Treba je omeniti, da se entropija vesolja ne zmanjšuje. Ostaja normalna ali trajno narašča.
Ilustrativni primer
Drugi zakon termodinamike je mogoče razložiti s standardnim primerom, ki se pogosto daje učencem. Imamo dve telesi z različnimi temperaturami. Bolj segreta snov bo oddajala svojo toploto manj ogrevano, dokler se njihove temperature ne izenačijo. Med tem postopkom se bo entropija prvega toplejšega telesa zmanjšala za manjšo sliko, kot se bo povečala pri drugem, hladnejšem telesu. Posledica takega spontanega procesa bo entropija sistema, katerega indeks bo višji od skupne vrednosti entropije dveh teles v začetnem položaju. Z drugimi besedami, kaos merilo sistema dveh snovi, ki izhaja iz izmenjave toplote, se je povečalo. 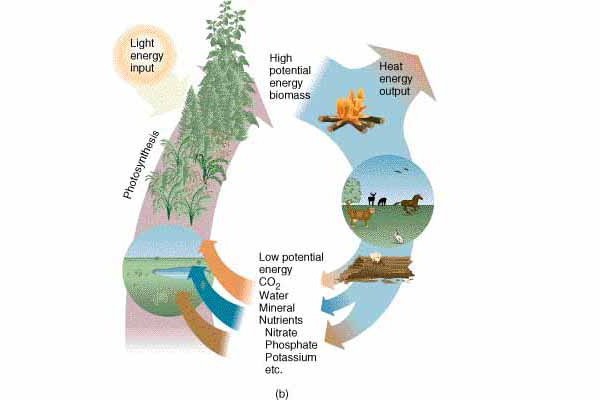
Termalna smrt vesolja
Clausis je pri opravljanju svojih raziskav ugotovil, da ne glede na to, kako odprt nam je prostor (naš planet, ločena območja, vodna območja itd.), Je vse to v vesolju. Vesolje je največji zaprt prostor, znotraj katerega potekajo makroskopski procesi. Ker je v zaprtem sistemu entropija nenehno povečevala svoj indeks, se naš svet približuje dejstvu, da bo kmalu v njem merilo kaosa doseglo neskončno vrednost. To pomeni, da se vsi procesi preprosto ustavijo zaradi dejstva, da je energija izčrpana. Takšna kritična točka, ki jo bomo v določeni prihodnosti dosegli, je dobila ime termalne smrti. Izkazalo se je, da so vsa naša dejanja (gibanje, hoja, tek), vsi pojavi, ki se pojavljajo na planetu (udarec vetra, cunami, gibanje litosferskih plošč) - vse to povzroči nepovratno povečanje entropije in izčrpa energijo.
Zavrnitev teorije
Človek še vedno ne more soditi o celotnem kozmosu. Vidimo le del sveta, v katerem živimo, in raziskujemo ta kotiček, dokazujemo določene zakone in na podlagi tega oblikujemo lastne ideje. Zato je prvo izpodbijanje možnosti termične smrti, ki temelji na drugem zakonu termodinamike, to, da vesolje morda ni zaprt sistem. Znano je, da je 85 odstotkov kozmosa sestavljeno iz antimaterije, katere lastnosti niso nikomur neznane. Drugo izpodbijanje je, da je naš kozmos, tudi če je zaprt, stalno nihanje. Zaradi različnih nihanj in sprememb v velikosti, masi, energiji in temperaturi se entropija ne poveča (v skupni univerzalni vrednosti) in se ne zmanjša. Zato smo že v stanju termodinamičnega ravnovesja ali po besedah Clausisa v stanju toplotne smrti.
Povzamemo
Drugi zakon termodinamike je neločljivo povezan z razvojem točnih znanosti. Odprla se je na začetku znanstvenega in tehnološkega napredka in postala, lahko rečemo, izhodišče za nadaljnje delo znanstvenikov s področja matematike, fizike in astronomije. Opozoriti je treba, da vse to predstavljamo predvsem v kopenskih razmerah. Verjetno je, da bo v drugačnem okolju, kjer imajo gravitacijska polja drugačno silo, termodinamika delovala po popolnoma drugačni shemi.