Redox. Redoks reakcije: opis, primeri
Redoks reakcije - redoks - predstavljajo nasprotno vzporedno interakcijo. Pri teh pojavih se spreminjajo nekatere značilnosti sestavnih delov. Te interakcije so realizirane z metodo elektronske redistribucije. Ta postopek poteka med oksidirajočimi atomi in reducenti. 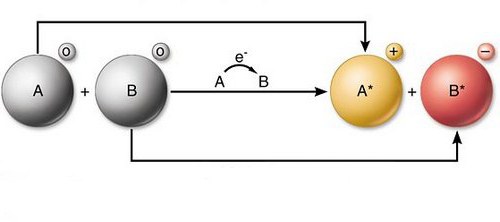
Lastnosti komponente
Organska kemija vključuje uporabo številnih oksidacijskih sredstev in reducentov. To vam omogoča, da izberete poseben reagent, ki ima selektivnost. To pomeni, da lahko komponenta selektivno vpliva na nekatere funkcionalne kategorije. Poleg tega je zaradi te širine izbire mogoče dobiti izdelke v določeni stopnji oksidacije. Tako, na primer, borogid Na ne more vplivati na estre in amide. Hkrati pa reducira aldehide ali ketone v alkohole. Med drugo skupino sestavin so tudi zelo selektivne spojine. Na primer, kompleks CrO3 in piridin. Ta struktura oksidira alkohole z visokim donosom na ketone. V zvezi s tem ne vpliva na komunikacijo CC. SeO 2 je tudi zelo selektiven. Spojina oksidira aldehidi in ketoni alfa dikarbonilnih spojin.
Splošne informacije
Redoks reakcije kažejo na drugačno spremembo lastnosti vhodnih komponent. To je odvisno od narave interakcije. Tako se med redukcijo zmanjša, in med oksidacijo se poveča. oksidacijsko stanje predmetov. Sprva je bil izraz tolmačen tako, da ga je bilo mogoče razumeti. Oksidacija se je štela za dodatek kisika, obnova - odstranitev. Po uvedbi elektronskih konceptov v znanost je bila definicija nekoliko razširjena. Od takrat se koncept razširi na interakcije, pri katerih kisik ni vključen. 
Lastnosti procesa
Redoks reakcije formalno predstavljajo gibanje elektronov. Komponente atoma enega reagenta se prenesejo v atom drugega. Torej je oksidacija, preprosto povedano, odpor elektronov. V nekaterih primerih lahko proces v molekuli izvirne snovi postane nestabilen. Posledično se lahko razcepi na manjše dele, vendar z visoko stopnjo stabilnosti. Atomi oksidirajočih snovi se običajno imenujejo darovalci elektronov, strukturni elementi oksidacijskega sredstva so sprejemljivi. Nadaljuje se nasprotni proces vezave elektronov. Imenuje se restavracija. V tovrstni interakciji se lahko pojavijo različni elementi. Na primer ogljik, vodik in drugo. Različne spojine je mogoče obnoviti. Na primer organske kisline v alkoholih in aldehidih. 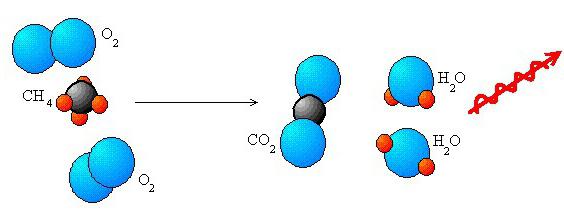
Vrste redoks reakcij
V skladu s formalnimi značilnostmi obravnavanih interakcij se delijo na intra- in intermolekularne. Slednje, na primer, vključujejo 2SO2 + O2 → SO3. Redoks reakcije so prav tako razvrščene kot nesorazmerne in nesorazmerne. V prvem primeru ima isti element različne lastnosti. Tako lahko komponenta istočasno postane tako redukcijsko sredstvo kot oksidacijsko sredstvo:
Cl2 + H20 → HClO + HCl.
Druga vrsta - reprocentacija ali sorazmernost - predstavlja več drugih interakcij. Pri takih reakcijah en element izhaja iz dveh različnih oksidacijskih stanj za en element:
NH4NO3 → N2O + 2H2O
Katalitični postopki
Znotraj teh interakcij zagotavlja visoko sposobnost selektivnosti. Tako lahko npr. V skladu s katalizatorjem in pogoji acetilenske ogljikovodike selektivno podvržemo hidrogeniranju do nasičenega ali etilena. In redukcija CO 2 v CO elektrokemičnega tipa v vodnem mediju v prisotnosti 1,4,8,11-tetraazaciklotetradekana iz nikljevega kompleksa omogoča izvedbo procesa pri nižjih potencialih in hkrati zatiranje. elektroliza vode med tvorbo H2. Ta interakcija ima ključno vrednost pri pretvorbi skozi CO CO 2 v različne organske snovi.
Pomen
Redox katalitične reakcije narava opravlja pomembne naloge v industriji. So precej razširjene narave in se uporabljajo v inženirstvu. Tudi osnova življenja so redoks reakcije, ki se pojavijo med transportom elektronov, dihalno aktivnostjo, fotosintezo. Te interakcije zagotavljajo večino porabe energije ljudi s sežiganjem različnih fosilnih goriv. 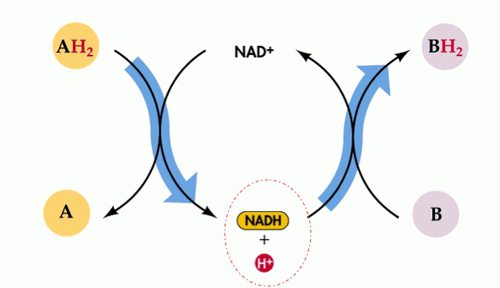
Tok interakcije
Redoks reakcije pogosto spremlja povečano sproščanje energije. To jim omogoča uporabo, na primer pri sprejemanju električne energije. Najbolj nasilne interakcije potekajo v odsotnosti topila. Če so prisotni, se takšne reakcije morda ne pojavijo. To je lahko posledica dejstva, da ena ali obe komponenti reagirata s topilom. Lahko navedemo naslednji primer. V vodni raztopini je reakcija 2Na + F 2 → 2NaF nemogoča. To je posledica dejstva, da se fluor in natrij odlikujeta po močni interakciji s H 2 O. Na nastanek kompleksa močno vplivajo lastnosti ionov v redoks reakcijah. Tako se na primer zgodi z [C0 2 + (CN) 6 ] 4 -. Ta kompleks velja za močno redukcijsko sredstvo, v nasprotju s hidratnim ionom CO 2 +.
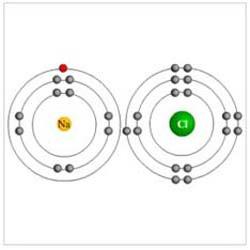
Organska kemija. Redoks reakcije
Na tem disciplinskem področju velja uporaba splošnih konceptov in konceptov o poteku in naravi procesa neproduktivna. To še posebej velja v primeru majhne polarnosti medatomske vezi. V organski kemiji je običajno, da se oksidacija obravnava kot proces povečevanja množine kislinskih ali poveča števila veziv, ki vsebujejo vodik. V nekaterih primerih se uporablja pristop, ki predpostavlja, da so atomi C pripisani različni stopnji oksidacije.

To pa je odvisno od števila vezav, sestavljenih s komponento, ki ima večjo elektronegativnost kot vodik. V tem primeru bo lokacija funkcionalnih derivatov izvedena v vrstnem redu naraščajočih oksidacijskih stanj. Tako je treba na primer nasičene ogljikovodike pripisati ničelni skupini (Art. Oxid. - 4), ROH, RNH 2 , RCl - prvemu (-2), R2CCl2 in R 2 CO - drugemu (0), RCCl. 3 in RCONH 2 - na 3. (+2), CO 2 in CCl 4 - na 4. (+4). V tem primeru je jasno, da je oksidacija proces, pri katerem se spojine prenesejo na višjo raven, zmanjšanje pa je obraten postopek. Pri proučevanju interakcij je treba posebno pozornost nameniti mehanizmom, s katerimi se procesi odvijajo. Opozoriti je treba, da so ti dejavniki zelo raznoliki. Tako lahko reakcije potekajo preko homolitskega ali heteroliznega mehanizma. V mnogih primerih pa je postopek prenosa z enim elektronom v začetni fazi interakcije. Postopek oksidacije je praviloma označen s pretokom v položajih z največjo gostoto in zmanjšanjem v položajih, kjer je elektronska gostota minimalna.