Tip atomske hibridizacije
Pri določanju geometrijske oblike kemičnega deleža je pomembno upoštevati, da so pari valentnih elektronov glavnega atoma, vključno s tistimi, ki ne tvorijo kemične vezi, v prostoru daleč drug od drugega.
Značilnosti izraza
Glede na vprašanje glede kovalentnega kemično vezavo pogosto uporabljamo pojem kot hibridizacijo atomskih orbital. Ta izraz je povezan s poravnavo oblike in energije. Hibridizacija atomskih orbital je povezana s procesom kvantne kemijske prestrukturiranja. Orbitale v primerjavi z izvirnimi atomi imajo drugačno strukturo. Bistvo hibridizacije je v tem, da elektron, ki se nahaja poleg jedra vezanega atoma, ne določa določena atomska orbital, temveč njihova kombinacija z enako glavno kvantno številko. V bistvu se ta proces nanaša na višje atomske energetske orbitale z elektroni.
Ad
Posebnosti procesa
Vrste hibridizacije atomov v molekulah so odvisne od tega, kako poteka orientacija novih orbital. Glede na vrsto hibridizacije je mogoče določiti geometrijo iona ali molekule, da bi prevzeli značilnosti kemijskih lastnosti.
Vrste hibridizacije
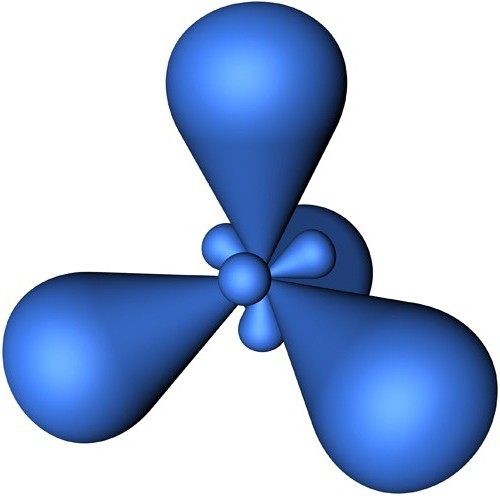
Ta vrsta hibridizacije, kot sp, je linearna struktura, kot med vezmi je 180 stopinj. Primer molekule s podobno možnostjo hibridizacije je BeCl2.
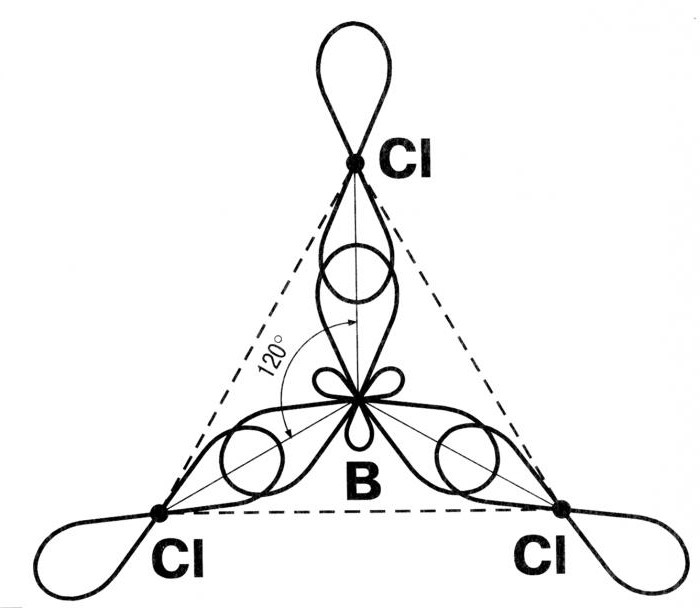
Naslednji tip hibridizacije je sp 2 . Za molekule je značilna trikotna oblika, kot med vezmi je 120 stopinj. Tipičen primer take različice hibridizacije je BC13.
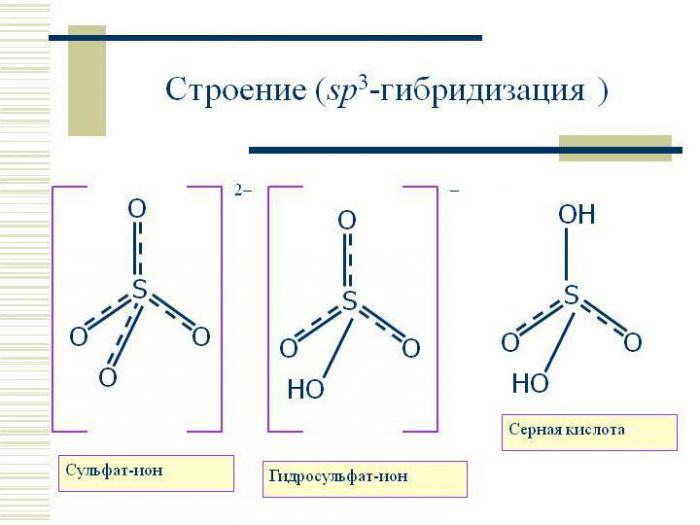
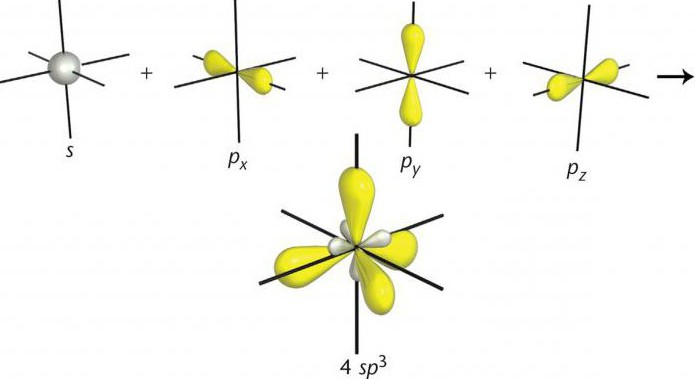
Vrsta sp3 hibridizacije kaže na tetraedrično strukturo molekule, tipičen primer snovi s to možnostjo hibridizacije je metanska molekula CH 4 . Valenčni kot je v tem primeru 109 stopinj 28 minut.
Ad
Ne samo par elektronov, temveč tudi neločeni pari elektronov so neposredno vključeni v hibridizacijo.
Hibridizacija v vodni molekuli
Na primer, v vodni molekuli med atomom kisika in atomom vodika obstajata dve kovalentne polarne vezi. Poleg tega ima sam atom kisika dva para zunanjih elektronov, ki ne sodelujeta pri ustvarjanju kemične vezi. Ti 4 parovi elektronov v prostoru zavzemajo posebno mesto okoli atoma kisika. Ker imajo vsi enako naboj, se v prostoru odbijajo, elektronski oblaki so med seboj precej oddaljeni. Vrsta hibridizacije atomov v dani snovi pomeni spremembo oblike atomskih orbital, izvlečene so in poravnane glede na tocke tetraedra. Posledično molekula vode dobi kotno obliko, med kisikovo-vodikovimi vezmi pa je valenčni kot 104,5 o .
Za napovedovanje vrste hibridizacije lahko uporabite donorsko-akceptorski mehanizem za tvorbo kemičnih vezi. Posledično je izvedeno prekrivanje prostih orbital elementa z nižjo elektronegativnostjo, kot tudi orbitale elementa z večjo električno negativnostjo, na kateri se nahaja par elektronov. V postopku zbiranja elektronsko konfiguracijo atom upošteva stopnjo njihove oksidacije.
Ad
Pravila za identifikacijo vrste hibridizacije
Za določitev vrste hibridizacije ogljika lahko uporabite določena pravila:
- razkrili osrednji atom, izračunali število σ-vezi;
- dajo delce oksidacijskega stanja atomov;
- beleženje elektronske konfiguracije glavnega atoma v želeni stopnji oksidacije;
- naredite diagram porazdelitve valentnih elektronov v orbitale, ki združujejo elektrone;
- oddajajo orbitale, ki neposredno sodelujejo pri nastanku vezi, iščejo neparne elektrone (če število valentnih orbital ni dovolj za hibridizacijo, orbitale naslednjih energije).
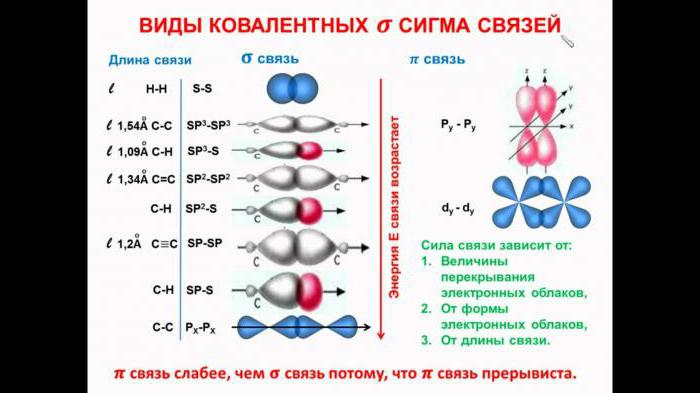
Geometrijo molekule določimo z vrsto hibridizacije. Prisotnost vezav pi ne vpliva nanj. V primeru dodatnega vezanja je možna sprememba valenčnega kota, vzrok je vzajemno odbijanje elektronov, ki tvorijo večkratno vez. Torej, v molekuli dušikov oksid (4) s sp 2 hibridizacijo se valenčni kot povečuje z 120 stopinj na 134 stopinj.
Hibridizacija amoniaka
Nepovezani par elektronov vpliva na rezultat indeksa dipolnega momenta celotne molekule. Amoniak ima tetraedrično strukturo z neločenim parom elektronov. Ionske vezi dušik-vodik in dušik-fluor imajo indikatorje 15 in 19 odstotkov, dolžine pa 101 in 137 pm. V molekuli dušikovega fluorida bi torej moral obstajati večji dipolni moment, vendar eksperimentalni rezultati kažejo na nasprotno.
Ad
Hibridizacija v organskih spojinah
Vsak razred ogljikovodikov ima svoj tip hibridizacije. Tako pri tvorbi molekul razreda alkanov (nasičenih ogljikovodikov) vsi štirje elektroni ogljikovega atoma tvorijo hibridne orbitale. Ko se prekrivajo, se oblikujejo 4 hibridni oblaki, ki se raztezajo do tock tetraedra. Poleg tega se njihova vozlišča prekrivajo z ne-hibridnimi s-orbitali vodika in tvorijo preprosto vez. Za nasičene ogljikovodike je značilna sp 3 hibridizacija.
Pri nenasičenih alkenih (njihov tipični predstavnik je etilen) sodelujejo le tri elektronske orbitale v hibridizaciji - s in 2 p, tri hibridne orbitale tvorijo v prostoru trikotno obliko. Ne-hibridni p-orbitali se prekrivajo in ustvarjajo večkratno vez v molekuli. Ta razred organskih ogljikovodikov je označen s sp2 hibridnim stanjem ogljikovega atoma.
Alkine se od prejšnjega razreda ogljikovodikov razlikujejo po tem, da sta v procesu hibridizacije vključeni samo dve vrsti orbital: s in p. Dva ne-hibridna p-elektrona, ki ostajata na vsakem atomu ogljika, se prekrivata v dveh smereh in tvorita dve večkratni vezi. Za ta razred ogljikovodikov je značilno sp-hibridno stanje ogljikovega atoma.
Zaključek
Z opredelitvijo vrste hibridizacije v molekuli je mogoče razložiti strukturo različnih anorganskih in organskih snovi ter predvideti možne kemijske lastnosti določene snovi.