Kemične in fizikalne lastnosti aluminija. Fizikalne lastnosti aluminijevega hidroksida
Ta lahka kovina s srebrno belim odtenkom je skoraj povsod v sodobnem življenju. Zaradi fizikalnih in kemijskih lastnosti aluminija se ta uporablja v industriji. Najbolj znani depoziti so v Afriki, Južni Ameriki in na Karibih. V Rusiji so rudarske lokacije boksita na Uralu. Svetovni voditelji v proizvodnji aluminija so Kitajska, Rusija, Kanada, ZDA. 
Al mining
V naravi se ta srebrna kovina zaradi svoje visoke kemijske aktivnosti nahaja le v obliki spojin. Najbolj znane geološke kamnine, ki vsebujejo aluminij, so boksit, aluminijev oksid, korund, feldspate. Boksit in aluminijev oksid sta industrijskega pomena, saj le-te teh rud omogočajo pridobivanje aluminija v njegovi čisti obliki.
Ad
Lastnosti
Fizikalne lastnosti aluminija olajšajo potegniti kovino v žico in jo zaviti v tanke liste. Ta kovina ni trajna, zato da bi povečala ta indikator med taljenjem, je legirana z različnimi dodatki: baker, silicij, magnezij, mangan, cink. Za industrijske namene je pomembno, da je druga fizikalna lastnost aluminijeve snovi njegova sposobnost hitre oksidacije v zraku. V naravnih pogojih je površina aluminijastega izdelka običajno prevlečena s tankim oksidnim filmom, ki učinkovito ščiti kovino in preprečuje njeno korozijo. Ko se ta film uniči, se srebrna kovina hitro oksidira, medtem ko se temperatura znatno poveča.
Notranja struktura aluminija
Fizikalne in kemijske lastnosti aluminija so v veliki meri odvisne od njegove notranje strukture. Kristalna rešetka Ta element je vrsta kocke, osredotočene na obraz. 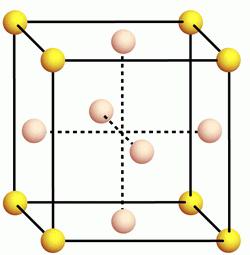 Ta vrsta rešetke je del številnih kovin, kot so baker, brom, srebro, zlato, kobalt in druge. Zaradi visoke toplotne prevodnosti in zmožnosti vodenja električne energije je ta kovina ena najbolj iskanih na svetu. Preostale fizikalne lastnosti aluminija, katerih tabela je predstavljena spodaj, v celoti razkrivajo njene lastnosti in prikazujejo obseg njihove uporabe.
Ta vrsta rešetke je del številnih kovin, kot so baker, brom, srebro, zlato, kobalt in druge. Zaradi visoke toplotne prevodnosti in zmožnosti vodenja električne energije je ta kovina ena najbolj iskanih na svetu. Preostale fizikalne lastnosti aluminija, katerih tabela je predstavljena spodaj, v celoti razkrivajo njene lastnosti in prikazujejo obseg njihove uporabe. 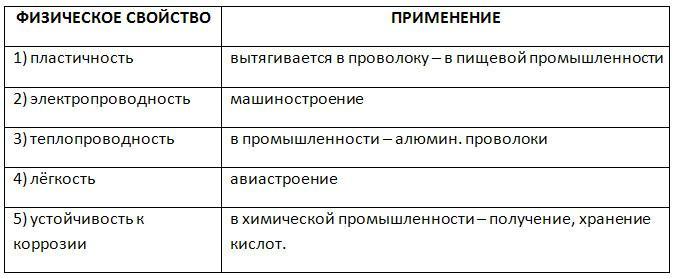
Legiranje aluminija
Fizikalne lastnosti bakra in aluminija so takšne, da ko se aluminijevi zlitini doda določena količina bakra, se njegova kristalna rešetka upogne in trdnost zlitine se poveča. Al temelji na tej lastnosti zlitin lahkih zlitin, da poveča njihovo trdnost in odpornost na agresivna okolja.
Ad
Razlaga procesa strjevanja je v obnašanju bakrovih atomov v kristalni rešetki aluminija. Delci Cu se nagibajo k padcu iz kristalne rešetke Al, so združeni v njenih posebnih območjih. 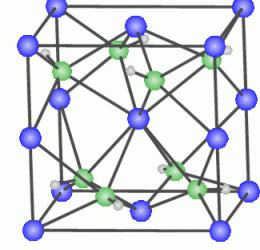 Kjer atomi bakra tvorijo grozde, se tvori mešana CuAl2 kristalna rešetka, v kateri so v skupni kristalni rešetki aluminija istočasno vključeni srebrni kovinski delci, v mešani CuAl 2 rešetki . običajno. To pomeni, da je moč novo oblikovane snovi veliko višja.
Kjer atomi bakra tvorijo grozde, se tvori mešana CuAl2 kristalna rešetka, v kateri so v skupni kristalni rešetki aluminija istočasno vključeni srebrni kovinski delci, v mešani CuAl 2 rešetki . običajno. To pomeni, da je moč novo oblikovane snovi veliko višja.
Kemijske lastnosti
Interakcija aluminija z razredčeno žveplovo kislino in. T klorovodikovo kislino. Pri segrevanju se ta kovina zlahka raztopi v njih. Hladno koncentrirana ali zelo razredčena dušikove kisline ne raztopi tega elementa. Vodne raztopine alkalij aktivno vplivajo na snov, med reakcijo tvorijo aluminatne soli, ki vsebujejo aluminijeve ione. Na primer:
Ad
Al2O3 + 3H2O + 2NaOH = 2Na [Al (OH) 4 ]
Nastalo spojino imenujemo natrijev tetrahidroksoaluminat.
Tanka folija na površini aluminijastih izdelkov ščiti to kovino ne samo od zraka, ampak tudi od vode. Če se ta tanka pregrada odstrani, bo element močno vplival na vodo in iz nje sprostil vodik.
2AL + 6H2O = 2 AL (OH) 3 + 3H2
Nastala snov se imenuje aluminijev hidroksid.
AL (OH) 3 reagira z alkalijami in tvori kristale hidroksialuminata:
Al (OH) 2 + NaOH = 2Na [Al (OH) 4 ]
Če se tej kemični enačbi doda prejšnja, dobimo formulo za raztapljanje elementa v alkalni raztopini.
Al (OH) 3 + 2NaOH + 6H2O = 2Na [Al (OH) 4 ] + 3H2
Alu gori
Fizikalne lastnosti aluminija omogočajo, da reagira s kisikom. Če se prah te kovinske ali aluminijaste folije segreje, potem utripa in gori z belim plamenom. Ob koncu reakcije nastane aluminijev oksid Al2O3 .
Alumina
Nastala glinica ima geološko ime aluminijev oksid. V naravnih pogojih se nahaja v obliki korunda - trdnih prozornih kristalov. Korund se odlikuje po visoki trdoti, njen indeks v lestvici trdnih snovi je 9. Sam korund je brezbarven, toda različne nečistoče ga lahko pobarvajo rdeče in modro, tako da dobimo dragulje, ki se v nakitu imenujejo rubini in safirji.
Ad
Fizikalne lastnosti aluminijevega oksida omogočajo gojenje teh dragih kamnov v umetnih pogojih. Tehnični dragulji se ne uporabljajo samo za nakit, temveč se uporabljajo tudi za izdelavo natančnih instrumentov, za izdelavo ur in drugih stvari. V laserskih napravah se pogosto uporabljajo tudi umetni kristali rubina. 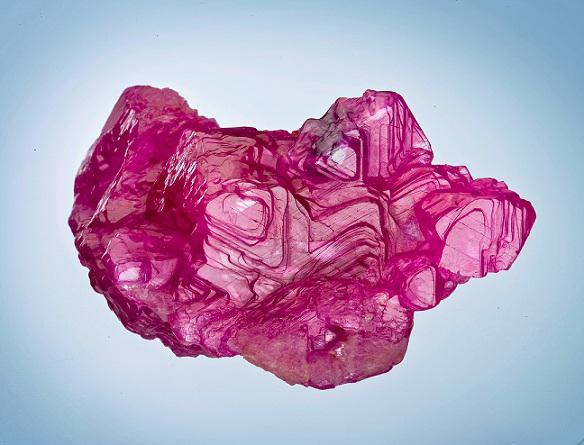
Drobnozrnate sorte korunda z veliko količino nečistoč, ki se odlagajo na posebno površino, ki je vsem znana kot smirka. Fizikalne lastnosti aluminijevega oksida pojasnjujejo visoke abrazivne lastnosti korunda, pa tudi trdoto in odpornost na trenje.
Aluminijev hidroksid
Al2 (OH) 3 je tipičen amfoterni hidroksid. V kombinaciji s kislino ta snov tvori sol, ki vsebuje pozitivno nabite aluminijeve ione, v alkalijah tvorijo aluminate. Amfoterična snov se kaže v dejstvu, da se lahko obnaša kot kislina in kot alkalija. Ta spojina lahko obstaja v želeju ali trdni obliki.  Praktično netopen v vodi, vendar reagira z večino aktivnih kislin in alkalij. Fizikalne lastnosti aluminijevega hidroksida se uporabljajo v medicini, je priljubljen in varen način za zmanjšanje kislosti v telesu, uporablja se pri gastritisu, duodenitisu, razjedah. V industriji se kot adsorbent uporablja Al 2 (OH) 3 , ki odlično očisti vodo in obori škodljive elemente, raztopljene v njem.
Praktično netopen v vodi, vendar reagira z večino aktivnih kislin in alkalij. Fizikalne lastnosti aluminijevega hidroksida se uporabljajo v medicini, je priljubljen in varen način za zmanjšanje kislosti v telesu, uporablja se pri gastritisu, duodenitisu, razjedah. V industriji se kot adsorbent uporablja Al 2 (OH) 3 , ki odlično očisti vodo in obori škodljive elemente, raztopljene v njem.
Industrijska uporaba
Aluminij so odkrili leta 1825. Sprva je bila ta kovina vrednotena nad zlatom in srebrom. To je posledica zapletenosti njegovega pridobivanja iz rude. Fizikalne lastnosti aluminija in njegova sposobnost hitrega oblikovanja zaščitne folije na njeni površini je otežila preučevanje tega elementa. Šele konec 19. stoletja je bila primerna metoda taljenja čistega elementa, primernega za industrijsko uporabo. 
Lahkost in odpornost proti koroziji so edinstvene fizikalne lastnosti aluminija. Zlitine te srebrne kovine se uporabljajo v raketni tehnologiji, v proizvodnji avtomobilov, ladij, letal in instrumentov, pri proizvodnji jedilnega pribora in namiznega pribora.
Ad
Kot čista kovina se Al uporablja pri izdelavi delov za kemično opremo, električne žice in kondenzatorje. Fizikalne lastnosti aluminija so takšne, da njegova električna prevodnost ni tako visoka kot pri bakru, vendar je ta pomanjkljivost kompenzirana z lahkoto zadevne kovine, ki omogoča izdelavo debelejših žic iz aluminija. Torej, z isto električno prevodnostjo, aluminijasta žica tehta dvakrat manj od bakra.
Enako pomembna je uporaba Al v procesu aluminizacije. To je tako imenovana reakcija nasičenja površine izdelka iz litega železa ali jekla z aluminijem, da bi zaščitili osnovno kovino pred korozijo pri segrevanju.
Trenutno so dokazane zaloge aluminijevih rud primerljive s potrebami ljudi v tej srebrni kovini. Fizikalne lastnosti aluminija lahko svojim raziskovalcem prinesejo veliko več presenečenj, področje uporabe te kovine pa je veliko širše, kot si lahko predstavljamo.