Kako izgleda anilinska formula?
Kaj je anilin? Kemijska formula te spojine kaže, da spada neposredno v dva glavna razreda organskih snovi. Je aromatski amin. Oglejmo podrobneje značilnosti njegove strukture, proizvodnje, uporabe.
Lastnosti aminov
To so snovi, ki izvirajo iz anorganskega amoniaka. Eden ali več vodikovih atomov je nadomeščenih z ogljikovodikovimi radikali. Kako izgleda anilinska formula? Kemija aromatskih aminov, ki ji ta spojina pripada, ima aromatski obroč in amino skupino. Lahko se imenuje fenilamin.
Anilinska struktura
Da bi razumeli formulo anilina, napišemo njeno molekulo. Ta snov je prva predstavnica v številnih aromatskih aminah. V njem je amino skupina povezana z aromatičnim jedrom. Prisotnost amino skupine daje tej spojini osnovne lastnosti.
Ad
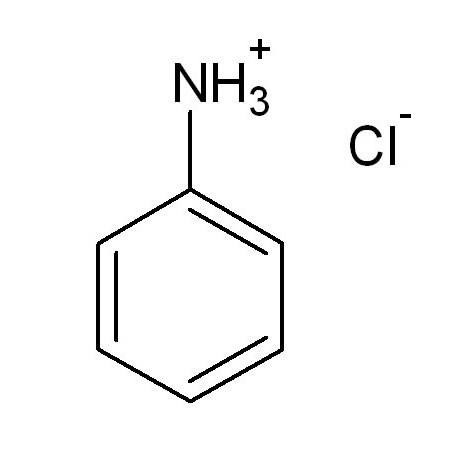
Pridobivanje
Formula anilina je znana že od leta 1826. V tem času se je spojina učila z destilacijo indigo indikatorja hidrirano apno. Nastala snov se je imenovala "kristalinična". Malo kasneje je Runge izoliral anilin iz premogovega katrana. Sredi devetnajstega stoletja je Frishtse sintetiziral ta amin pri segrevanju z raztopino kalijev hidroksid indigo
Ta znanstvenik je opisal anilinsko formulo. Okoli istega zgodovinskega obdobja je Nikolai Zinin sintetiziral to organsko spojino z zmanjšanjem nitrobenzena.
V laboratorijskih pogojih je ta spojina pridobljena z interakcijo v kislem okolju cinka z nitrobenzenom.
Vpliv skupin atomov v molekuli
Amino skupina je donor prostih elektronov, zato premika elektronsko gostoto v obroč. Orientant prve vrste, ki je skupina NH2, koncentrira presežno gostoto v enakih položajih (orto, para). Posledica tega je, da je anilinska formula sposobna zamenljivih reakcij v benzenskem obroču, ki se pojavljajo v parnih (2, 4, 6 pozicijah).
Ad
Del opazovanega zamika elektronske gostote, ki vodi do slabšanja osnovnih lastnosti te spojine v primerjavi z alifatskimi amini.
V vodni raztopini anilina ni opaziti spremembe barve indikatorjev, kar je pojasnjeno z učinkom na amino skupino benzenskega obroča.
Fizične lastnosti
Ta organska spojina je brezbarvna oljnata tekočina s specifičnim vonjem. Malo anilina težji od vode. Ta amin ima odlično topnost v organskih topilih, slabo topen v vodi. Spojina se hitro oksidira v zraku in pridobi značilno rjavo-rdečo barvo. Anilin je strup.
Značilnosti kemijskih lastnosti
Za razliko od benzena je za anilin značilna interakcija z bromovo vodo, kar vodi do nastanka netopne oborine 2,4,6-tribromanilina.
Poleg tega ta amin medsebojno deluje z raztopino klora v etanolu. Osnovne lastnosti anilina se kažejo v interakciji z močnimi anorganskimi kislinami. Na primer, v reakciji z dušikova kislina, Nastane 2,4,6-trinitroanilin.
Ad
Preveč kisika, anilin opekline, sprošča dušik, vodne pare in ogljikov dioksid.
Z dušikovo kislino tvori diazo spojine. Glede na to, da je diazonijeva skupina zamenjana brez težav z drugimi funkcionalnimi skupinami, so take spojine potrebne v organski sintezi. Diazo spojin ni treba izolirati v obliki kristalov, lahko jih uporabimo v sveže pripravljeni različici.

Zaključek
Kako izgleda anilinska barvna formula? To so soli tega amina, ki omogočajo pridobivanje barv različnih barv. Anilin daje tkanini bogat odtenek, vendar pod vplivom sončne svetlobe pride do izgube prvotne barve.
Barve so nestabilne glede na vodo, s prekomerno vlago, njihove lastnosti so izgubljene. Trenutno podjetja, ki proizvajajo anilinska barvila, sistematično posodabljanje tehnologije, ki pozitivno vpliva na kemijske in fizikalne lastnosti anilinskih barvil, povečuje področje njihove praktične uporabe.