Vrste kemijskih vezi. Kako povezati atome?
Kemija je neverjetna in, priznam, zapletena znanost. Iz neznanega razloga je povezana s svetlimi poskusi, večbarvnimi epruvetami, debelimi oblaki pare. Toda malo ljudi misli o tem, od kod prihaja ta »magija«. Dejstvo je, da reakcija ne poteka brez tvorbe spojin med atomi reaktantov. Poleg tega so ti "skakalci" včasih najdeni v preprostih elementih. Vplivajo na sposobnost reagiranja snovi in pojasnjujejo nekatere njihove fizikalne lastnosti.
Katere vrste kemičnih vezi obstajajo in kako vplivajo na spojine?
Teorija
Začeti moramo z najpreprostejšimi. Kemična vez je interakcija, v kateri se atomi snovi združijo v bolj kompleksne snovi. Napačno je verjeti, da je to značilno le za spojine, kot so soli, kisline in baze - celo preproste snovi, katerih molekule so sestavljene iz dveh atomov, imajo te »mostove«, če lahko tako pogojno kličete vez. Mimogrede, pomembno je, da se spomnimo, da se lahko združijo le atomi z različnimi naboji (to so temelji fizike: enako nabiti delci se odbijajo, nasprotni pa se med seboj privlačijo), tako da v kompleksnih snoveh vedno obstaja kation (ion s pozitivnim nabojem) in anion (negativni delci). in sama povezava bo vedno nevtralna.
Zdaj bomo poskušali razumeti, kako nastane kemična vez.
Mehanizem izobraževanja
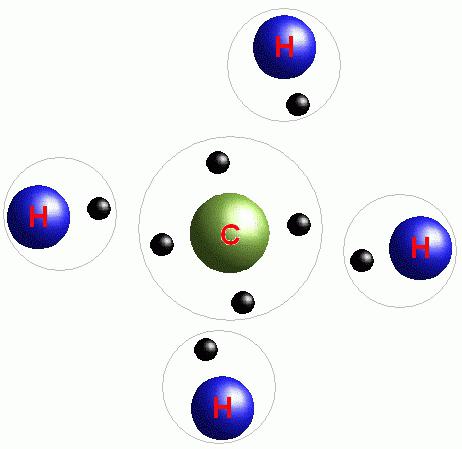
Vsaka snov ima določeno število elektronov, razporejenih v energetskih slojih. Najbolj obremenjena je najbolj oddaljena plast, na kateri se običajno nahaja najmanjša količina teh delcev. Njihovo število lahko ugotovite tako, da pogledate številko skupine (vrstica s številkami od enega do osem na vrhu periodnega sistema), v kateri se nahaja kemični element, število energijskih plasti pa je enako številu obdobja (od enega do sedem, navpična črta na levi strani elementov).
V idealnem primeru je v zunanji energijski plasti osem elektronov. Če niso dovolj, jih atom poskuša povleči iz drugega delca. Med izbirnim postopkom elektronov, potrebnih za dokončanje zunanjega energetskega sloja, nastanejo kemične vezi. Njihovo število se lahko spreminja in je odvisno od števila valenc ali neparnih delcev (da bi ugotovili, koliko jih je v atomu, morate narediti njegovo elektronsko formulo). Število elektronov, ki nimajo para, bo enako številu nastalih vezi.
Malo več o vrstah
Vrste kemijskih vezi, ki nastanejo med reakcijami ali preprosto v molekuli snovi, so v celoti odvisne od samega elementa. Obstajajo tri vrste "skakalcev" med atomi: ionski, kovinski in kovalentni. Slednji je razdeljen na polarne in nepolarne.
Da bi razumeli, s kakšnimi veznimi atomi so povezani, uporabite nekakšno pravilo: če so elementi v desnem in levem delu tabele (to so, so kovine in nekovine, na primer NaCl), potem je njihova povezava odličen primer ionske vezi. Dva oblika nekovin kovalentna polarna vez (HCl) in dva atoma iste snovi, ki se združita v eno molekulo - kovalentno nepolarno (Cl 2 , O 2 ). Zgornje vrste kemičnih vezi niso primerne za snovi, ki jih sestavljajo kovine - obstajajo samo kovinska vez.
Kovalentna interakcija
Kot smo že omenili, imajo vrste kemičnih vezi določene učinke na snovi. Na primer, kovalentni "most" je zelo nestabilen, zato se spojine z njim zlahka uničijo z najmanjšim zunanjim vplivom, na primer z ogrevanjem. Vendar pa gre le za molekularne snovi. Tisti, ki imajo ne-molekularno strukturo, so praktično neuničljivi (odličen primer je kristal diamanta - kombinacija ogljikovih atomov).

Nazaj na polarno in nepolarno kovalentna vez. Pri nepolarnem je vse preprosto - elektroni, med katerimi se oblikuje »most«, so enako oddaljeni od atomov. Toda v drugem primeru se premaknejo na enega od elementov. Zmagovalec v "preobremenjenosti" bo snov, katere elektronegativnost (sposobnost privabljanja elektronov) je višja. Določena je s posebnimi tabelami, in večja je razlika te velikosti med dvema elementoma, bolj polarna bo povezava med njimi. Res je, da je edina stvar, za katero je lahko koristno znanje o elektronegativnosti elementov, definicija kationa (pozitivni naboj - snov, ki ima to količino manj) in anion (negativni delec z boljšo sposobnostjo privabljanja elektronov).
Jonska vez
Za kombinacijo kovin in nekovin niso primerne vse vrste kemičnih vezi. Kot je omenjeno zgoraj, če je razlika v elektronegativnosti elementov ogromna (in to velja, če se nahajajo v nasprotnih delih tabele), se med njimi tvori ionska vez. V tem primeru se valentni elektroni od atoma z nižjo elektronegativnostjo prenesejo na atom z večjim, tvorijo anion in kation. Najbolj presenetljiv primer take vezi je spojina halogena in kovine, na primer AlCl2 ali HF.
Kovinska vez
S kovinami je še vedno lažje. Zgornje vrste kemičnih vezi so tuje, ker imajo svoje. Lahko združuje oba atoma ene snovi (Li 2 ) in različna (AlCr 2 ), v slednjem primeru nastanejo zlitine. Če govorimo o fizičnih lastnostih, potem kovine združujejo v sebi plastičnost in moč, to pomeni, da se pri najmanjšem vplivu ne uničijo, ampak preprosto spremenijo obliko.

Intermolekularna vez
Mimogrede, kemijske vezi v molekulah obstajajo. Imenujejo se medmolekularni. Najpogostejši tip je vodikova vez, v kateri atom vodika izposodi elektrone iz elementa z visoko elektronegativnostjo (npr. Iz vodne molekule).