Oksidacijsko sredstvo je atom, ki sprejema elektrone.
Oksidacijsko sredstvo in redukcijsko sredstvo uporabljamo za formuliranje reakcije v organski in anorganski kemiji. Preučimo glavne značilnosti takih interakcij, identificiramo algoritem za kompilacijo enačbe in razporeditev koeficientov.

Definicije
Oksidator je atom ali ion, ki pri interakciji z drugimi elementi sprejema elektrone. Proces izdelave elektronov se imenuje redukcija in je povezan z zmanjšanjem stopnje oksidacije.
V teku anorganska kemija Upoštevata se dve glavni metodi določanja koeficientov. Reducirno sredstvo in oksidacijsko sredstvo v reakcijah določimo z elektronskim ravnotežjem ali s pol-reakcijsko metodo. Obravnavali bomo prvo metodo umeščanja koeficientov v OVR.
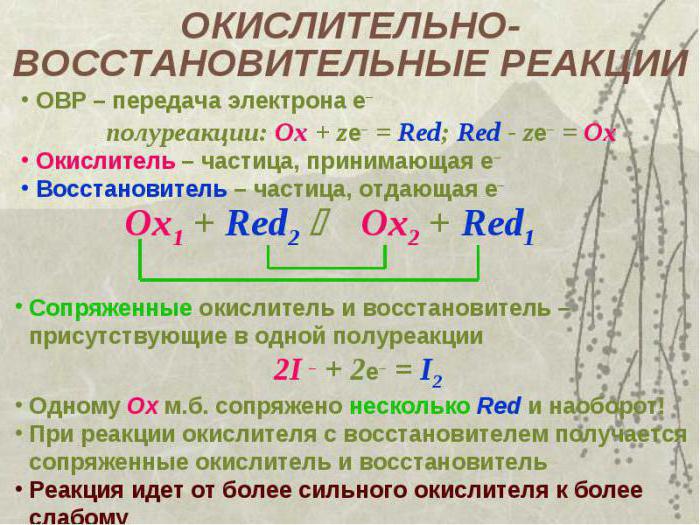
Oksidacijska stanja
Pred določitvijo oksidanta v reakciji morate postaviti oksidacijska stanja vse elemente v snoveh, vključenih v transformacijo. Predstavlja naboj atoma elementa, izračunanega po določenih pravilih. V kompleksnih snoveh mora biti vsota vseh pozitivnih in negativnih oksidacijskih stanj enaka nič. Za kovine glavnih podskupin ustreza valenci in ima pozitivno vrednost.
Za nekovine, ki se nahajajo v formuli na koncu, se stopnja določi z odštevanjem števila skupine od osem in ima negativno vrednost.
Za preproste snovi je enaka nič, ker ni postopka sprejemanja ali sproščanja elektronov.
Za kompleksne spojine, sestavljene iz več kemijskih elementov, se za določitev stopnje oksidacije uporabljajo matematični izračuni.
Oksidator je torej atom, ki v procesu interakcije znižuje svoje oksidacijsko stanje, nasprotno pa redukcijsko sredstvo povečuje njegovo vrednost.
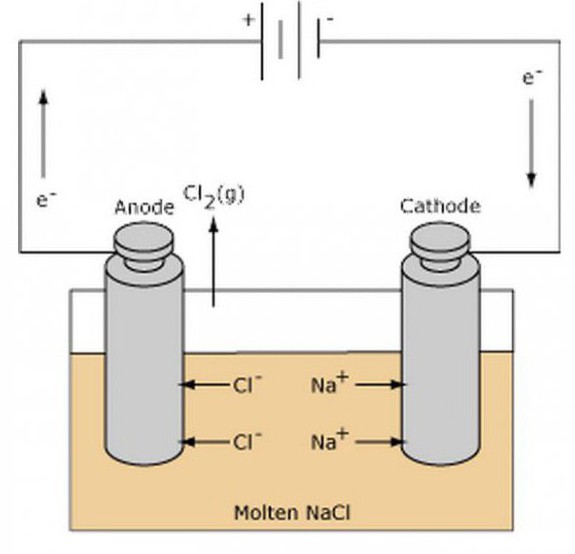
Primeri iad
Glavna značilnost nalog, povezanih s porazdelitvijo koeficientov pri redoks reakcijah, je definicija izpuščenih snovi in formulacija njihovih formul. Oksidacijsko sredstvo je element, ki bo sprejemal elektrone, poleg tega pa mora v reakciji sodelovati tudi reducent, ki jih oddaja.
Podan je splošni algoritem, s katerim lahko opravljate naloge, ki so ponujene diplomantom srednje šole na enem državnem izpitu. Razmislite o nekaj posebnih primerih, da bi razumeli, da oksidant ni le element v kompleksni snovi, ampak tudi preprosta snov.
Najprej je treba določiti vrednosti oksidacijskih stanj za vsak element z uporabo določenih pravil.
Nato morate analizirati elemente, ki niso sodelovali pri nastajanju snovi, in sestaviti formulo za njih. Po odstranitvi vseh rež lahko nadaljujete s postopkom priprave elektronskega ravnovesja med oksidacijskim sredstvom in reducentom. Dobljeni koeficienti se po potrebi vnesejo v enačbo in se dodajo tistim snovem, ki niso vključene v bilanco.
Na primer, z uporabo elektronske bilančne metode je treba dokončati predlagano enačbo, postaviti potrebne koeficiente pred formulami.
H 2 O 2 + H 2 SO 4 + KMnO 4 = MnSO 4 + O 2 + ... + ...
Za začetek bomo določili vrednosti oksidacijskih stanj, ki jih bomo dobili
+K + Mn +7 O 4 -2 = Mn +2 S +6 O 4 -2 + O 2 0 + …+… H 2+ O 2 - + H 2+ S + 6 O 4 -2 + K + Mn +7 O 4 -2 = Mn + 2 S +6 O 4 -2 + O 2 0 + ... + ...
V predlagani shemi se razlikujejo po kisiku in tudi pri manganu v kalijev permanganat. Tako najdemo redukcijsko sredstvo in oksidacijsko sredstvo. V desnem delu ni nobene snovi, v kateri bi bil kalij, zato namesto opustitev pripravimo formulo njegovega sulfata.
Nato napišemo elektronsko ravnovesje. Kisik bo v tem primeru pokazal redukcijske lastnosti, tako da bo dal dva elektrona. Mangan jih vzame in kaže oksidativno sposobnost.
Zadnji korak pri tej nalogi je določiti koeficiente.
5H 2 O 2 + 3H 2 SO 4 + 2KMnO 4 = 2Mn SO 4 + 5O 2 + 8H 2 O + K 2 SO 4
Kisline, kalijev permanganat, vodikov peroksid. Vse kovine imajo reducirne lastnosti, ki se spreminjajo v reakcije v katione s pozitivnim nabojem.
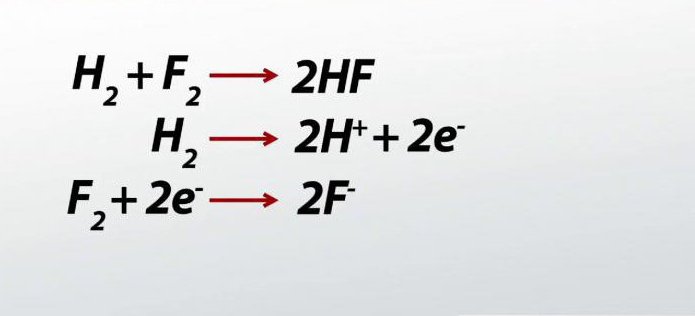
Zaključek
Procesi, povezani s sprejemanjem in sproščanjem negativnih elektronov, se pojavljajo ne le v anorganski kemiji. Presnova, ki se izvaja v živih organizmih, je jasna varianta poteka redoks reakcij v organski kemiji. To potrjuje pomembnost obravnavanih procesov, njihov pomen za živo in nežive naravo.