Proizvodnja alkoholov, uporaba, lastnosti. Metode za proizvodnjo alkoholov
Alkoholi so v naravi pogosti. Večino ljudi pozna etilni alkohol (etanol) je učinkovina v alkoholnih pijačah, vendar je le ena od družine organskih spojin, znanih kot alkoholi. Dobiti jih je bilo predvsem etil (vino kot rezultat encimske fermentacije grozdnega soka, je bil eden prvih kemičnih procesov, ki jih je človeštvo obvladalo.
Nomenklatura alkoholov
Alkoholi predstavljajo organske spojine hidroksilna (OH) funkcionalna skupina z alifatskim atomom ogljika. Ker je OH član molekul vseh alkoholov, so pogosto predstavljeni kot derivati vode s splošno formulo ROH, kjer R pomeni alkilno skupino.
Proizvodnja metanolnih alkoholov (CH 3 OH) in etanola (CH 3 CH 2 OH), ki sta prvi dve članici njunih homolognih serij, je pomembna naloga kemijske industrije v mnogih državah. Če vsebujejo od enega do štiri atome ogljika, se pogosto imenujejo splošna imena, v katerih po imenu alkilne skupine sledi beseda alkohol: 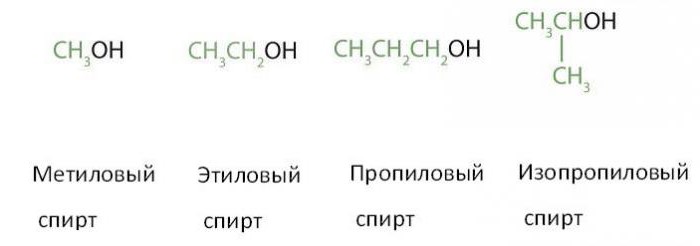
Vidimo lahko, da vsi štirje (zadnji dve sta izomera ene snovi), zgoraj navedene molekule alkohola vsebujejo eno hidroksilno skupino. Na tej podlagi spadajo v razred enodolnih alkoholov (obstajajo tudi dva, tri, štiri in poliatomski). Poleg tega so vsi derivati nasičenih ogljikovodikov iz številnih alkanov: metan, etan, propan (imena alkoholov dobimo z dodajanjem imena alkena končnemu "-ol"). Zato se imenujejo tudi obrobni monohidrični alkoholi.
Ad
Monohidrični alkoholi
Pridelava, lastnosti (fizikalne in kemijske) teh spojin so odvisne od števila atomov ogljika, povezanih z njegovim atomom, ki so neposredno povezani z OH skupino. Zato lahko na tej osnovi združimo monohidrične alkohole v tri razrede.
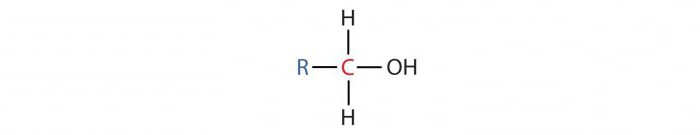
- Primarni alkoholi imajo molekulo, v kateri je en ogljikov atom vezan na OH skupino vezan na drug atom C. Njihova splošna formula je RCH20H. Etanol je na primer primarni alkohol.
- Sekundarni alkoholi imajo v molekuli en atom ogljika z OH skupino, vezano na dva druga C atoma, njihova splošna formula pa je R2CHOH. Sem spadajo propil in izopropil alkoholi.
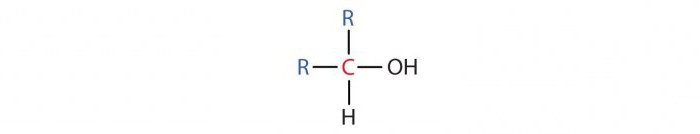
- Terciarni alkoholi vsebujejo v molekuli ogljikov atom z OH skupino, vezano na tri druge C atome, njihova splošna formula je R3COH.

Pridobivanje monohidričnih alkoholov v industriji je možno na več načinov, kar bomo obravnavali spodaj.
Metanol kot produkt zemeljskega plina
Metanol dobimo z mešanjem plina vodika in ogljikovega monoksida pri visokih temperaturah in tlakih (200 pri 350 ° C). v prisotnosti katalizatorja, ki sestoji iz cinkov oksid (ZnO) in kromovega oksida (Cr203) kot katalizatorja: 2H2 + CO → CH3OH. 
V tem primeru je surovina za proizvodnjo reagentov zemeljski plin in vodna para, ki mešata produkt sinteznega plina, ki je mešanica CO in H 2 .
Metanol je pomembno topilo in se uporablja kot avtomobilsko gorivo, bodisi kot čista tekočina - v nekaterih dirkalnih avtomobilih, ali kot visoko-oktanski dodatek bencinu. Proizvodnja in uporaba alkoholov na svetu, zlasti metanola, se meri v milijonih ton. Konec leta 2013 je bilo po vsem svetu porabljenih 66 milijonov ton metanola, od tega 65% v Aziji, 17% v Evropi in 11% v ZDA.
Ad
Pridobivanje najboljših alkoholov iz alkenov
Mnogo preprostih masnih alkoholov industrijskega pomena se proizvaja s hidracijo (z dodajanjem vode) alkenov (etilen, propilen, buten). S to reakcijo dobimo etanol, izopropanol, butanol (sekundarni in terciarni).
Znane so neposredne in posredne metode proizvodnje alkoholov s hidracijo. Neposredna vam omogoča, da se izognete nastanku stabilnih vmesnih proizvodov, običajno s pomočjo kislih katalizatorjev.
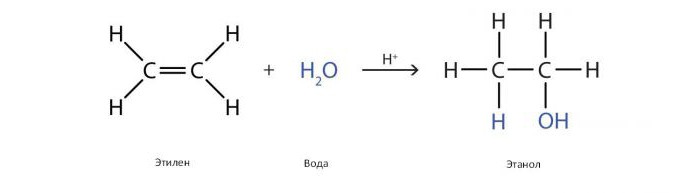
Katalizator je običajno fosforjeva kislina, na poroznem nosilcu, kot je silikagel ali kieselguhr. Ta katalizator je bil prvič uporabljen za proizvodnjo velike količine etanola v Združenih državah Amerike s strani Shella leta 1947. Reakcijo izvedemo v prisotnosti pare pod visokim tlakom pri 300 ° C, pri čemer se med etilenom in paro vzdržuje razmerje 1,0: 0,6.
Ad
Podobna reakcija na proizvodnjo izopropil alkohola s katalizatorji v obliki žveplove kisline izgleda tako 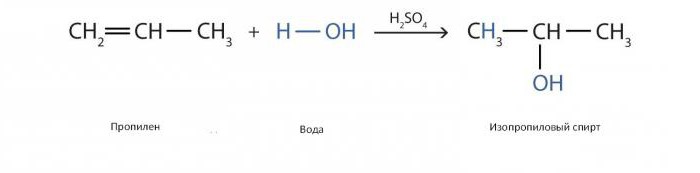
Posredna metoda hidratacije etilena
Posredno, v praksi prvič na industrijski ravni leta 1930, danes pa se šteje, da je skoraj popolnoma zastarela, je reakcija za proizvodnjo alkoholov pretvorba alkena v sulfatne estre, ki se nato hidrolizirajo. Tradicionalno, alken obdelamo z žveplovo kislino, da dobimo alkil sulfatne estre. Pri proizvodnji etanola se ta korak lahko napiše na naslednji način: H 2 SO 4 + C 2 H 4 → C 2 H 5 -O-SO 3 H
Nato ta sulfatni ester hidroliziramo, dokler se ne regenerira žveplova kislina in sprostimo etanol: C2H5-O-S03H + H20 → H2S04 + C2H5OH.
Metode za proizvodnjo alkoholov so izjemno raznolike, vendar je postopek, ki je opisan spodaj, verjetno znan, vsaj z govoricami, za vsakega bralca.
Alkoholna fermentacija
To je biološki proces, pri katerem se molekule, kot so glukoza, fruktoza in saharoza, pretvorijo v celično energijo z vzporedno proizvodnjo etanola in ogljikovega dioksida kot produkta presnove. Fermentacijo katalizirajo encimi, ki jih vsebujejo kvasovke, in poteka skozi kompleksen večstopenjski mehanizem, ki običajno vključuje pretvorbo (v prvi fazi) škroba, ki ga vsebujejo rastlinska zrna, v glukozo, ki ji sledi proizvodnja etanola. Ker kvas opravlja to transformacijo v odsotnosti kisika, se alkoholna fermentacija šteje za anaerobni proces.
Ad
Reakcije fermentacije alkoholov so lahko predstavljene na naslednji način: 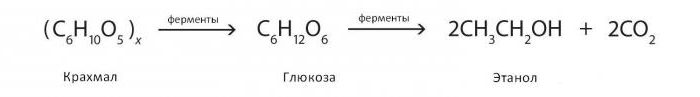
Možnosti za nakup alkoholnih pijač
Ves etanol, ki ga vsebujejo alkoholne pijače, se proizvaja s fermentacijo, ki jo povzroča kvas.
Vino se pridobiva s fermentacijo naravnih sladkorjev v grozdju; Jabolčnik se pridobiva z analogno fermentacijo naravnega sladkorja v jabolkih oz. Hruškah; in druga sadna vina se pridobivajo s fermentacijo sladkorjev v drugih vrstah sadja. Žganje in žganja (npr. Šljivovica) se proizvajajo z destilacijo pijač, pridobljenih s fermentacijo sadnih sladkorjev.
Medeni napitki se pridobivajo s fermentacijo iz naravnih sladkorjev v medu. 
Pivo, viski in vodka se proizvajajo s fermentacijo zrn škroba, ki se pretvorijo v sladkor z delovanjem encima amilaze, ki je prisotna v zrnih jedrcah, ki so bile podvržene kalju. V mešanico se lahko dodajo drugi viri škroba (npr. Krompir in zrna brez sladu), ker bo amilaza delovala tudi na njihov škrob.
Ad
Riževa vina (vključno s sakejem) se proizvajajo s fermentacijo žitnega škroba, ki ga Asugi Aspergillus ogugae pretvori v sladkor.
Rum in nekatere druge pijače se pridobivajo s fermentacijo in destilacijo sladkornega trsa. Rum je običajno narejen iz sladkornega trsa - melase.
V vsakem primeru naj pride do fermentacije v posodi, ki omogoča izpust ogljikovega dioksida, vendar preprečuje vstop zunanjega zraka. To je potrebno zato, ker učinek kisika preprečuje nastajanje etanola in kopičenje ogljikovega dioksida ustvarja tveganje za razpok plovila. 
Nukleofilna substitucijska reakcija
Alkoholi se proizvajajo v laboratorijih po metodah, ki uporabljajo kemične snovi različnih razredov, od ogljikovodikov do karbonilnih spojin, kot izhodne produkte za reakcije. Obstaja več načinov, ki se skrajšajo na nekaj osnovnih reakcij.
Primarni halogenoalkani reagirajo z vodnimi raztopinami alkalijskega NaOH ali KOH, pri čemer tvorijo predvsem primarne alkohole v reakciji nukleofilne alifatske substitucije. Ko npr. Metil bromid reagira z raztopino natrijevega hidroksida, se hidroksilne skupine, ki nastanejo med disociacijo alkalij, nadomestijo z bromovimi ioni z tvorbo metanola. 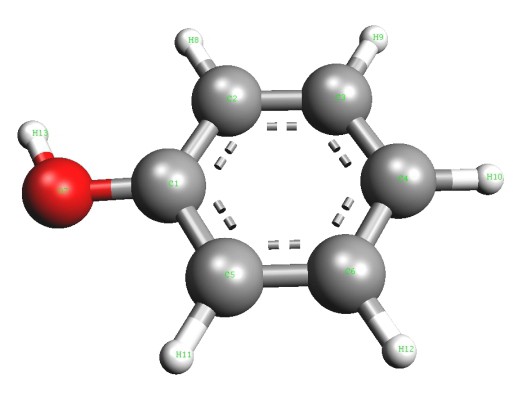
Spodaj je navedenih več reakcij, ki omogočajo proizvodnjo alkoholov v laboratorijih.
Nukleofilni dodatek.
Grignardovi reagenti (magnezijeve spojine z alkil halidi - jodidi ali bromidi) ter organokovinske spojine bakra in litija reagirajo z karbonilnimi skupinami (C = O) aldehidov, da tvorijo primarne in sekundarne alkohole, odvisno od mehanizma dodajanja. . 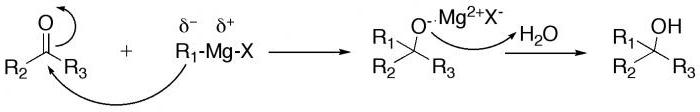
Barbierjeva reakcija poteka med halogen-alkanom in karbonilno skupino kot elektrofilnim substratom v prisotnosti magnezija, aluminija, cinka, indija, kositra ali njegovih soli. Reakcijski produkt je primarni, sekundarni ali terciarni alkohol. Njegov mehanizem je podoben Grignardovi reakciji, z razliko, da je Barbierjeva reakcija sinteza v eni posodi, medtem ko je Grignardov reagent pripravljen ločeno pred dodatkom karbonilne spojine. 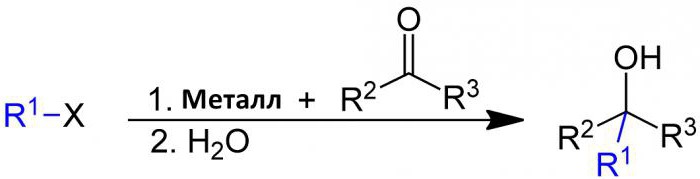 Kot nukleofilna adicijska reakcija se v nasprotju z relativno poceni in vodoodpornimi kovinami ali njihovimi spojinami, za razliko od Grignardovih reagentov ali organolitijevih reagentov. Iz tega razloga je v mnogih primerih mogoče voditi vodo v vodo, zaradi česar je proces del zelene kemije. Reakcija Barbier je poimenovana po Philipu Barbierju, učitelju Victorja Grignarda.
Kot nukleofilna adicijska reakcija se v nasprotju z relativno poceni in vodoodpornimi kovinami ali njihovimi spojinami, za razliko od Grignardovih reagentov ali organolitijevih reagentov. Iz tega razloga je v mnogih primerih mogoče voditi vodo v vodo, zaradi česar je proces del zelene kemije. Reakcija Barbier je poimenovana po Philipu Barbierju, učitelju Victorja Grignarda.
Reakcija obnove
Aldehidi ali ketoni so reducirani do alkoholov z natrijevim borohidridom (NaBH4) ali (po obdelavi s kislino) z litijevim aluminijevim hidridom (LiAlH).
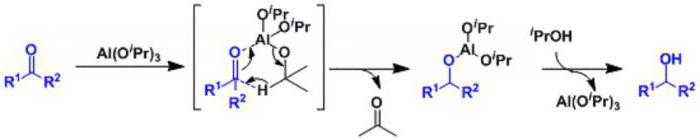
V reakciji Meerwein-Pondorf-Wehrli (MPV) se proizvodnja alkoholov z njihovo redukcijo iz ketonov in aldehidov izvaja s pomočjo aluminijevega alkoksidnega katalizatorja. Prednosti MPV so visoka kemoselektivnost in uporaba poceni, okolju prijaznega kovinskega katalizatorja. Reakcijo so odkrili Meerwein in Schmidt in neodvisno Verli leta 1925. Ugotovili so, da lahko zmes aluminijevega etoksida in etanola reducira aldehide v njihove alkohole. Ponndorf je uporabil reakcijo na ketone in posodobil katalizator na aluminijev izopropilat (Al (Oi-Pr) 3 , kjer je i-Pr izopropilna skupina (CH (CH3) 2 ). da dobimo izopropanol.
Splošna enačba za pridobivanje alkohola z redukcijo ketonov na alkohole z MPV je naslednja:
To seveda ni vse, kar lahko rečemo o alkoholih in njihovih lastnostih, vendar upamo, da vam je uspelo dobiti splošno predstavo o njih.