Glicerin: strukturna formula, lastnosti in uporaba
To je najpreprostejši triatomski alkohol. Kemična formula glicerola je C3H5 (OH) 3 . Je bistra viskozna tekočina. Brez vonja in sladkega okusa. Ni strupena, zato se pogosto uporablja v vsakdanjem življenju, živilski industriji, kozmetiki in medicini. Strukturna formula glicerola je prikazana na sliki. Toda kako je izkopana?
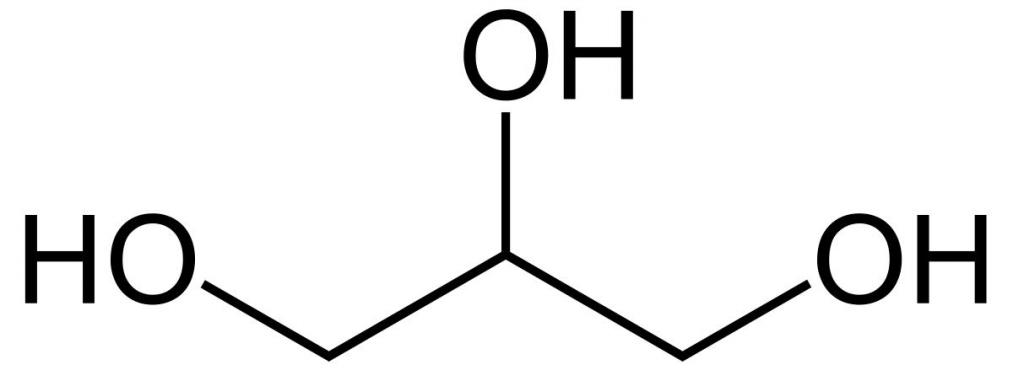
Možnosti za pridobivanje glicerina
Skoraj vsi industrijski glicerol se pridobiva iz maščob. S kemičnega stališča so estri glicerola. Med saponifikacijo teh maščob (milo) nastane glicerin kot stranski proizvod. Potem je zelo enostavno izstopati iz reakcijske zmesi.
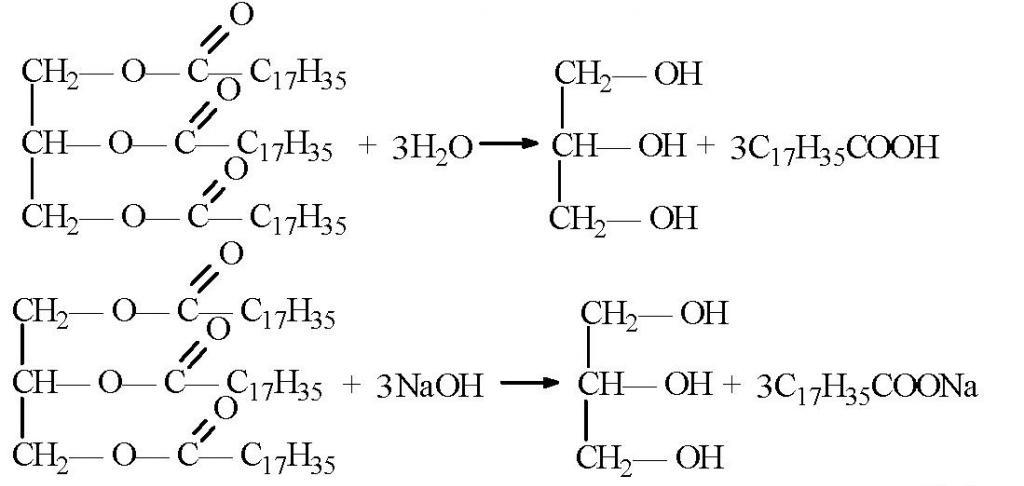
Glicerin je mogoče sintetizirati na druge načine. Na primer iz acetona. V tem primeru se reducira z vodikom, da dobimo izopropilni alkohol. V naslednjem koraku se molekula vode odcepi z dehidracijo, da dobimo propilen, ki se nato klorira. Dobljeni dikloropropan se ponovno klorira, da dobimo trikloropropan. Zadnja faza proizvodnje glicerola je hidrirana pri segrevanju. Na tej stopnji so vse tri molekule klora zamenjane s hidroksilnimi skupinami. Na podoben način zdaj v industriji prejmejo sintetične snovi. Samo kot surovina se uporablja propilen, ki se med destilacijo olja sprosti iz stranskih plinov.
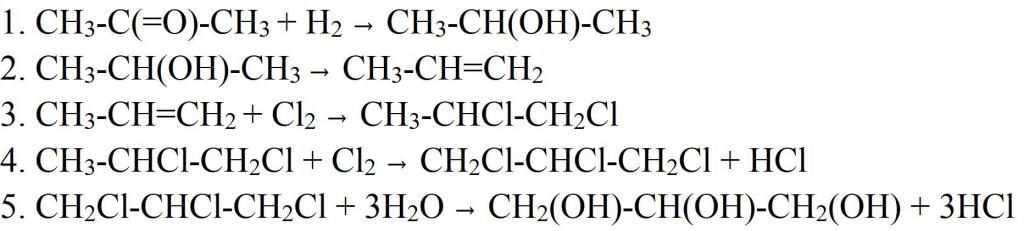
Ampak od propilena, da bi dobili glicerin je lahko drugačen način. Za to se propilen oksidira v akrolein. Oksidacijo izvedemo s kisikom v zraku v prisotnosti katalizatorja (bakra) in povišane temperature. Nato k temu dodamo vodikov peroksid, da dobimo dihidrov aldehidni alkohol. Osmijev oksid (VIII) se uporablja kot katalizator za to reakcijo. Aldehidna skupina v nastali spojini je hidrogenirana, tako da je postala tretja hidroksilna skupina. Izkazalo se je, da je glicerin.
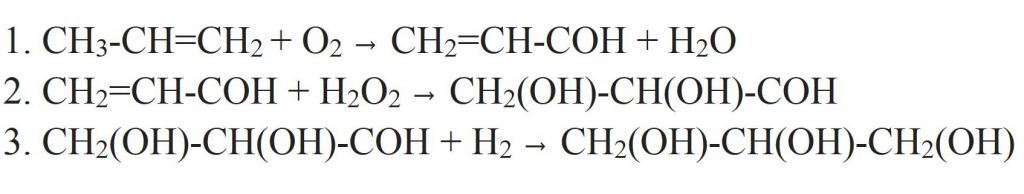
Druga različica sinteze naenkrat je predlagala EE Wagner. Z oksidacijo alilnega alkohola s kalijevim permanganatom v alkalnem mediju lahko dobimo glicerol v eni fazi.
Fizične lastnosti
Glicerin je brezbarvna tekočina brez vonja in sladkastega okusa. Je higroskopičen, kar pomeni, da je sposoben absorbirati vodo. Pri temperaturi 20 ° C se topi in pri temperaturi 290 ° C zavre z delnim razkrojem. Meša z vodo in alkoholi v vseh razmerjih. To je posledica kemijske formule. Hidroksilne skupine omogočajo glicerolu, da tvori veliko vodikovih vezi z vodnimi molekulami. To omogoča raztapljanje.
Raztopimo glicerin tudi v acetonu in nekaterih drugih organskih snoveh. Netopen v benzenu in etrih. Sam je lahko tak za mnoge organske in anorganske spojine. Njegova gostota v tekočem stanju je 1,26 g / cm 3 . Prav tako je treba omeniti, da je glicerin zelo viskozna tekočina. Lastnina je 1474-krat večja od vode.
Kemijske lastnosti
Prihaja iz strukturna formula Glicerin vsebuje tri hidroksilne skupine. Zato so za to značilne kemične reakcije enodolnih alkoholov. Poleg tega so kisle lastnosti glicerola veliko močnejše od tistih iz kateregakoli drugega enodolnega alkohola. Torej lahko komunicira s kovinami, njihovimi oksidi ali alkalijami. V nadaljevanju so predstavljene enačbe kemijskih reakcij glicerola.
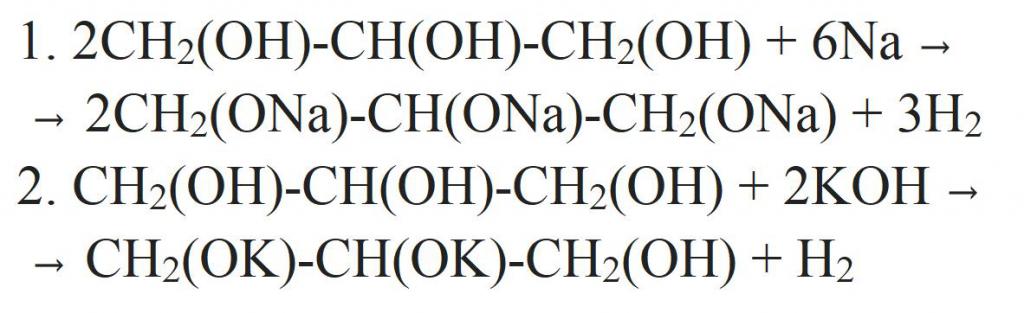
Lahko se vključi tudi v dehidracijske reakcije, ki tvorijo veliko različnih izdelkov. Torej dobite akrolein.
Ločeno je treba povedati o substituciji hidroksilne skupine za halogen. To se lahko zgodi, če glicerin medsebojno deluje z vodikovim halidom. Kot je razvidno iz strukturne formule glicerola, lahko kot rezultat reakcije nastanejo mono-, di- in tri-derivati. Bolj popolno zamenjavo lahko dosežemo, če se interakcija izvede s fosforjevimi halidi.
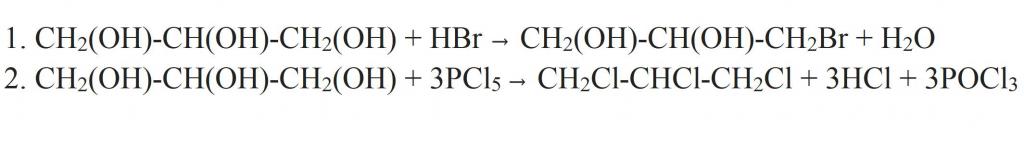
Toda glicerin ima specifične lastnosti, ki so edinstvene za polihidrične alkohole. Na primer, interagira z bakrovim (II) hidroksidom in tvori kompleksno spojino modre barve - bakrovega glicerata. Ta reakcija je kvalitativna za vse polihidrične alkohole.
Znaki zanj in reakcija zaestrenja. To je reakcija interakcij s kislinami, kar ima za posledico ester. Poleg tega je glicerin zaestren z organskimi in mineralnimi kislinami. Na primer, dušik. Ta reakcija se imenuje tudi nitriranje. Kot rezultat, se izkaže zelo koristen, vendar izjemno eksplozivni izdelek - nitroglicerin. Tudi iz strukturne formule glicerola lahko vidimo, da niso vse hidroksilne skupine lahko erificirane. Vse je odvisno od pogojev reakcije.
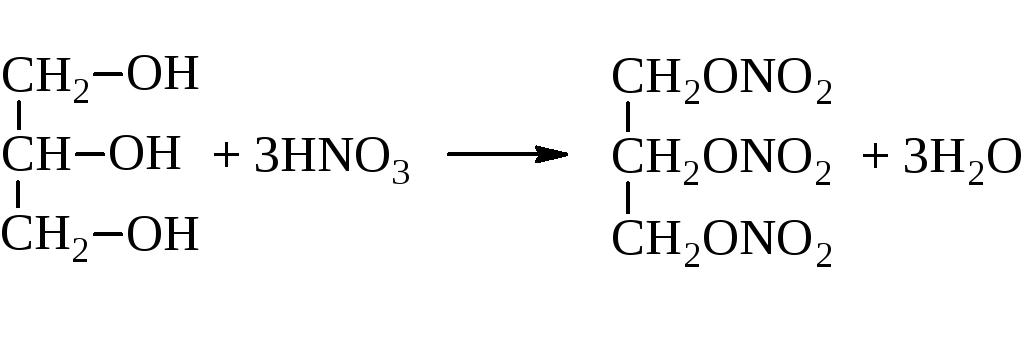
Pri medsebojnem delovanju z vodikom pri visokem tlaku in v prisotnosti katalizatorjev se zmanjša ena od hidroksilnih skupin. Kot rezultat reakcije dobimo dihidrični alkohol - propilenglikol.
Glicerin lahko vstopi tudi v reakcije polikondenzacije, pri čemer nastane zmes poliglicerolov. Za to se zelo dolgo segreva na skoraj 300 ° C v šibko alkalnem okolju. Pregledana je kemijska formula glicerina.
Oksidacija
Glicerin ima veliko možnosti oksidacije. Končni produkt je odvisen od narave oksidacijskega sredstva, katalizatorjev in drugih reakcijskih pogojev. Tako lahko glicerin oksidiramo z močnimi oksidacijskimi sredstvi, na primer s kalijevim dikromatom v kislem mediju. Zaradi te reakcije se ves glicerin razgradi v ogljikov dioksid in vodo.
Oksidacija se lahko pojavi bolj nežno. Na primer, z reakcijo z vodikovim peroksidom dobimo aldehid ali keton. Kot katalizator uporabimo soli železa (II).
Oksidacijo lahko izvedemo, da dobimo glicerinsko kislino. V tem primeru se interakcija izvede s koncentriranim dušikove kisline. Ena izmed hidroksilnih skupin se preprosto oksidira v karboksilno skupino. Iz glicerina dobimo tudi bolj eksotične kisline. Pri interakciji z raztopino kalijevega permanganata nastajajo tartronske in mezoksalne kisline. Ko oksidiramo z zrakom s segrevanjem v prisotnosti barijevega hidroksida, dobimo zmes oksalne in mravljične kisline. Jodna kislina glicerin se lahko oksidira v mravljični in formaldehidni.
Industrijske aplikacije
Glicerin se zaradi svoje sestave in lastnosti uporablja v industriji.
- V tekstilni industriji se uporablja za izdelavo mehkih in elastičnih tkanin ter za sintezo barvil in sintetičnih vlaken.
- Uporablja se pri izdelavi nekaterih vrst papirja.
- V usnjarski industriji se njene rešitve uporabljajo za strojenje in pitanje usnja.
- V kmetijstvu se semena obdelujejo z glicerinom, da se zagotovi bolj stabilna kalitev.
- V industriji barv se glicerin uporablja za sintezo polirnih spojin in lakov.
- Pri izdelavi embalažnih materialov, kot je celofan, se uporablja kot mehčalec.
- Polimeri na osnovi glicerina se uporabljajo za pakiranje. Papir, impregniran z glicerinom, pridobi požarno odporne lastnosti.
Uporaba v živilski industriji
Glicerin je prehransko dopolnilo E422. Uporablja se kot stabilizator za ohranjanje in povečevanje viskoznosti izdelkov. Uporablja se pri proizvodnji pekarskih in slaščičarskih izdelkov (zlasti čokolade) kot zgoščevalca in sredstva za zadrževanje vlage. Pomaga dodati količino končnih izdelkov. Zaradi tega dodatka lahko kruh ostane dlje časa svež.
Ekstrakti na osnovi glicerina se pogosto dodajajo pijačam. Omogočajo, da postane njihov okus manj oster. Uporablja se tudi pri proizvodnji alkohola. Dodajte in tobak za uravnavanje vlage, odpravite draži okus.
Medicinske aplikacije
Glicerin je del nekaterih zdravil, ki se uporabljajo pri zdravljenju kožnih bolezni. Ima antiseptične lastnosti, preprečuje okužbo ran. Prav tako pomaga pri zmanjševanju intrakranialnega in intraokularnega tlaka, zato se uporablja pri zdravljenju možganskega edema.
Ker je glicerin dobro topilo, se aktivno uporablja v farmakološki industriji. S to snovjo lahko dosežemo zelo visoko koncentracijo aktivne sestavine. Lahko da tudi želeno konsistenco zdravil. Pogosto se dodaja mazilom in kremam, saj preprečuje izhlapevanje vlage in sušenje.
Uporaba v kozmetologiji
Glicerin je del številnih kozmetičnih izdelkov: mila, šamponi, kreme, vlažilne maske. Ko pride v stik s kožo v majhnih količinah, zadrži vlago v zgornjih plasteh kože. Vendar pa nekateri trdijo, da pogosta uporaba izdelkov z glicerinovo bazo kožo prikrajša za naravno vlago in le še poslabša suho. Glicerin se pogosto uporablja kot dodatek v milu. S tem se poveča njegova sposobnost pranja.
Vpliv na človeško telo
Glicerin se v telesu dobro absorbira, saj ga prebavni sistem zlahka pretvori v maščobo. Zato se ne šteje za strupeno. Dnevna poraba te snovi ni omejena. Ampak ne pozabite, da je glicerin higroskopičen, zato vodi v veliko sproščanje volov v telesu, kar pomeni, da obstaja nevarnost dehidracije. Zato je njegova uporaba v živilskih proizvodih strogo urejena. Ko pride v stik s kožo, ima tudi učinek sušenja. Še vedno obstajajo razprave o potrebi po uporabi snovi v kozmetiki.
V članku smo preučili sestavo in lastnosti glicerina, njegovo uporabo.