Dietil eter: formula. Dietileter: fizikalne in kemijske lastnosti
Pred stotimi leti, znan tisti čas, Lully, ki se je po smrti imenoval alkimist, je odkril nepogrešljiv dietilni eter. Formula, lastnosti, vrelišče, metode pridobivanja snovi bodo podrobneje opisane v tem članku. 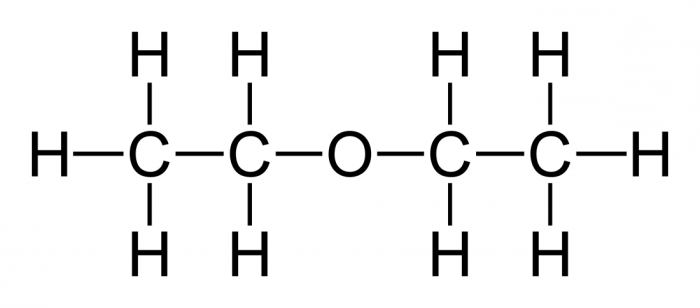
Zgodovina
V 13. stoletju je slavni španski znanstvenik Raymond Llull odkril dietil eter. Njegove lastnosti je leta 1540 opisal ne manj znani znanstvenik Paracelsus. Leta 1846 se je eter najprej uporabil kot anestezija. Operacija, ki jo je vodil ameriški zdravnik D. Warren z uporabo hlapov te snovi, je bila uspešna. Izumitelji anestezije se obravnavajo kot zobozdravnik W. Morton in njegov mentor - zdravnik in kemik C. Jackson.
Metode za pridobivanje etra so v 16. stoletju opisali Valerius Cordus, slavni botanik in farmacevt iz Kassela. Od začetka 18. stoletja je bila kot pomirjevalo uporabljena mešanica alkoholnega etra - to je bil predlog Friedricha Hoffmanna. Petersburgski farmacevt Thomas Lovits leta 1796 je prejel čisti dietil eter, katerega formula ima mimogrede dve možnosti (več o tem kasneje). Toda načelo delovanja omenjene snovi na človeškem telesu je napovedal angleški fizik M. Faraday, po katerem je leta 1818 objavljen celo znanstveni članek o tej temi. 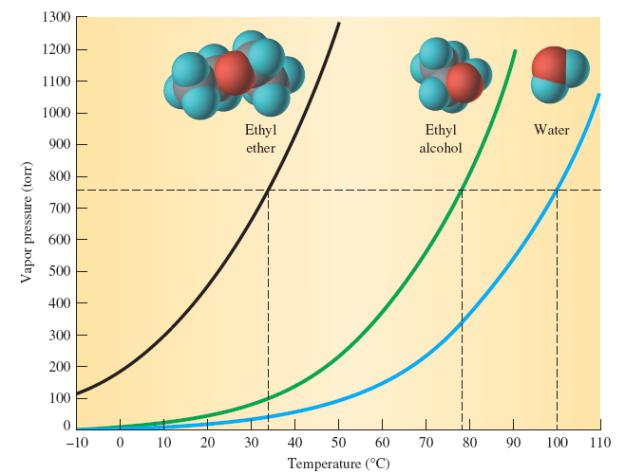
Značilno
Kaj se imenuje preprost eter? To je organske spojine katerih molekule sestavljajo dva ogljikovodikova radikala in kisikov atom. Najpomembnejši preprost, dietil eter, katerega formula ima naslednjo obliko:
(C2H5) 20 ali C4H10O.
Je brezbarvna, transparentna, zelo mobilna hlapna tekočina z značilnim vonjem in pekočim okusom.
Pod vplivom svetlobe, zraka, toplote in vlage se lahko eter razgradi, pri čemer nastanejo strupeni aldehidi, peroksidi in ketoni, ki dražijo dihalne poti.
Ko je temperatura vode 20 stopinj, se raztopi za 6,5%. Dobro se meša z mastnimi in eteričnimi olji, benzenom in alkoholom, ne glede na razmerje.
Sam eter pa je, tako kot njegove pare, lahko vnetljiv. V določenem razmerju s kisikom ali zrakom so pare dietiletra, ki se uporabljajo za anestezijo, eksplozivne. 
Kemijske lastnosti
Vse kemijske lastnosti etrov so značilne za dietil eter. Torej, obravnavajmo to vprašanje podrobneje. Je precej inertna snov. Glavna razlika od estrov je odsotnost hidrolize, čeprav obstajajo izjeme. Na mrazu ne vpliva na fosforjev klorid, kovinski natrij in veliko razredčenih mineralnih kislin. Kljub temu, koncentrirana kisline (žveplove) in vodikov jodid) razgradijo te estre tudi pri nizkih temperaturah, ogrevan kovinski natrij pa jih razdeli.
Eter z osamljenimi elektronskimi pari sodeluje s protonom močna kislina nastane nestabilna oksonijeva spojina:
- Acidoliza. Žveplove in jodovodikove kisline ter FeCl3 v anhidridu ocetne kisline so sposobne cepiti etre. Kemijska reakcija je naslednja: CH3-CH2-O-CH2-CH3 + HJ → CH3-CH2-OH + J-CH2-CH3.
- Reakcija metalacije, imenovana reakcija Shorygin. Ogrevani kovinski natrijev razcepi dietil eter: C2H5 - O - C2H5 + 2Na → C2H5ONa + C2H5Na
- Relativna kemična inertnost ne preprečuje nastajanju estrov v zraku, da tvorijo perokside, kar pogosto povzroči eksplozije na koncu destilacije.
Dietileter: fizikalne lastnosti
Poseben vonj, nizko vrelišče etrov - dokaz slabih intermolekularnih učinkov, kar kaže na nizko polarnost in odsotnost predpogojev za nastanek vodikovih vezi. V nasprotju z alkoholi imajo estri močnejše lastnosti, ki dajejo elektrone, kar potrjuje vrednost ionizacijskih potencialov. Izboljšanje teh lastnosti je povezano s pozitivnim induktivnim učinkom skupine atomov, ki se pridobijo iz alkanov, ko je vodikov atom odstranjen. 
Vrelišče dietiletra je 35,6 stopinj Celzija (veliko nižje kot pri izomernih alkoholih), zamrzovanje pa je 117 ° C. Eterji se skoraj ne mešajo z vodo. Razlaga za to je precej preprosta: ne morejo oblikovati vodikovih vezi, ker njihove molekule nimajo polarnih vezi. Slabo topen v vodi in dietil etru, katerega gostota glede na vodikov oksid je 0,714. Ena od značilnosti zadevne snovi je težnja po elektrifikaciji. Verjetnost statičnih izpustov je še posebej visoka pri transfuziji ali izpustu kemične sestave, zaradi česar lahko pride do vžiga. Hlapi etra tvorijo zrak, ki je 2,5-krat lažji, eksplozivne zmesi. Spodnja meja eksplozivnosti je 1,7%, zgornja pa 49%. Pri delu z etrom ne smemo pozabiti, da se njeni pari razprostirajo na dolge razdalje, ne da bi izgubili sposobnost izgorevanja. Zato je glavni previdnostni ukrep odsotnost odprtega ognja in drugih virov vžiga.
Eter je nizko aktivna spojina, manj reaktivna kot alkoholi. Izjemno raztaplja večino organske snovi, zato se uporablja kot topilo. Izjema ni dietil eter. Fizikalne lastnosti in kemikalije omogočajo njegovo uporabo v medicini in industriji.
Pridobivanje dietiletra
Eterji se v naravi ne pojavljajo - pridobivajo se sintetično. Pod vplivom kislih katalizatorjev etilni alkohol pri povišani temperaturi dobimo dietil eter (formula je navedena zgoraj). Najlažji način za pridobivanje te snovi je z destilacijo zmesi, ki jo sestavljajo žveplova kislina in alkohol. Če želite to narediti, je potrebno ogreti na 140-150 stopinj Celzija. Potrebovali bomo etil alkohol in žveplovo kislino (v enakih deležih), pipete, epruvete in parne cevi.
Po pripravi opreme in reagentov lahko poskus začnete. V epruveto (mora biti suha) vlijemo 2-3 ml mešanice alkohola in kisline ter jo počasi segrevamo. Takoj, ko se začne vretje, se gorilnik odstrani in 5 do 10 kapljic etilnega alkohola dodamo v vročo mešanico s pipeto vzdolž stene cevi. Reakcija poteka na naslednji način: t
- CH3-CH2-OH (etilsulfatna kislina) + H2S04 CH3-CH2-OSO3H + H20;
- CH3-CH2-OS03H + CH3-CH3-O;
- CH3-CH2-0-CH2-CH3 (dietileter) + H2S04.
Nastanek dietil etra se kaže v vonju, ki se je pojavil. 
Uporaba v medicini
Zdravniki uporabljajo dietil eter kot splošno anestetično zdravilo. Lastnosti te snovi ne dovoljujejo, da bi se uporabljale v operacijah, kjer so vključena električna orodja, ker je vnetljiva in lahko eksplodira v kombinaciji z zrakom. Dietileter je široko razširjen v kirurgiji, kjer se uporablja za inhalacijsko anestezijo. V zobozdravstvu jih zdravimo z zobnimi koreninskimi kanali in karioznimi mesti, s čimer pripravimo ustno votlino za polnjenje. 
Dietileter kot gorivo
Snov ima visoko cetansko število (85-96), tako da se lahko uporablja kot izhodna tekočina za bencinske in dizelske motorje. Zaradi velike variabilnosti in nizkih plamenišč se kot sestavina gorivne mešanice za vzorčne dizelske motorje uporablja dietil eter. Izkazalo se je, da je ta snov podobna etanolu.
Pravilno shranjevanje
Dietil eter je priporočljivo shranjevati v steklenicah temne barve (skrbno zaprte) na hladnem, ker se razpade na svetlobi, v vročini in pod vplivom vlage, kar povzroči strupene snovi.