Sestava in struktura atomskega jedra (na kratko)
Davno pred pojavom zanesljivih podatkov o notranji strukturi vsega, kar obstaja, grški misleci so zamislili materijo v obliki najmanjših ognjevitih delcev, ki so bili v stalnem gibanju. Verjetno je ta vizija svetovnega reda stvari izpeljana iz povsem logičnih zaključkov. Kljub nekateri naivnosti in popolni neutemeljenosti te izjave se je izkazalo, da je res. Čeprav so znanstveniki lahko potrdili pogumno ugibanje šele triindvajset stoletij kasneje.
Atomska struktura
Ob koncu 19. stoletja so raziskovali lastnosti odvodne cevi, skozi katero je potekal tok. Opazovanja so pokazala, da se v tem primeru oddajajo dva toka delcev:
- Katodni žarki, ki se tvorijo v bližini elektrod, priključenih na negativni konec baterije. Katodni žarki so šli skozi cev in so lahko zdrsnili skozi luknjo v pozitivni elektrodi, kot tok nabitih delcev. Ugotovitve so pokazale, da je razmerje naboja takega delca na njegovo maso vedno enako in ni odvisno od vrste plina.
- Pozitivni žarki. Drugi tok delcev gre v nasprotno smer in lahko preide v luknjo na negativni elektrodi. Odstopanja na poljih dokazujejo, da imajo visoke hitrosti in različne vrednosti razmerja med nabojem in maso.
Negativni delci katodnih žarkov so bili imenovani elektroni. Nato so v mnogih procesih našli delce z enakim razmerjem med nabojem in maso. Zdi se, da so elektroni univerzalni sestavni deli različnih atomov, ki se zlahka ločijo pri bombardiranju ionov in atomov.
Zdi se, da so delci, ki nosijo pozitivni naboj, fragmenti atomov po izgubi enega ali več elektronov. Dejstvo je, da so bili pozitivni žarki skupine atomov brez negativnih delcev in posledično pozitivnega naboja.
Thompsonov model
Na podlagi poskusov je bilo ugotovljeno, da so pozitivni in negativni delci predstavljali bistvo atoma, njegove komponente. Angleški znanstvenik J. Thomson je predlagal svojo teorijo. Po njegovem mnenju je bila struktura atoma in atomskega jedra nekakšna masa, v kateri so bili negativni naboji stisnjeni v pozitivno nabito kroglo, kot so rozine v torti. Kompenzacija naboja je povzročila, da je »cupcake« električno nevtralen. 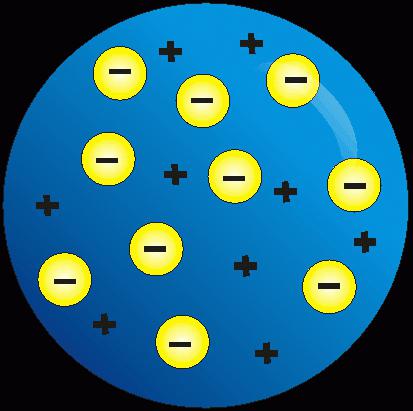
Rutherfordov model
Mladi ameriški znanstvenik Rutherford, ki je analiziral sledi po alfa delcih, je prišel do zaključka, da je Thompsonov model nepopoln. Nekateri alfa delci so bili upognjeni pri majhnih kotih - 5-10 o . V redkih primerih so alfa delci odstopali z velikimi koti 60-80 o , v izjemnih primerih pa so bili koti zelo veliki - 120-150 o . Thompsonov model atoma ne more pojasniti take razlike.
Rutherford predlaga nov model, ki pojasnjuje strukturo atoma in atomsko jedro. Fizika procesov trdi, da mora biti atom 99% prazen, okoli katerega se vrtijo majhno jedro in elektroni, ki se gibljejo po orbiti. 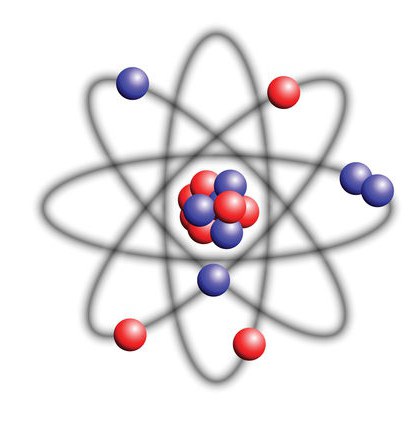
Odstopanja v udarcih, razlaga dejstvo, da imajo delci atoma svoje električni naboji. Pod vplivom bombardiranja nabitih delcev se atomski elementi obnašajo kot navadna nabita telesa v makrokozmosu: delci z enakimi naboji se odbijajo in se z nasprotnimi naboji medsebojno privlačijo.
Stanje atomov
V začetku prejšnjega stoletja, ko so začeli s prvimi pospeševalniki elementarnih delcev, so vse teorije, ki so razložile strukturo atomskega jedra in sam atom, čakale na eksperimentalno preverjanje. Do takrat so bile interakcije alfa in beta žarkov z atomi že temeljito preučene. Do leta 1917 so mislili, da so atomi stabilni ali radioaktivni. Stabilnih atomov ni mogoče razdeliti, razpada radioaktivnih jeder ni mogoče nadzorovati. Toda Rutherford je uspel ovreči to mnenje.
Prvi proton
Leta 1911 je E. Rutherford predstavil idejo, da so vsa jedra sestavljena iz enakih elementov, katerih osnova je atom vodika. Na tej ideji je znanstvenik podal pomemben zaključek iz prejšnjih študij o strukturi snovi: mase vseh kemijskih elementov so brez preostanka razdeljene na maso vodika. Nova predpostavka je odprla nove priložnosti, ki omogočajo nov pogled na strukturo atomskega jedra. Jedrske reakcije morajo potrditi ali ovreči novo hipotezo.
Poskusi so bili izvedeni leta 1919 z atomi dušika. Z bombardiranjem z alfa delci je Rutherford dosegel presenetljiv rezultat.
Atom N je absorbiral delce alfa, nato se je spremenil v kisikov atom O17 in izpustil jedro vodika. To je bila prva umetna transformacija atoma enega elementa v drugega. Takšna izkušnja je vzbudila upanje, da struktura atomskega jedra, fizika obstoječih procesov omogoča druge jedrske transformacije.

Znanstvenik je v svojih poskusih uporabil metodo utripanja. Iz pogostosti izbruha je naredil sklepe o sestavi in strukturi atomskega jedra, o značilnostih proizvedenih delcev, o njihovi atomski masi in zaporedni številki. Neznan delec se je imenoval Rutherfordov proton. Imel je vse lastnosti vodikovega atoma, brez svojega edinega elektrona - posameznega pozitivnega naboja in ustrezne mase. Tako je bilo dokazano, da sta proton in jedro vodika isti delci.
Leta 1930, ko so bili zgrajeni in zagnani prvi veliki pospeševalniki, je bil testiran in dokazan Rutherfordov atomski model: vsak atom vodika je sestavljen iz enega samega elektrona, katerega položaj ni mogoče določiti, in prostega atoma z enim samim pozitivnim protonom. Ker protoni, elektroni in alfa delci lahko letijo iz atoma, ko so bombardirani, so znanstveniki mislili, da so komponente kateregakoli atomskega jedra. Toda tak model atomskega jedra se je zdel nestabilen - elektroni so bili preveliki, da bi se ujemali z jedrom, poleg tega pa so obstajale resne težave, povezane s kršitvijo zakona gibanja in ohranjanja energije. Ta dva zakona, kot stroga računovodja, sta dejala, da količina gibanja in masa med bombardiranjem izgine v neznani smeri. Ker so bili ti zakoni splošno sprejeti, je bilo treba poiskati pojasnila za takšno uhajanje.
Nevtroni
Znanstveniki po vsem svetu so postavili eksperimente za odkrivanje novih sestavin atomskih jeder. V tridesetih letih so nemški fiziki Becker in Bothe bombardirali atome berilija z alfa delci. V tem primeru je bilo zabeleženo neznano sevanje, za katerega je bilo odločeno, da se imenuje G-žarki. Podrobne študije so opisale nekatere značilnosti novih žarkov: lahko so se širile strogo v ravni liniji, niso bile v interakciji z električnimi in magnetnimi polji in so imele visoko prodorno moč. Kasneje so delci, ki tvorijo to vrsto sevanja, našli v interakciji alfa delcev z drugimi elementi - borom, kromom in drugimi.
Chadwickova hipoteza
Potem je James Chadwick, sodelavec in študent Rutherforda, v reviji Nature podal kratko sporočilo, ki je kasneje postalo dobro znano. Chadwick je opozoril na dejstvo, da so protislovja v ohranjevalnih zakonih zlahka rešena, ob predpostavki, da je novo sevanje tok nevtralnih delcev, od katerih ima vsaka maso približno enako masi protona. Ob upoštevanju te predpostavke so fiziki bistveno dopolnili hipotezo, ki pojasnjuje strukturo atomskega jedra. Na kratko, bistvo dodatkov je bilo reducirano na nov delec in njegovo vlogo v strukturi atoma. 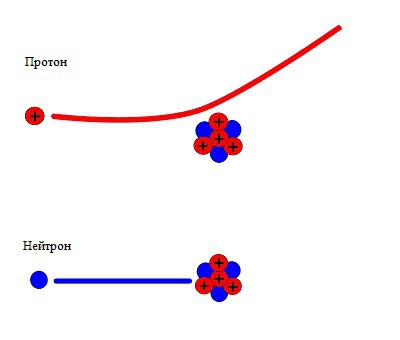
Nevtronske lastnosti
Zaznani delci so dobili ime "nevtron". Na novo odkriti delci niso tvorili elektromagnetnih polj okoli sebe, z lahkoto so prešli skozi snov brez izgube energije. V redkih trkih z lahkimi atomi atomov lahko nevtron iz jedra izloči jedro, izgubi pomemben del svoje energije. Struktura atomskega jedra je predvidevala prisotnost različnega števila nevtronov v vsaki snovi. Atomi z enakim jedrskim nabojem, vendar z različnim številom nevtronov, se imenujejo izotopi.
Nevtroni so služili kot odličen nadomestek za alfa delce. Trenutno se uporabljajo za proučevanje strukture atomskega jedra. Na kratko, njihov pomen za znanost ni mogoče opisati, toda fiziki so prav zaradi nevtronskega bombardiranja atomskih jeder lahko pridobili izotope skoraj vseh znanih elementov.
Sestava jedra atoma
Trenutno je struktura atomskega jedra kombinacija protonov in nevtronov, ki jih držijo jedrske sile. Na primer, jedro helija je snop dveh nevtronov in dveh protonov. Svetlobni elementi imajo skoraj enako število protonov in nevtronov, težji elementi pa imajo veliko več nevtronov. 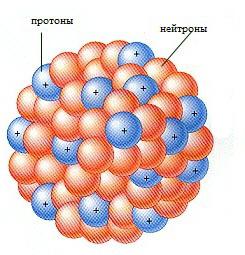 To sliko strukture jedra potrjujejo eksperimenti na modernih velikih pospeševalnikih s hitrimi protoni. Električne sile odganjanja protona so uravnotežene z jedrskimi silami, ki delujejo samo v jedru samega. Čeprav narava jedrske sile ki še niso popolnoma razumeli, je njihov obstoj skoraj dokazan in v celoti pojasnjuje strukturo atomskega jedra.
To sliko strukture jedra potrjujejo eksperimenti na modernih velikih pospeševalnikih s hitrimi protoni. Električne sile odganjanja protona so uravnotežene z jedrskimi silami, ki delujejo samo v jedru samega. Čeprav narava jedrske sile ki še niso popolnoma razumeli, je njihov obstoj skoraj dokazan in v celoti pojasnjuje strukturo atomskega jedra.
Razmerje med maso in energijo
Leta 1932 je Wilsonova kamera posnela neverjetno fotografijo, ki dokazuje obstoj pozitivno nabitih delcev masa elektronov. Pred tem je P. Dirac teoretično napovedal pozitivne elektrone. Prav tako je bil v kozmičnem sevanju zaznan pozitiven elektron. Nov kos se je imenoval pozitron. Pri trku s svojim dvojčkom - elektronom, pride do anihilacije - medsebojnega uničenja dveh delcev. To sprosti določeno količino energije.
Pred tem je P. Dirac teoretično napovedal pozitivne elektrone. Prav tako je bil v kozmičnem sevanju zaznan pozitiven elektron. Nov kos se je imenoval pozitron. Pri trku s svojim dvojčkom - elektronom, pride do anihilacije - medsebojnega uničenja dveh delcev. To sprosti določeno količino energije.
Tako je teorija razvita za makro-svet popolnoma primerna za opisovanje obnašanja najmanjših elementov snovi.