Kemijske lastnosti monohidričnih in polihidričnih alkoholov
Alkoholi so velika skupina organskih kemikalij. Vključuje podrazrede enobarvnih in polihidričnih alkoholov ter vse sestavine kombinirane strukture: aldehidni alkoholi, derivati fenola, biološke molekule. Te snovi vstopajo v številne vrste reakcij tako na hidroksilno skupino kot na ogljikov atom, ki ga nosi. Te kemijske lastnosti alkoholov je treba podrobno preučiti.

Vrste alkoholov
Snovi alkoholov vsebujejo hidroksilno skupino, vezano na nosilni ogljikov atom. Odvisno od števila atomov ogljika, s katerimi je povezan nosilec C, se alkoholi delijo na:
- primarno (povezano s terminalnim ogljikom);
- sekundarne (povezane z eno hidroksilno skupino, enim vodikom in dvema ogljikovima atomoma);
- terciarni (vezan na tri ogljikove atome in eno hidroksilno skupino);
- mešani (polihidrični alkoholi, v katerih obstajajo hidroksilne skupine v sekundarnih, primarnih ali terciarnih ogljikovih atomih).
Tudi alkoholi so razdeljeni glede na količino hidroksilnih radikalov na enomaterialni in poliatomski. Prvi vsebuje le eno hidroksilno skupino na atomu, ki nosi ogljik, na primer etanol. Polihidrični alkoholi vsebujejo dve ali več hidroksilnih skupin različnih nosilnih ogljikovih atomov.
Kemijske lastnosti alkoholov: tabela
Najbolj priročno je, da nam posredujete zanimivo gradivo preko tabele, ki odraža splošna načela reaktivnosti alkoholov.
Reakcijska vez, reakcijski tip | Reagent | Izdelek |
OH komunikacija, zamenjava | Aktivna kovina, aktivni kovinski hidrid, alkalija ali amid aktivnih kovin | Alkoholni |
C-O in O-H vez, medmolekularna dehidracija | Alkohol pri segrevanju v kislem okolju | Preprost zrak |
C-O in O-H vez, intramolekularna dehidracija | Alkohol pri segrevanju nad koncentrirano žveplovo kislino | Nenasičeni ogljikovodiki |
Povezava CO, substitucija | Vodikov halid, tionilklorid, kvazifosfonijeva sol, fosforjevi halidi | Haloalkani |
C-O vez - oksidacija | Donorji kisika (kalijev permanganat) s primarnim alkoholom | Aldehid |
C-O vez - oksidacija | Donorji kisika (kalijev permanganat) s sekundarnim alkoholom | Keton |
Alkoholna molekula | Kisik (gorenje) | Ogljikov dioksid in voda. |
Reaktivnost alkoholov
Zaradi prisotnosti v molekuli enodolnega alkohola radikal ogljikovodikov - C-O vezi in OH vezi - ta razred spojin vstopa v številne kemijske reakcije. Določajo kemijske lastnosti alkoholov in so odvisne od reaktivnosti snovi. Slednje je odvisno od dolžine ogljikovodikovih radikalov, ki so vezani na nosilni ogljikov atom. Večja kot je, manjša je polarnost O-H vezi, zaradi česar se bodo reakcije, ki potekajo z izločanjem vodika iz alkohola, nadaljevati počasneje. To prav tako zmanjšuje disociacijsko konstanto snovi.
Ad
Kemijske lastnosti alkoholov so odvisne tudi od števila hidroksilnih skupin. Ena od gostote elektronov se premakne proti sebi vzdolž sigma vezi, kar poveča reaktivnost v OH skupini. Ker ta polarizira C-O vez, so reakcije z razpokom bolj aktivne v alkoholih, ki imajo dve ali več OH skupin. Zato je bolj verjetno, da bodo reagirali polihidrični alkoholi, katerih kemijske lastnosti so številnejše. Vsebujejo tudi več skupin alkohola, zaradi katerih se lahko vsak od njih svobodno odzovejo.
Tipične reakcije monohidričnih in polihidričnih alkoholov
Značilne kemijske lastnosti alkoholov se kažejo samo v reakciji z aktivnimi kovinami, njihovimi bazami in hidridi, Lewisovimi kislinami. Značilne so tudi interakcije z vodikovimi halidi, fosforjevimi halidi in drugimi sestavinami za proizvodnjo haloalkanov. Alkoholi so tudi šibke baze, zato reagirajo s kislinami in tako tvorijo vodikove halide in estre anorganskih kislin.
Ad
Eterji pri medmolekularni dehidraciji tvorijo alkoholi. Iste snovi vstopajo v dehidrogenacijske reakcije z nastajanjem aldehidov iz primarnega alkohola in ketonov iz sekundarnega. Terciarni alkoholi ne vstopajo v takšne reakcije. Tudi kemijske lastnosti etilni alkohol (in drugi alkoholi) dopušča možnost njihove popolne oksidacije s kisikom. To je preprosta reakcija zgorevanja, ki jo spremlja izpust vode ogljikov dioksid in nekaj toplote.

Reakcije na vodikov atom OH vezi
Kemične lastnosti monohidričnih alkoholov omogočajo razpok OH vezi in izločanje vodika. Te reakcije se pojavijo pri interakciji z aktivnimi kovinami in njihovimi bazami (alkalijami), s hidridi aktivnih kovin, kot tudi z Lewisovimi kislinami.
Ad
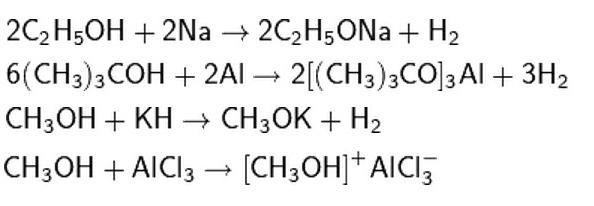
Tudi alkoholi aktivno reagirajo s standardnimi organskimi in anorganskimi kislinami. V tem primeru je reakcijski produkt ester ali halougljikovodik.
Reakcija sinteze halogen-alkanov (s C-O vezjo)
Haloalkani so značilne spojine, ki jih lahko dobimo iz alkoholov med več vrstami kemijskih reakcij. Predvsem kemijske lastnosti monohidričnih alkoholov omogočajo interakcijo z vodikovimi halogenidi, tri- in pentavalentnimi fosforjevimi halidi, kvazifosfonijeve soli in tionil kloridom. Halogen-alkani iz alkoholov lahko dobimo tudi z vmesnim načinom, to je s sintezo alkil sulfonata, ki bo kasneje vstopil v substitucijsko reakcijo.
Ad
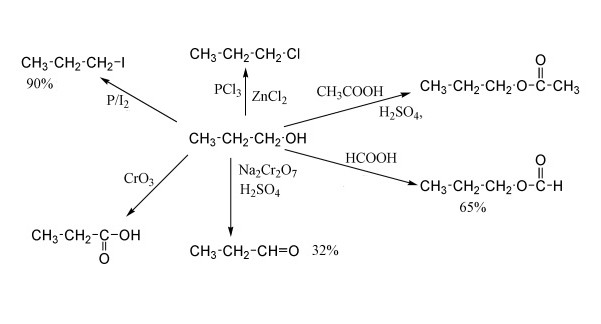
Primer prve reakcije z vodikovim halidom je naveden na zgornji grafični aplikaciji. V tem primeru butil alkohol reagira s klorovodikom, da nastane klorbutan. Na splošno se razred spojin, ki vsebujejo klor in nasičene ogljikovodikove radikale, imenuje alkil klorid. Stranski produkt kemijske interakcije je voda.
Reakcije s pridobivanjem alkil klorida (jodid, bromid ali fluorid) so precej številne. Tipičen primer je interakcija s fosforjevim tribromidom, fosforjevim pentakloridom in drugimi spojinami tega elementa in njegovimi halidi, perkloridi in perfluoridi. Tečejo po mehanizmu nukleofilne substitucije. Alkoholi prav tako reagirajo s tionil kloridom, da tvorijo kloralkan in sproščanje SO2.
Jasno je, da so kemijske lastnosti monohidričnih nasičenih alkoholov, ki vsebujejo nasičen ogljikovodični radikal, predstavljene kot reakcije v spodnji ilustraciji.
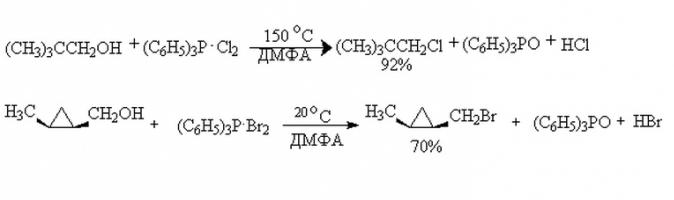
Alkoholi z lahkoto delujejo s kvazifosfonijevo soljo. Vendar pa je ta reakcija najbolj ugodna med potekom monomatskih sekundarnih in terciarnih alkoholov. So regioselektivni, omogočajo "vsaditev" halogenske skupine na strogo določen kraj. Produkte teh reakcij dobimo z visokim masnim deležem donosa. In polihidrični alkoholi, katerih kemijske lastnosti so nekoliko drugačne od tistih, ki so enaki monohidričnih, se lahko med reakcijo izomerizirajo. Zato je pridobivanje ciljnega izdelka težko. Primer reakcije na sliki.
Ad
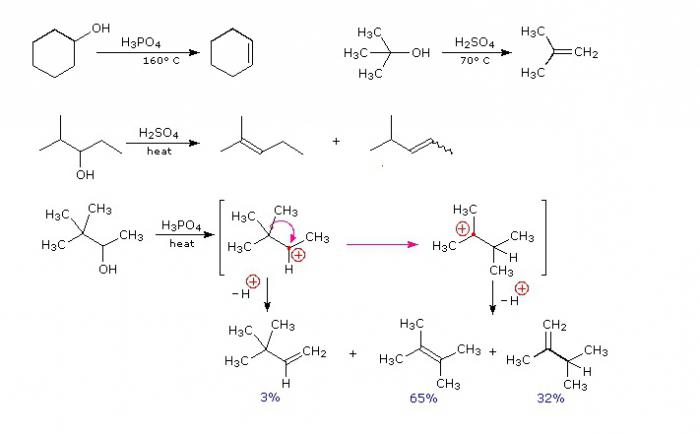
Intramolekularna in medmolekularna dehidracija alkoholov
Hidroksilna skupina, ki se nahaja na atomu, ki nosi ogljik, se lahko odcepi z uporabo močnih akceptorjev. Tako potekajo intermolekularne dehidracijske reakcije. Pri interakciji ene molekule alkohola z drugo v raztopini koncentriranega žveplove kisline vodna molekula je odcepljena iz obeh hidroksilnih skupin, katerih radikali se združijo in tvorijo etrsko molekulo. Pri medmolekularni dehidraciji etanala lahko dobimo dioksan - produkt dehidracije v štirih hidroksilnih skupinah.
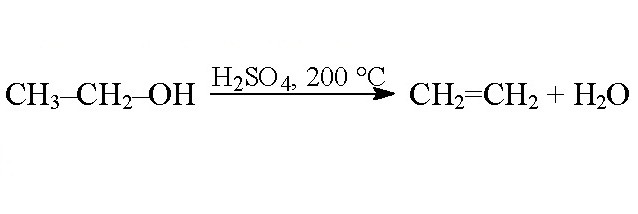
Za intramolekularno dehidracijo je izdelek alken.