Kemijske lastnosti karboksilnih kislin in metode pridobivanja
Kemijske spojine, ki so sestavljene predvsem iz karboksilne skupine COOH, so dobile ime karboksilne kisline znanstvenikov. Obstaja veliko število imen teh spojin. Razvrščamo jih glede na različne parametre, na primer število funkcionalnih skupin, prisotnost aromatskega obroča itd.
Struktura karboksilnih kislin
Kot že omenjeno, da je kislina karboksilna, mora imeti karboksilno skupino, ki ima dva funkcionalna dela: hidroksil in karbonil. Njihovo interakcijo zagotavlja funkcionalna kombinacija enega ogljikovega atoma z dvema kisikoma. Kemijske lastnosti karboksilnih kislin so odvisne od strukture te skupine.
Ad
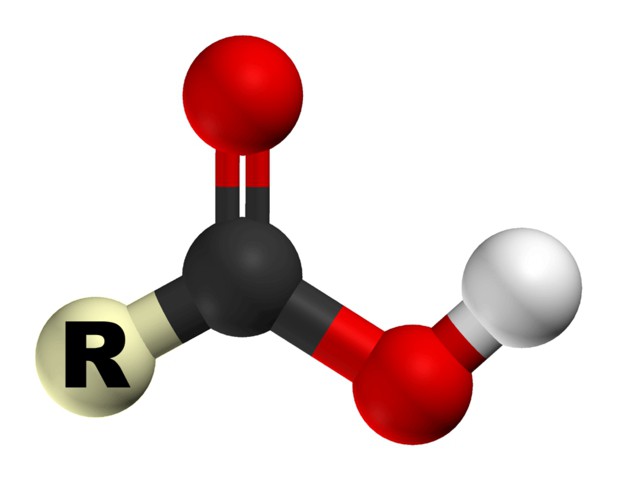
Zaradi karboksilne skupine so te organske spojine lahko imenujemo kisline. Njihove lastnosti so posledica povečane sposobnosti H + iona, da ga pritegne kisik, kar dodatno polarizira OH vez. Tudi zaradi te lastnosti lahko organske kisline disociirajo v vodnih raztopinah. Sposobnost raztapljanja se zmanjša obratno s povečanjem molekulske mase kisline.
Vrste karboksilnih kislin
Kemiki izločajo več skupin organskih kislin.
Razvrstitev karboksilne kisline | |
Po številu funkcionalnih skupin | Monokarbon |
Dikarbonat | |
Polikarbonat | |
Po naravi radikalen | Alifatski |
Aromatično | |
Ciklični | |
Glede na stopnjo nasičenosti radikala | Nenasičena |
Nasičene | |
S prisotnostjo funkcionalnih skupin v radikalu, to je s substitucijo enega vodikovega atoma | Halogen (Cl 2 , F 2 , Br 2 , I 2 ) |
Oxogroup (COH) | |
Hidroksi (OH) | |
Amino skupina (NH 2) | |
Monobazične karboksilne kisline so sestavljene iz ogljikovega ogrodja in samo ene funkcionalne karboksilne skupine. Vsak študent pozna kemijske lastnosti karboksilnih kislin. Kurikulum 10. stopnje iz kemije vključuje neposredno proučevanje lastnosti monobaznih kislin. Dibazične in polibazične kisline imajo v svoji strukturi dve ali več karboksilnih skupin.
Ad
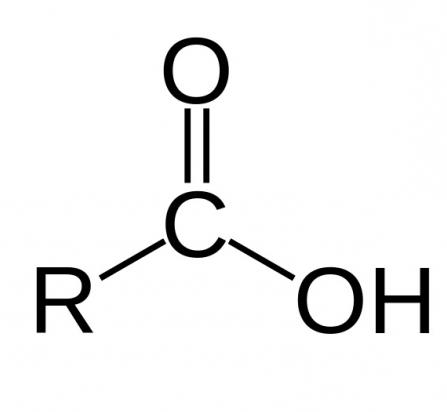
Tudi zaradi prisotnosti ali odsotnosti dvojnih in trojnih vezi v molekuli obstajajo nenasičene in nasičene karboksilne kisline. Kemijske lastnosti in njihove razlike bodo obravnavane spodaj.
Če ima organska kislina v radikalu substituiran atom, potem njeno ime vključuje ime skupine substituenta. Torej, če je vodikov atom nadomeščen s halogenom, potem bo ime kisline vsebovalo ime halogena. Iste spremembe bodo podvržene imenu, če obstaja zamenjava z aldehidnimi, hidroksilnimi ali amino skupinami.
Izomerizem organskih karboksilnih kislin
Skoraj vsi organske snovi imajo sposobnost izomerizacije. Karboksilne kisline niso izjema. Razlikujemo naslednje vrste izomerizma:
- Ogljikov skelet.
- Interklasna izomerija.
- Prostorska izomerija;
Sposobnost izomerizacije neposredno vpliva na kemijske lastnosti karboksilnih kislin.
Izomerizem okostja je možen za kisline, katerih ogljikovodiki vsebujejo vsaj štiri atome ogljika. Interklasa pa je možna za kisline z dvema ogljikovima atomoma v radikalu. Samo karboksilne kisline z enotnimi vezmi v okostju so sposobne prostora.
Ad
Seznam in bistvene karboksilne kisline
Imena in formule znanih karboksilnih kislin | ||
Sistematično ime kisline | Trivialno ime | Formula karboksilne kisline |
Metanojska kislina | Ant | HCOOH |
Etanojska kislina | Acetic | CH2COOH |
Propanojska kislina | Propionski | CH3CH2COOH |
Butanska kislina | Mastna | CH3CH2CH2COOH |
Pentanojska kislina | Valerian | CH3CH2CH2CH2COOH |
Pentenska kislina | Akril | CH2 = CH-COOH |
Benzen karboksilna kislina | Benzoin | C6H5COOH |
Heksadekan | Palmitic | C15H31COOH |
Oksodekan | Stearic | C17H35COOH |
Ethandium | Sorrel | HOOC-COOH |
Propandia | Malonovaya | HOOC-CH2-COOH |
Butandiova | Amber | HOOC-CH2-CH2-COOH |
Benzen dikarboksil | Ftalni | HOOC-C6H5-COOH |
2-hidroksi-propanojske kisline | Mlečni | CH3CHOHCOOH |
Hidroksibutandiojska kislina | Apple | HOOC-CH2CHOH-COOH |
2,3-dihidroksibutandiojske kisline | Vinska klet | HOOC-OHCH-OHCH-COOH |
3-karboksi-3-hidroksipentanid | Lemon | HOOC-CH2-CHOH-COOH-CH2COOH |
2-oksopropanojske kisline | Pyruvic | CH3 COCOOH |
2-hidroksibenzojska kislina | Salicilna | C6H5OHCOOH |
Karboksilne kisline: kemijske lastnosti
Za podrobnejše razumevanje bistva karboksilnih kislin upoštevajte njihove lastnosti. V šolskem kurikulumu se monobazne karboksilne kisline obravnavajo v velikem obsegu, katerih kemijske lastnosti se kažejo v reakcijah med vodikovimi halidi, vodo in drugimi snovmi. Vse te vrste kislin:
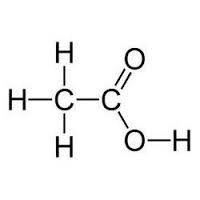
- Raztopimo v raztopini na vodikove ione in radikal s karboksilom. S tem mravljične kisline se nanaša na elektrolite srednje moči in ocetno šibko, to je moč disociacije se zmanjšuje navzdol po homolognih serijah.
- Obarvajte lakmusov test v rdeči barvi.
- Izvedite tok električne energije.
- Reagira s halogeni: 2RCOOH + Cl2 = 2RCOOCl + 2HCL.
- Preidejo v reakcijo esterifikacije z alkoholi: R-COOH + R'OH = RCOOR '+ H2O.
- Interakcija z nekaterimi kovinami: RCOOH + Mg = RCOOMg + H2.
- Reagirajte z osnovne okside vrsta in hidroksidi, ki tvorijo soli: RCOOH + NaOH = RCOONa + H2O.
- Reakcija s solmi: RCOOH + Na2CO3 = RCOONa + H2O + CO2.
Takšne lastnosti monobaznih kislin so razložene s spremembo karboksilne skupine, od hidroksila, pri katerem se elektroni premaknejo do najbližjega ogljikovega atoma, in delno pogasijo njegov pozitivni naboj. Poleg tega imajo karboksilne kisline, katerih kemijske lastnosti so opisane zgoraj, dvosmerno interakcijo med atomi.
Ad
Kemijske lastnosti drugih monobaznih kislin
Iz klasifikacije je znano, da so prisotne tudi monobazične nenasičene karboksilne kisline, katerih kemijske lastnosti se razlikujejo od lastnosti mejne vrednosti.
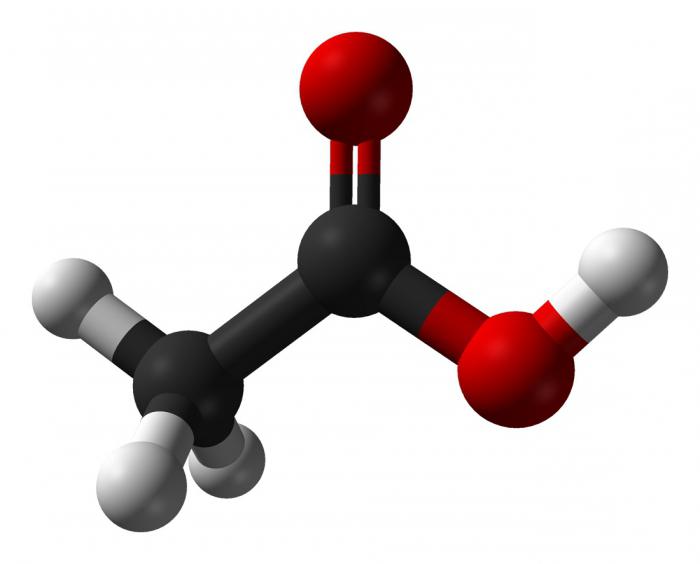
Dvo-vezne kisline v ogljikovodičnem radikalu so torej monobazične nenasičene karboksilne kisline. Kemijske lastnosti teh kislin so izražene v reakcijah:
- Z vodikovim halidom, vendar veliko počasnejši od mejnih in v nasprotju z Markovnikovim pravilom, ker karboksilna skupina zmanjšuje elektronsko gostoto dvojne vezi: R = CH-COOH + HCl = RCl-CH2-COOH.
- S halogeni: Br2 + R = CH-COOH = RBr-CHBr-COOH.
- Z vodikom, ki povzroči prekinitev dvojne vezi: H2 + R = CH-COOH = COOH-R-CH.
- Previdna oksidacija, zaradi katere nastanejo hidroksi kisline: R = CH-COOH + H2O [O] R (OH) -CH (OH) COOH.
- Radikalna oksidacija, ki se pojavi z razpokom kislinske molekule (npr. Propenske kisline): CH3-CH = C-COOH + H20 [O] CH3COOH + HOOC-COOH.
- Polimerizacija: n COOH- (CH = CH) -R = n (-COOH-CH-CH-R-)
Kemijske lastnosti bikarboksilnih kislin
Dikarboksilne organske kisline so dvobazne karboksilne kisline. Kemijske lastnosti teh kislin se razlikujejo od lastnosti monokarboksilnih kislin. To je posledica dejstva, da je jakost dvobaznih kislin večja od jakosti monobazične zaradi vpliva druge skupine karboksila in hidroksila. Poleg tega se ta učinek zmanjša z razdaljo od verige ogljikovih atomov.
Ad
Dibazične kisline imajo naslednje lastnosti:
- Dekarboksilacija kisline (npr. Etandin): HOOC-COOH (t) = HOOC + CO2. Pomembno je vedeti, da se oksalna in malonska kislina dekarboksilirajo veliko lažje kot druge.
- Nastajanje kislih in srednje soli: HOOC-RR-COOK ali HOOK-RR-COOK.
- Oblikovanje popolnih in nepopolnih etrov.
- Malonska kislina lahko vstopi v substitucijske reakcije: vodik iz skupine CH2 ogljikovodikovih radikalov se zlahka nadomesti z atomi kovin.
Soli, ki jih tvorijo karboksilne kisline
Soli so organske spojine, ki nastanejo zaradi zamenjave vodikovega atoma in hidroksilne skupine karboksilne kisline karboksilne kisline s kovino. To pomeni, da lahko organske kisline v reakcijah z bazami ali anorganskimi solmi tvorijo soli karboksilnih kislin. Kemične lastnosti, s katerimi se pridobivajo organske spojine, kot so soli, se uporabljajo v gospodinjstvu za proizvodnjo mila.
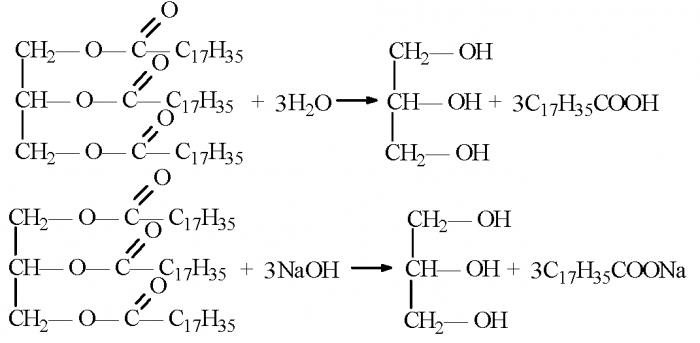
Stearinska (oktadekanska) in palmitinska (heksadekanska) kislina sta najprimernejši za sintezo trdnih in tekočih mil. Oleic (cis-9-oktadecen) ali miristik (tetradekan kisline).
Osnova mila je reakcija sinteze estrov zgoraj navedenih kislin s kalijevo ali natrijevo soljo.
Metode za proizvodnjo karboksilnih kislin
Obstajajo številne metode in metode za proizvodnjo kislin s skupino COOH, najpogosteje pa se uporabljajo:
- Ekstrakcija iz naravnih snovi (maščob in drugih stvari).
- Oksidacija monoalkoholov ali spojin s COH-skupino (aldehidi): ROH (RCOH) [O] R-COOH.
- Hidroliza trihaloalkanov v alkali z vmesno produkcijo mono-alkohola: RCl3 + NaOH = (ROH + 3NaCl) = RCOOH + H2O.
- Saponifikacija ali hidroliza estrov kisline in alkohola (estrov): R-COOR '+ NaOH = (R-COONa + R'OH) = R-COOH + NaCl.
- Oksidacija alkanov s permanganatom (trda oksidacija): R = CH2 [O], (KMnO4) RCOOH.
Vrednost karboksilnih kislin za ljudi in industrijo

Kemijske lastnosti karboksilnih kislin so zelo pomembne za človeško življenje. So izredno potrebne za telo, kot v velikih količinah, ki jih vsebuje vsaka celica. Presnova maščob, beljakovin in ogljikovih hidratov vedno poteka skozi stopnjo, pri kateri dobimo eno ali drugo karboksilno kislino.
Poleg tega se pri ustvarjanju zdravil uporabljajo karboksilne kisline. Nobena farmacevtska industrija ne more obstajati brez praktične uporabe lastnosti organskih kislin.

Pomembno vlogo imajo spojine s karboksilno skupino v kozmetični industriji. Sinteza maščobe za kasnejšo proizvodnjo mila, detergentov in gospodinjskih kemikalij temelji na reakciji esterifikacije s karboksilno kislino.
Kemijske lastnosti karboksilnih kislin se odražajo v človeškem življenju. So zelo pomembne za človeško telo, saj so v vsaki celici velike številke. Presnova maščob, beljakovin in ogljikovih hidratov vedno poteka skozi stopnjo, pri kateri dobimo eno ali drugo karboksilno kislino.