Boltzmannova konstanta: pomen in fizični pomen
Fizika kot natančna kvantitativna znanost ne more storiti brez niza zelo pomembnih konstant, ki so vključene kot univerzalni koeficienti v enačbah, ki vzpostavljajo povezavo med temi ali drugimi količinami. To so temeljne konstante, zaradi katerih taki odnosi pridobijo invarianco in so sposobni razložiti obnašanje fizičnih sistemov na drugačni lestvici.
Med temi parametri, ki so značilni za lastnosti v našem vesolju, je Boltzmannova konstanta, količina, ki je vključena v več najpomembnejših enačb. Vendar, preden se obrnemo na upoštevanje njenih značilnosti in pomenov, je nemogoče reči nekaj besed o znanstveniku, čigar ime nosi.
Ludwig Boltzmann: znanstvena vrednost
Eden največjih znanstvenikov XIX. Stoletja, avstrijski Ludwig Boltzmann (1844–1906) je pomembno prispeval k razvoju molekularne kinetične teorije in postal eden od ustanoviteljev statistične mehanike. Bil je avtor ergodične hipoteze, statistične metode v opisu idealnega plina, osnovne enačbe fizikalne kinetike. Veliko je delal na temah termodinamike (H-Boltzmannov teorem, statistično načelo za drugi zakon termodinamike), teorija sevanja (Stefan-Boltzmannov zakon). V svojih delih se je dotaknil tudi nekaterih vprašanj elektrodinamike, optike in drugih vej fizike. Njegovo ime je imortalizirano v dveh fizikalnih konstantah, o katerih bomo govorili spodaj.
Ad
Ludwig Boltzmann je bil zanesljiv in dosleden zagovornik teorije atomsko-molekularne strukture snovi. Z leti je bil prisiljen boriti se s pomanjkanjem razumevanja in zavračanja teh idej v znanstveni skupnosti časa, ko so mnogi fiziki atome in molekule obravnavali kot nepotrebno abstrakcijo, v najboljšem primeru kot pogojno napravo za udobje izračunov. Boleča bolezen in napadi konzervativno mislečih kolegov so v Boltzmannu povzročili hudo depresijo, ki ni mogla nositi izjemnega znanstvenika, ki je storil samomor. Na grobnem spomeniku, nad Boltzmannovim doprsjem, kot znak priznanja njegovih zaslug, je izločena enačba S = k ∙ logW - eden od rezultatov njegove plodne znanstvene dejavnosti. Konstanta k v tej enačbi je Boltzmannova konstanta.
Ad

Energija in temperatura molekule
Koncept temperature služi za označevanje stopnje toplote telesa. V fiziki se uporablja absolutna temperaturna lestvica, ki temelji na zaključku molekularne kinetične teorije temperature kot mere, ki odraža energijo toplotnega gibanja delcev snovi (kar pomeni seveda povprečno kinetično energijo množice delcev).
Tako Joule, ki je bil sprejet v sistemu SI, kot tudi erg, uporabljen v GHS sistemu, sta preveliki enoti za izražanje energije molekul, prav tako je bilo zelo težko izmeriti temperaturo na ta način. Primerna temperaturna enota je stopnja, merjenje pa se izvaja posredno, z registracijo spreminjajočih se makroskopskih lastnosti snovi - na primer, volumna.

Kako energijo in temperaturo
Za izračun stanja realne snovi pri temperaturah in tlakih blizu normale se uspešno uporablja model idealnega plina, to je molekula, katere velikost je veliko manjša od volumna, ki ga zaseda določena količina plina, razdalja med delci pa znatno presega polmer njihove interakcije. Na osnovi enačb kinetične teorije je povprečna energija takih delcev definirana kot E cf = 3/2, kT, kjer je E kinetična energija, T je temperatura in 3/2 is k koeficient sorazmernosti, ki ga je uvedel Boltzmann. Številka 3 tukaj označuje število stopenj svobode translacijskega gibanja molekul v treh prostorskih dimenzijah.
Količina, ki je bila kasneje poimenovana po avstrijskem fiziku kot Boltzmannova konstanta, kaže, kateri del joula ali erg vsebuje eno stopnjo. Z drugimi besedami, njegova vrednost določa, kako statistično povprečno v povprečju zvišuje energijo toplotnega kaotičnega gibanja posameznega delca monatomnega idealnega plina, ko se temperatura dvigne za 1 stopinjo.
Ad
Kolikokrat je stopnja manj kot joule
Številčno vrednost te konstante lahko dobimo na različne načine, na primer z merjenjem absolutne temperature in tlaka, z uporabo enačbe idealnega plina ali z uporabo Brownovega gibalnega modela. Teoretična izpeljava te količine na sedanji ravni znanja ni mogoča.
Boltzmannova konstanta je enaka 1.38 × 10 -23 J / K (tu je K Kelvin, stopnja absolutne temperaturne lestvice). Za skupino delcev v 1 molu idealnega plina (22,4 litra) dobimo koeficient, ki povezuje energijo s temperaturo (univerzalna plinska konstanta) z množenjem Boltzmannove konstante z Avogadrovim številom (število molekul v molu): R = kN A , in je 8,31 J / (mol vin Kelvin). Za razliko od slednje pa je Boltzmannova konstanta bolj univerzalna po naravi, saj vstopa tudi v druge pomembne odnose in služi tudi za opredelitev druge fizične konstante.
Ad
Statistična energijska porazdelitev molekul
Ker so stanja snovi makroskopskega reda rezultat obnašanja velikega števila delcev, so opisana s statističnimi metodami. Slednje vključuje ugotavljanje porazdelitve energijskih parametrov plinskih molekul:
- Maxwellova porazdelitev kinetičnih energij (in hitrosti). To kaže, da ima v plinu v ravnotežju večina molekul hitrosti blizu nekaj verjetne hitrosti v = √ (2kT / m 0 ), kjer je m 0 masa molekule.
- Boltzmannova porazdelitev potencialnih energij za pline, ki so v polju katere koli sile, kot je gravitacija Zemlje. Odvisno je od razmerja med dvema dejavnikoma: privlačnostjo do Zemlje in kaotičnim toplotnim gibanjem delcev plina. Posledično je nižja potencialna energija molekul (bližje površini planeta), višja je njihova koncentracija.
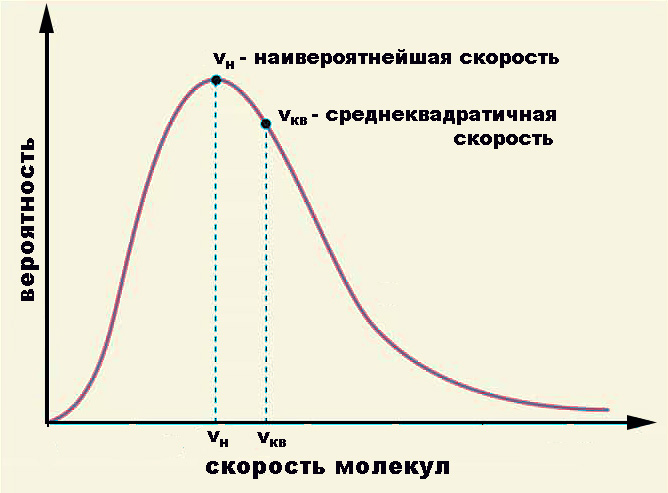
Obe statistični metodi sta združeni v Maxwell - Boltzmannovo porazdelitev, ki vsebuje eksponentni faktor e - E / kT , kjer je E vsota kinetičnih in potencialnih energij, in kT je povprečna energija toplotnega gibanja, ki nam je že znana in je kontrolirana z Boltzmannovo konstanto.
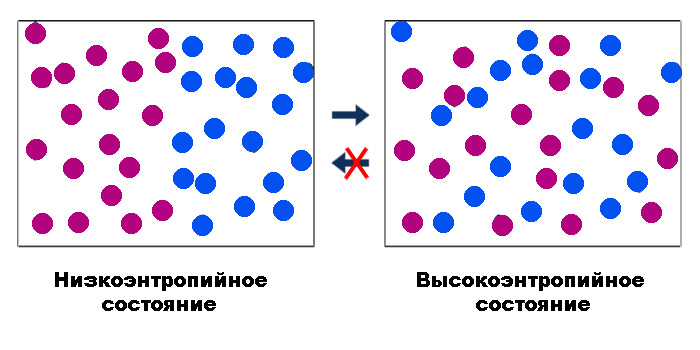
Stalna k in entropija
V splošnem lahko entropijo označimo kot merilo nepovratnosti termodinamičnega procesa. Ta nepovratnost je povezana s sipanjem - razpršitvijo energije. S statističnim pristopom, ki ga je predlagal Boltzmann, je entropija funkcija števila načinov, kako se lahko fizični sistem izvede brez spreminjanja njegovega stanja: S = k ∙ lnW.
Ad
Tu konstanta k postavi lestvico rasti entropije s povečanjem tega števila (W) variant sistema ali mikrostestov. Max Planck, ki je vodil to formulo v sodobno obliko, je predlagal, da bi konstanto k dali ime Boltzmann.
Zakon sevanja Stefana - Boltzmanna
Fizični zakon, ki določa, kako je energijska svetilnost (moč sevanja na enoto površine) absolutno črnega telesa odvisna od njene temperature, ima obliko j = σT 4 , to pomeni, da telo izžareva sorazmerno s četrto močjo njene temperature. Ta zakon se uporablja, na primer, v astrofiziki, saj je emisija zvezd po značilnostih blizu črnemu telesu.
V tem razmerju je še ena konstanta, ki prav tako nadzoruje obseg pojava. To je Stefan - Boltzmannova konstanta σ, ki je približno 5.67 × 10 -8 W / (m 2 K 4 ). Njegova dimenzija vključuje Kelvina - to pomeni, da je jasno, da tu sodeluje tudi Boltzmannova konstanta. Dejansko je količina σ definirana kot (2π 2 ∙ k 4 ) / (15c 2 h 3 ), kjer je c hitrost svetlobe, h pa je Planckova konstanta. Tako Boltzmannova konstanta, skupaj z drugimi svetovnimi konstantami, tvori količino, ki spet povezuje energijo (moč) in temperaturo med njimi - v tem primeru glede na sevanje.

Fizikalno bistvo Boltzmannove konstante
Ugotovljeno je bilo že, da je Boltzmannova konstanta ena od tako imenovanih temeljnih konstant. Ne gre le za to, da nam omogoča, da vzpostavimo povezavo med značilnostmi mikroskopskih pojavov molekularne ravni in parametri procesov, ki jih opazimo v makrosvetu. In ne samo, da je ta konstanta vključena v številne pomembne enačbe.
Trenutno ni znano, ali obstaja kakšno fizično načelo, na podlagi katerega bi ga lahko izpeljali teoretično. Z drugimi besedami, iz ničesar ne sledi, da bi morala biti vrednost dane konstante prav ta. Kot merilo ustreznosti kinetične energije delcev bi lahko uporabili druge vrednosti in druge enote namesto stopinj, potem bi bila numerična vrednost konstante drugačna, vendar bi ostala konstantna vrednost. Skupaj z drugimi tovrstnimi vrednotami - omejitveno hitrostjo c, Planckovo konstanto h, elementarno naboj e, gravitacijsko konstanto G - znanost prevzame Boltzmannovo konstanto kot danost našega sveta in se uporablja za teoretični opis fizikalnih procesov, ki se v njem odvijajo.