Hidracija alkenov: reakcija in enačbe
Ugotovite, kakšna je reakcija hidracije alkena. V ta namen podamo kratek opis tega razreda ogljikovodikov.
Splošna formula
Alkeni so nenasičeni organske spojine ki imajo splošno formulo SpN2n, v molekulah, v katerih je ena dvojna vez, in so prisotne tudi posamezne (preproste) vezi. Atomi ogljika v njem so v hibridnem stanju sp2. Predstavniki tega razreda se imenujejo etilen, saj je prednik te serije etilen.

Značilnosti nomenklature
Da bi razumeli mehanizem hidracije alkena, je treba razlikovati med značilnostmi njihovega imena. V skladu s sistematično nomenklaturo se pri sestavljanju imena alkena uporablja določen algoritem ukrepov.
Ad
Najprej morate določiti najdaljšo ogljikovo verigo, vključno z dvojno vezjo. Številke označujejo lokacijo radikalov ogljikovodikov, začenši z najmanjšo v ruski abecedi.
Če je v molekuli več enakih radikalov, se imenu dodajo di-, tri-, tetra-določujoče predpone.
Šele potem se imenuje veriga ogljikovih atomov, ki na koncu doda pripono -en. Da bi pojasnili lokacijo nenasičene (dvojne) molekule vezave, je to označeno s številom. Na primer 2metilpenten-2.

Hibridizacija v alkenih
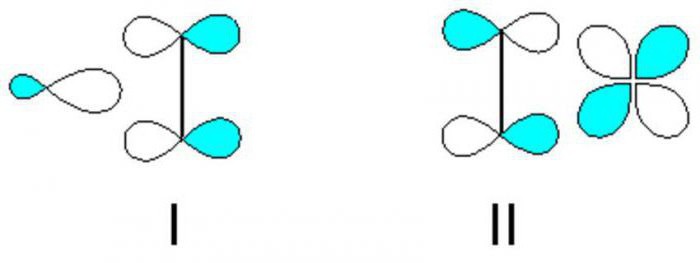
Za spoprijemanje z naslednjo nalogo: »Vzpostaviti molekulsko formulo alkena, katerega hidracija je dobila sekundarni alkohol«, je treba ugotoviti strukturne značilnosti predstavnikov tega razreda ogljikovodikov. Prisotnost dvojne vezi pojasnjuje sposobnost ShNu, da vstopi v adicijsko reakcijo. Kot med dvojnimi vezmi je 120 stopinj. Za nenasičeno vezjo ni opaziti rotacije, zato je izomerizem značilen za predstavnike tega razreda. To je dvojna vez, ki deluje kot glavno reakcijsko mesto v molekulah alkenov.
Ad
Fizične lastnosti
Podobne so nasičenim ogljikovodikom. Najnižji predstavniki tega razreda organskih ogljikovodikov so v normalnih pogojih plinaste snovi. Nadalje poteka postopen prehod na tekočine, za alkene, katerih molekule vsebujejo več kot sedemnajst atomov ogljika, je značilno trdno stanje. Vse spojine tega razreda imajo rahlo topnost v vodi, medtem ko so popolnoma topne v polarnih organskih topilih.
Značilnosti izomerizma
Prisotnost etilenskih spojin v molekulah pojasnjuje raznolikost njihovih strukturnih formul. Poleg izomerizacije ogljikovega skeleta, ki je značilen za predstavnike vseh razredov organskih spojin, imajo interklasni izomeri. To so cikloparafini. Na primer, za propen je interklasni izomer ciklopropan.
Prisotnost dvojne vezi v tem razredu molekul pojasnjuje možnost geometrijske cis in trans izomerije. Takšne strukture so možne le v simetričnih nenasičenih ogljikovodikih, ki imajo v svoji sestavi dvojno vez.
Obstoj te različice izomerije je določen z nemožnostjo proste rotacije atomov ogljika preko dvojne vezi.
Specifičnost kemijskih lastnosti
Mehanizem hidracije alkena ima določene značilnosti. Ta reakcija se nanaša na elektrofilno dodajanje.
Kako poteka reakcija hidracije? Če želite odgovoriti na to vprašanje, upoštevajte pravilo Markovnikov. Njegovo bistvo je v tem, da se hidracija alkenov asimetrične strukture izvaja na določen način. Vodikov atom se bo združil z bolj hidrogeniranim ogljikom. Hidroksilna skupina je vezana na ogljikov atom, ki je manjši od N. Hidracija alkenov vodi do tvorbe sekundarnih enodolnih alkoholov.
Ad
Da bi reakcija potekala v celoti, se kot katalizatorji uporabljajo mineralne kisline. Zagotavljajo vnos zahtevane količine vodikovih kationov v reakcijsko zmes.
Z hidracijo alkenov ni mogoče dobiti primarnih monohidričnih alkoholov, ker Markovnikovega pravila ne bomo opazili. Ta lastnost se uporablja v organski sintezi sekundarnih alkoholov. Vsaka hidracija alkenov se izvede brez uporabe težkih pogojev, zato je postopek našel svojo praktično uporabo.
Če je etilen vzet kot začetni predstavnik razreda SpN2p, Markovnikovo pravilo ne deluje. Katerih alkoholov ni mogoče dobiti s hidracijo alkenov? Zaradi takšnega kemijskega procesa ni mogoče dobiti primarnih alkoholov iz asimetričnih alkenov. Kako so alkeni hidrirani? Pridobivanje alkoholov sekundarni tip se izvaja na ta način. Če se kot ogljikovodik izbere reprezentativna serija acetilenov (alkini), hidracija povzroči proizvodnjo ketonov in aldehidov. 
Po Markovnikovem pravilu so alkeni hidrirani. Reakcija ima mehanizem elektrofilne adicije, katerega bistvo je dobro raziskano.
Poglejmo nekaj konkretnih primerov takšnih transformacij. Kaj povzroča hidracijo alkenov? Primeri, ki so na voljo v šolskem kemijskem tečaju, kažejo, da lahko propanol-2 dobimo iz propena z medsebojnim delovanjem z vodo in butanol-2 dobimo iz butena-1.
Ad
V industrijskih količinah se uporablja hidracija alkenov. Tako dobimo alkohole sekundarne sestave.

Halogenacija
Kvalitativna reakcija dvojna vez obravnava interakcijo nenasičenih ogljikovodikov s halogenskimi molekulami. Analizirali smo, kako poteka hidracija alkenov. Mehanizem halogeniranja je podoben.
Halogenske molekule imajo kovalentno nepolarno kemično vez. Z manifestacijo časovnih nihanj v vsaki molekuli se pojavi elektrofilnost. Posledično se poveča verjetnost pojava dodatka, ki ga spremlja uničenje dvojne vezi v molekulah nenasičenih ogljikovodikov. Po zaključku postopka je reakcijski produkt dihalogenalkan derivat. Brominacija je kvalitativna reakcija na nenasičene ogljikovodike, saj rjava barva halogena postopoma izgine.

Hidrohalogenacija
Preučili smo formulo za hidracijo alkenov. Reakcije medsebojnega delovanja z vodikovim bromidom imajo podobno različico. V tej anorganski spojini je torej kovalentna polarna kemijska vez elektronska gostota premaknjena na bolj elektronegativni atom broma. Vodik pridobi delni pozitivni naboj, da da halogen halogenu, napade molekulo alkena.
Ad
Če ima nenasičen ogljikovodik asimetrično strukturo, se tvorita dva produkta, ko medsebojno deluje z vodikovim halidom. Tako dobimo 1-bromoproan in 2-bromopropan iz propena med hidrohalogeniranjem.
Za predhodno oceno možnosti interakcij se upošteva elektronegativnost izbirnega substituenta.
Oksidacija
Dvojna vez nezasičenih ogljikovodikovih molekul je izpostavljena močnim oksidacijskim sredstvom. Imajo tudi elektrofilni značaj, ki se uporabljajo v kemični industriji. Posebej zanimiv je oksidacija alkenov z vodno (ali šibko alkalno) raztopino. kalijev permanganat. Imenuje se reakcija hidroksilacije, kar je posledica pridobivanja dihidričnih alkoholov.
Na primer, etilen-diol-1,2 (etilen glikol) dobimo z oksidacijo molekul etilena z vodno raztopino kalijevega permanganata. Ta interakcija se šteje za kvalitativno reakcijo na dvojno vez, saj med medsebojnim delovanjem opazimo razbarvanje raztopine kalijevega permanganata.
V kislem okolju (v težkih pogojih) lahko med reakcijskimi produkti opazimo aldehid.
Pri medsebojnem delovanju z atmosferskim kisikom opazimo oksidacijo ustreznega alkena v ogljikov dioksid in vodno paro. Proces spremlja sproščanje toplotne energije, zato se v industriji uporablja za pridobivanje toplote.
Prisotnost dvojne vezi v molekuli alkena kaže na možnost reakcij hidrogeniranja v tem razredu. Interakcija SpN2p z vodikovimi molekulami poteka med toplotno uporabo kot katalizatorji platine, niklja.
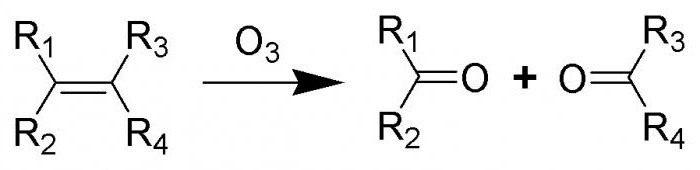
Mnogi predstavniki razreda alkenov so nagnjeni k ozoniranju. Pri nizkih temperaturah se predstavniki tega razreda odzovejo z ozonom. Proces spremlja prekinitev dvojne vezi, nastajanje cikličnih peroksidnih spojin, ki se imenujejo ozonidi. O-O vezi so prisotne v njihovih molekulah, zato so snovi eksplozivne snovi. Ozonidi niso sintetizirani v čisti obliki, razgrajujejo se s postopkom hidrolize, nato pa zmanjšujejo s pomočjo cinka. Produkti te reakcije so karbonilne spojine, ki so jih izolirali in identificirali raziskovalci.
Polimerizacija
Ta reakcija vključuje zaporedno integracijo več molekul alkena (monomerov) v veliko makromolekulo (polimer). Iz izhodnega etena dobimo polietilen z industrijsko uporabo. Polimer je snov, ki ima visoko molekulsko maso.
V makromolekuli je določeno število ponavljajočih se fragmentov, imenovanih strukturne enote. Za polimerizacijo etilena velja, da je skupina -CH2-CH2- strukturna enota. Stopnja polimerizacije kaže število enot, ki se ponavljajo v polimerni strukturi.
Stopnja polimerizacije določa lastnosti polimernih spojin. Na primer, polietilen s kratko verigo je tekočina, ki ima mazalne lastnosti. Za makromolekule z dolgimi verigami je trdno stanje nenavadno. Prožnost in plastičnost materiala, ki se uporablja pri izdelavi cevi, steklenic, filmov. Polietilen, v katerem je stopnja polimerizacije od pet do šest tisoč, ima visoko trdnost in se zato uporablja pri izdelavi trajnih niti, trdih cevi, litih izdelkov.
Med izdelki, pridobljenimi s polimerizacijo alkenov, ki imajo praktično vrednost, izberemo polivinil klorid. To spojino pripravimo s polimerizacijo vinilklorida. Nastali izdelek ima dragocene lastnosti delovanja. Zanj je značilna povečana odpornost na agresivne kemikalije, negorljiva, enostavna za barvanje. Kaj lahko naredimo iz polivinilklorida? Aktovke, dežni plašči, ogrinjalo, umetno usnje, kabli, izolacija električnih žic.
Teflon je produkt polimerizacije tetrafluoroetilena. Ta organska inertna spojina je odporna na nenadne temperaturne spremembe.
Polistiren je elastična prosojna snov, ki nastane s polimerizacijo prvotnega stirena. Nepogrešljiv je pri proizvodnji dielektrikov v radio in elektrotehniki. Poleg tega se polistiren v velikih količinah uporablja za proizvodnjo kislinsko odpornih cevi, igrač, glavnikov, porozne plastike.
Značilnosti pridobivanja alkenov
Predstavniki tega razreda so v povpraševanju v sodobni kemični industriji, zato so bile razvite različne metode za njihovo industrijsko in laboratorijsko pripravo. V naravi ne obstajajo etilena in njegovi homologi.
Številne laboratorijske možnosti za pridobitev predstavnikov tega razreda ogljikovodikov so povezane z inverznimi reakcijami dodajanja, imenovanimi izločanje (izločanje). Na primer, pri dehidrogeniranju parafinov (nasičenih ogljikovodikov) dobimo ustrezne alkene.
Pri interakciji halogenskih derivatov alkanov s kovinskim magnezijem je mogoče dobiti tudi spojine s splošno formulo SpH2n. Izločanje se izvaja po Zaitsevem pravilu, nasprotno Markovnikovo pravilo.
V industrijskih količinah so nenasičeni ogljikovodiki iz etilenskih serij pridobljeni s krekingom nafte. Plinski razpok in piroliza nafte in plina vsebuje od deset do dvajset odstotkov nenasičenih ogljikovodikov. V mešanici reakcijskih produktov so parafini in alkeni, ki so med seboj ločeni s frakcijsko destilacijo.
Nekatere aplikacije
Alkeni so pomembni razred organskih spojin. Možnost njihove uporabe je posledica odlične reaktivnosti, enostavnosti izdelave, razumnih stroškov. Med številnimi industrijskimi sektorji, ki uporabljajo alkenes, izberemo industrijo polimerov. Velika količina etilena, propilena, njihovih derivatov gre v proizvodnjo polimernih spojin.
Zato so vprašanja, povezana z iskanjem novih načinov proizvodnje alkenskih ogljikovodikov, tako pomembna.
Polivinilklorid velja za enega najpomembnejših izdelkov za uporabo, pridobljenih iz alkenov. Odlikujejo ga kemijska in toplotna stabilnost, nizka vnetljivost. Ker ta snov ni topna v mineralih, ampak topna v organskih topilih, se lahko uporablja v različnih industrijskih sektorjih.
Njegova molekulska teža je več sto tisoč. S povišanjem temperature se snov razgradi, čemur sledi sproščanje klorovodika.
Posebej zanimive so njegove dielektrične lastnosti, ki se uporabljajo v sodobni elektrotehniki. Med industrijami, v katerih se uporablja polivinilklorid, lahko izpostavimo proizvodnjo umetnega usnja. Nastali material v izvedbi nikakor ni slabši od naravnega materiala, medtem ko ima veliko nižje stroške. Oblačila iz tega materiala postajajo vedno bolj priljubljena pri modnih oblikovalcih, ki ustvarjajo svetle in barvite zbirke mladinskih oblačil iz polivinilklorida v različnih barvah.
Polivinil klorid se v velikih količinah uporablja kot tesnilo v hladilnikih. Zaradi svoje elastičnosti, odpornosti je ta kemična spojina potrebna pri izdelavi filmov in sodobnih razteznih stropov. Pralna tapeta je dodatno prekrita s tanko PVC folijo. To jim omogoča, da dodajo mehansko trdnost. Takšni zaključni materiali bodo idealna možnost za obnovo pisarniških prostorov.
Hidratacija alkenov povzroča tudi tvorbo primarnih in sekundarnih enodolnih alkoholov, ki so odlična organska topila.