Kakšna je porazdelitev elektronov v energijskih nivojih različnih kemijskih elementov?
Porazdelitev elektronov v energijskih nivojih pojasnjuje kovinske in nekovinske lastnosti vseh elementov.
Elektronska formula
Obstaja določeno pravilo, po katerem so prosti in parni negativni delci postavljeni na ravni in podravne. Oglejmo podrobneje porazdelitev elektronov po energijskih nivojih.
Na prvi energetski ravni sta le dva elektrona. Orbitale zapolnijo z naraščanjem oskrbe z energijo. Porazdelitev elektronov v atomu kemičnega elementa ustreza zaporedni številki. Na energetski ravni z najmanjšim številom najbolj izrazitih težnost valenčni elektroni do jedra.
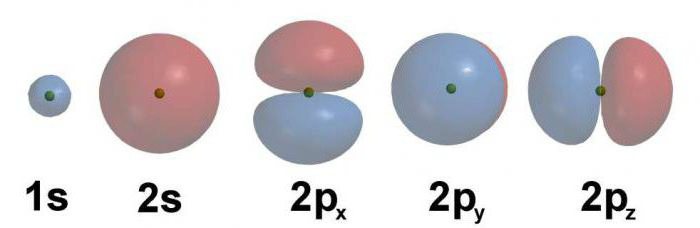
Primer elektronske formule
Razmislite o porazdelitvi elektronov energije s primerom ogljikovega atoma. Njegova zaporedna številka je 6, zato je v jedru šest protonov s pozitivnim nabojem. Glede na to, da je ogljik reprezentativen za drugo obdobje, je značilna prisotnost dveh energetskih nivojev. Na prvi sta dva elektrona, na drugi - štiri.
Ad
Pravilo Hunda razlaga razporeditev v isti celici le dveh elektronov, ki imajo različne vrte. Na drugi energetski ravni so štirje elektroni. Posledično ima porazdelitev elektronov v atomu kemičnega elementa naslednjo obliko: 1s22s22p2.
Obstajajo določena pravila, po katerih je porazdelitev elektronov po nivojih in nivojih.
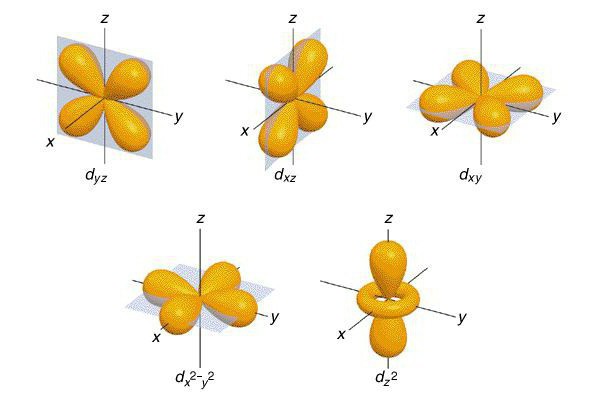
Princip Paulija
To načelo je oblikoval Pauli leta 1925. Znanstvenik se je strinjal z možnostjo postavitve v atom le dva elektrona, ki imata enaka kvantna števila: n, l, m, s. Upoštevajte, da se porazdelitev elektronov v energijskih nivojih pojavi, ko se zaloga proste energije poveča.
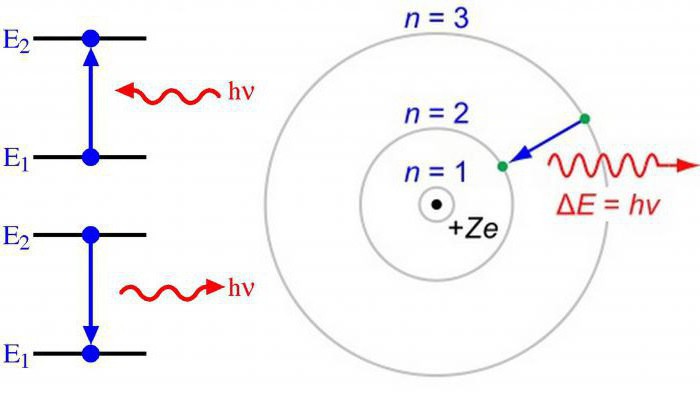
Pravilo Klechkovsky
Polnjenje energijskih orbital se izvaja glede na povečanje kvantnih števil n + l in je značilno povečanje zaloge energije.
Razmislite o porazdelitvi elektronov v atomu kalcija.
V normalnem stanju ima njegova elektronska formula naslednjo obliko:
Ca 1s2 2s2 2p6 3s2 3p6 3d0 4s2.
Elementi podobnih podskupin, ki se nanašajo na d- in f-elemente, imajo "neuspeh" elektrona iz zunanje ravni, ki ima manjšo energetsko rezervo, do prejšnjega d- ali f-podrazreda. Podoben pojav je značilen za baker, srebro, platino, zlato.
Ad
Porazdelitev elektronov v atomu vključuje polnjenje nižjih nivojev z neparnimi elektroni, ki imajo enake vrtljaje.
Šele potem, ko so vse proste orbite popolnoma napolnjene z enojnimi elektroni, se kvantne celice dopolnijo z drugimi negativnimi delci, ki imajo obrnjene nasprotne spine.
Na primer, v nepokritem stanju dušika:
1s2 2s2 2p3.
Lastnosti snovi imajo učinek elektronsko konfiguracijo valenčni elektroni. S svojim številom lahko določite višjo in nižjo valenco, kemijsko aktivnost. Če je element v glavni podskupini periodnega sistema, lahko s številko skupine naredite zunanjo energetsko raven, jo določite oksidacijska stanja. Na primer, fosfor, ki je v peti skupini (glavna podskupina), vsebuje pet valentnih elektronov, zato je sposoben sprejeti tri elektrone ali dati pet delcev drugemu atomu.
Ad
Izjeme od tega pravila so vsi predstavniki podskupin periodnega sistema.
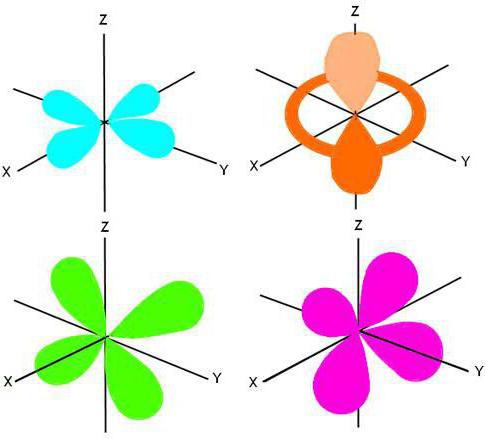
Družinske funkcije
Glede na strukturo zunanje energije je razčlenitev vseh nevtralnih atomov v periodnem sistemu v štiri družine:
- s-elementi so v prvi in drugi skupini (glavne podskupine);
- p-družina se nahaja v skupinah III-VIII (podskupine A);
- d-elemente lahko najdemo v podobnih podskupinah od I. do VIII. skupine;
- F-družino sestavljajo aktinidi in lantanidi.
Vsi s-elementi v normalnem stanju imajo valentne elektrone na s-podnizu. Prisotnost prostih elektronov na s- in p-nivojih je značilna za p-elemente.
D-elementi v neizraženem stanju imajo valentne elektrone tako na zadnjem s- kot tudi na zadnjem d-nivoju.
Zaključek
Stanje katerega koli elektrona v atomu je mogoče opisati z uporabo niza osnovnih števil. Glede na značilnosti njegove strukture lahko govorimo o določeni količini energije. Z uporabo pravila Hund, Klechkovsky, Pauli za vsak element, ki je vključen v periodni sistem, lahko ustvarite konfiguracijo nevtralnega atoma.
Elektroni, ki se nahajajo na prvih ravneh, imajo najmanjšo količino energije v neizraženem stanju. Ko se nevtralni atom segreje, opazimo prehod elektronov, ki ga vedno spremlja sprememba števila prostih elektronov, kar vodi do pomembne spremembe v stopnji oksidacije elementa in spremembi njegove kemijske aktivnosti.