Kaj je elektroliza v kemiji?
Najprej poskušajmo razumeti, kaj je elektroliza. To so kemijske reakcije, ki nastanejo pod vplivom električnega toka na elektrode, ki se vstavijo v talilno ali elektrolitno raztopino.
Nekateri teoretični koncepti
Elektrolit je snov, ki prevaja elektriko. Elektrode so dveh vrst. Katoda je negativno nabita elektroda, na njej se pojavi redukcijska reakcija.
Anoda se imenuje pozitivno naelektrena elektroda, kjer se izvaja restavracija.
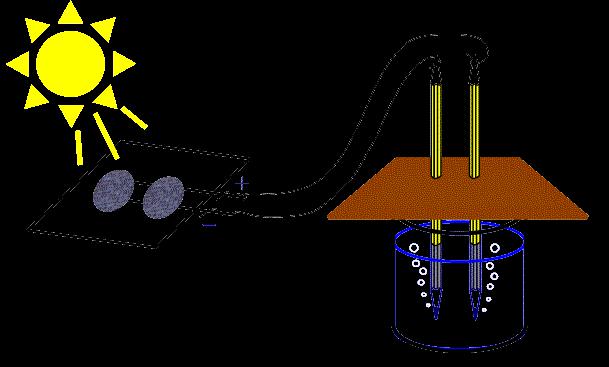
Uporaba procesa
Elektroliza raztopin se uporablja v različnih vejah sodobne industrije. V kemični industriji se s tem postopkom pridobiva klor, alkalija, perklorat, klorat, persulfat, organska snov, kalijev permanganat, persulfurna kislina, fluor, kisik, vodik in drugi dragoceni proizvodi.
V barvni metalurgiji se elektroliza taline uporablja za pridobivanje čiste kovine iz rud. Kovine, ki jih zaradi visokega negativnega potenciala vodnih raztopin ni mogoče izolirati, pridobimo v barvni metalurgiji z elektrolizo taline. Med kovinami, ki se proizvajajo z elektrolizo tako imenovanih staljenih medijev, opažamo magnezij, aluminij, uran, berilij, cirkonij.
Elektroliza se uporablja v strojništvu, elektronski industriji, radijskem inženirstvu, tiskarstvu, za nanašanje tankih kovinskih premazov na izdelke, jih ščiti pred korozijo, povečuje odpornost proti obrabi, povečuje toplotno odpornost.

Zgodovinsko ozadje
Kaj je elektroliza? To je eno najpomembnejših področij elektrokemije. Znanost se je rodila na prelomu 18-19 stoletja. V tem obdobju so eksperimente vodili italijanski fiziolog L. Galvani in fizik A. Volt. Konec 18. stoletja so se pojavili prvi kemijski tokovni viri. V začetku 20. stoletja je elektrokemija začela preučevati elektrokemijske procese. Eksperimentalno je bilo ugotovljeno, da električni tok, ki prehaja skozi vodne raztopine soli, povzroča kemične transformacije, ki vodijo v tvorbo novih spojin.
Trdimo, kaj je elektroliza, ugotavljamo, da gre za kompleksen sklop procesov: migracija ionov, difuzija, ionske elektrokemijske reakcije, sekundarne kemijske reakcije produktov elektrolize med seboj.
Klasifikacija procesov
Ko že govorimo o tem, kaj je elektroliza, je treba razmišljati o klasifikaciji elektrolitskih procesov. Razdeljeni so na:
- proizvodnja anorganskih spojin (klor, kisik, vodik);
- tvorbo kovin (magnezij, baker, aluminij, kalij, natrij, berilij, srebro, baker);
- pridobivanje kovinskih in galvanskih prevlek;
- nitriranje, električno poliranje, boroizacija kovinske površine;
- filmska aplikacija z elektroforezo;
- razsoljevanje vode in elektrodializa;
- proizvodnjo različnih organskih snovi.
Poskusi elektrolize
Kako narediti enačbo elektrolize? Ta postopek poteka v elektrolitih. Z dvema ogljikovima elektrodama je mogoče povezati žice, ki prihajajo iz omrežja za razsvetljavo.
V eni od njih vklopite električno svetilko, ki bo potrdila prisotnost v tokokrogu električnega toka. Proste konce elektrod lahko postavimo v suho namizno sol ali brezvodno žveplovo kislino.
Žarnica ne gori, ker snovi ne morejo izvajati električnega toka, vezje pa ostane odprto. Podoben rezultat opazimo v primeru, ko so elektrode potopljene v steklo z destilirano vodo.
Ko se v vodi raztopi majhna količina soli, alkalij in kisline, opazimo svetlo luminiscenco.
Ko se elektrode spustijo v raztopino glicerina ali sladkorja, žarnica preneha svetiti.
Ta poskus seveda potrjuje prevodnost soli, baz, kislih raztopin električnega toka.
S prehodom električnega toka skozi raztopine ali taline opazimo kemične spremembe, ki se izražajo v sproščanju produktov razgradnje topila ali raztopine.

Kakšen je postopek v primeru kuhinjske soli
Med eksperimentalnimi opazovanji je bilo ugotovljeno, da elektroliza vodne raztopine natrijevega klorida vodi do tvorbe vodika na katodi, pri čemer se na anodi sprosti plinasti klor. Kako matematično opisati ta proces? Elektrolit natrijevega klorida se pojavi v talini, kar povzroči nastanek čiste alkalijske kovine na katodi in plinastega klora na anodi.
... in magnezijev klorid
Po prehodu eklektičnega toka skozi talino magnezijevega klorida opazimo pojav magnezijevih kationov in klorovih anionov.
Na katodi opazimo redukcijo magnezijevih kationov na čisto kovino, klorni anioni, ki gredo v anodo, darovajo elektrone, proces oksidacije poteka. Elektrolizo magnezijevega klorida lahko zapišemo kot povzetek enačbe:
MgCl2 = Mg + Cl2
Značilnosti elektrolize v raztopinah
Pomembno je upoštevati dejstvo, da poleg ionov elektrolitov v raztopini obstajajo tudi vodne raztopine: vodikovi kationi in anioni hidroksilne skupine. Zato katoda lahko odvaja elektrolitski kation in vodikov proton. Na anodi se izpraznijo hidroksilni ioni in elektrolitski anioni.

Tudi vodne molekule so lahko izpostavljene elektrokemični redukciji ali oksidaciji.
S skrbnim upoštevanjem katodnih procesov, ki se pojavijo med elektrolizo vodne raztopine, je pomembno upoštevati potencialni potencial redukcije vodikovih protonov. Odvisna je od koncentracije vodikovih kationov, ki imajo vrednost -0,41 V.
Če je v raztopini elektrolita kovina, pri kateri ima potencial elektrode več pozitivne vrednosti, bo katoda obnovljena v okviru elektrolize. Ta trditev velja za tiste kovine, ki se nahajajo v bližini vodika v elektrokemični seriji Beketovih napetosti. Z bolj negativno vrednostjo elektrodnega potenciala kot pri vodikovih kationih se kovina ne bo obnovila na katodi. V takšnih primerih se na tej elektrodi nabira vodik.
Če je potencial kovine podoben vrednosti -0,41 V, je dopustna istočasna tvorba vodika in čiste kovine na katodi.
Na naravo katodnega procesa pri elektrolizi raztopine soli (alkalij) vpliva položaj kovine v seriji elektrokemičnih napetosti Beketovih kovin.
Pri analizi procesov, ki se odvijajo na anodi, je treba upoštevati dejstvo, da je mogoča oksidacija anodnega materiala. Zato bo elektrokemija ločila inertno anodo kot tudi elektrodo, ki jo sestavljajo njihova aktivna anoda.
Inertna je anoda, v kateri se material ne oksidira kot del procesa elektrolize. Aktivno se šteje za anodo, ki lahko oksidira med elektrolizo.
Za inertne anode izberite platino, premog, grafit. Ta možnost se upošteva pri šolskem kemijskem tečaju.

Tipični primeri elektrolize vodnih raztopin
Začnimo s posebnostmi elektrolize v raztopini bakrovega klorida (2). Ker se ta kovina v elektrokemični seriji kovinskih aktivnosti nahaja na desni strani vodika, se na katodi tvori kovinski baker. Kloridni ioni se odvajajo v anodni prostor in tvorijo plinasti klor. Shema postopka je predstavljena v naslednji obliki:
- Katoda: Cu 2+ 2e = Cu.
- Anoda: 2Cl - -2e = Cl2 .
Kumulativna enačba:
- CuCl2 = Cu + Cl2 .
Kakšna je elektroliza vodne raztopine natrijevega sulfata? Ker se natrij nahaja v območju aktivnosti kovin na levi strani vodika, se na katodi opazi nastajanje molekularnega vodika. Poleg tega se v prostoru katode kopičijo hidroksidni ioni.
Na anodi se sprosti plinasti kisik in v bližini te elektrode se kopičijo hidroksidni ioni.
Ker natrijevi kationi in sulfatni ioni ostajajo v raztopini, ta del raztopine ostaja električno nevtralen. Shemo takšne elektrolize lahko predstavimo na naslednji način:
- 2Na2S04 + 6H2O = 4NaOH + 2H2S04 + O2 + 2H2

Dejavniki, ki vplivajo na postopek elektrolize
Učinkovitost te kemijske reakcije ovrednoti več dejavnikov, med katerimi je mogoče opozoriti: napetost, jakost toka, trenutna učinkovitost, učinkovitost, poraba električne energije na enoto nastalega proizvoda, gostota toka.
Trenutna moč označuje delovanje elektrolizatorja. In ko je višja, večja je količina izdelka na elektrodah.
Tokovni izhod omogoća upośtevanje ućinkovitosti uporabe elektrićnega toka, ki poteka skozi elektrolizer.