Kaj je atom? Katere dele sestavlja in kako se meri njegova masa?
Sodobni človek nenehno sliši fraze, ki vsebujejo derivate iz besede "atom". To je energija elektrarna, bomba. Nekdo vzame to za samoumevno, nekateri pa postavljajo vprašanje: "Kaj je atom?".
Kaj pomeni ta beseda?
Ima starogrške korenine. Prihaja iz "atoma", kar dobesedno pomeni "neobrezan".
Nekdo, ki je že malo seznanjen s fiziko atoma, bo ogorčen: "Kot" nerezan, "je sestavljen iz nekaterih delcev!" Stvar je v tem, da se je ime pojavilo, ko znanstveniki še vedno niso vedeli, da atomi niso najmanjši delci.
Po izkušenem dokazu o tem dejstvu je bilo odločeno, da ne spremeni običajnega imena. Leta 1860 se je »atom« začel imenovati najmanjši delček, ki ima vse lastnosti kemičnega elementa, ki mu pripada.
Ad
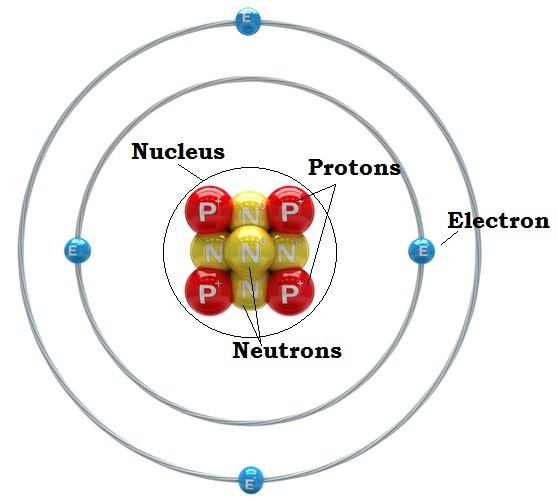
Kaj je več kot atom in manj?
Molekula je vedno večja. Oblikovan je iz več atomov in je najmanjši delček snovi.
Toda manj - elementarni delci. Na primer, elektroni in protoni, nevtroni in kvarkovi. Veliko jih je.

Že veliko stvari je bilo povedanih o njem. Vendar še vedno ni povsem jasno, kaj je atom.
Kakšen je?
Vprašanje, kako predstaviti model atoma, so že dolgo zasedli znanstveniki. Danes je bila predlagana E. Rutherford in dokončno oblikoval N. Bor. Po njem je atom razdeljen na dva dela: jedro in elektronski oblak.

Večina mase atoma je zgoščena v njenem središču. Jedro je sestavljeno iz nevtronov in protonov. In elektroni v atomu se nahajajo na dovolj veliki razdalji od centra. Izkazalo se je, da je nekaj podobnega sončnemu sistemu. V središču, kot so sonce, jedro in okoli njega se elektroni vrtijo v svojih orbitalih, kot planeti. Zato se model pogosto imenuje planetarni.
Ad
Zanimivo je, da jedro in elektroni zavzemajo zelo majhen prostor v primerjavi s celotno velikostjo atoma. Izkazalo se je, da je v središču majhnega jedra. Potem praznina. Zelo velika praznina. In potem ozek trak majhnih elektronov.
Takemu modelu atomov znanstveniki niso prišli takoj. Pred tem je bilo podanih veliko predpostavk, ki so jih poskusi ovrgli.
Ena od teh zamisli je bila predstavitev atoma kot trdnega telesa, ki ima pozitiven naboj. In elektroni v atomu naj bi bili postavljeni po vsem tem telesu. Takšno idejo je predstavil J. Thomson. Njegov model atoma se je imenoval tudi »puding z rozinami«. Model je zelo podoben tej posodi.
Ampak to je bilo nevzdržno, ker ni moglo pojasniti nekaterih lastnosti atoma. Zato je bila zavrnjena.
Japonski znanstvenik H. Nagaoka je na vprašanje, kaj je atom, predlagal takšen model. Po njegovem mnenju ima ta delček podobno podobo planetu Saturn. V središču jedra in elektroni se vrtijo okoli njega v orbitah, povezanih v obroč. Kljub temu, da model ni bil sprejet, so bile nekatere njegove določbe uporabljene v planetarni shemi.
O številkah, povezanih z atomom
Prvič, o fizikalnih količinah. Celotni naboj atoma je vedno nič. To je posledica dejstva, da je število elektronov in protonov v njem enako. Njihova dajatev je enake velikosti in ima nasprotne znake.
Ad
Pogosto obstajajo situacije, ko atom izgubi elektrone ali, nasprotno, pritegne odvečno. V takih situacijah je rečeno, da je postal ion. In njegova obremenitev je odvisna od tega, kaj se je zgodilo z elektroni. Če je njihovo število manj, je ionski naboj pozitiven. Ko je več elektronov, ion postane negativen.

Zdaj o kemiji. Ta znanost, kot nobena druga, daje najbolj razumevanje o tem, kaj je atom. Navsezadnje tudi glavna miza, ki jo proučujemo, temelji na dejstvu, da so atomi v njej razporejeni v določenem zaporedju. Govorimo o periodnem sistemu.
V njem je vsakemu elementu dodeljeno določeno število, ki je povezano s številom protonov v jedru. Običajno je označena z črko z.
Naslednja vrednost je masna številka. Je enaka vsoti protonov in nevtronov, ki se nahajajo v jedru atoma. Njena oznaka je sprejeta s črko A.
Ti dve številki sta med seboj povezani z naslednjo enakostjo:
A = z + N.
Tu je N število nevtronov v atomskem jedru.
Druga pomembna količina je masa atoma. Za njeno merjenje je uvedena posebna vrednost. Zmanjšuje se : a.e.m. In bere kot atomska enota mase. Izhajajoč iz te enote, imajo trije delci, ki sestavljajo vse atome vesolja:
| elementarni delec | masa v amu |
| proton | 1.0073 |
| nevtron | 1,0087 |
| elektron | 0,0005 |
Te vrednosti so pogosto potrebne pri reševanju kemijskih problemov.