Kaj je reverzibilna reakcija?
Kaj je reverzibilna reakcija? To je kemijski proces, ki poteka v dveh nasprotnih smereh. Razmislite o glavnih značilnostih takšnih transformacij in njihovih značilnih parametrih.
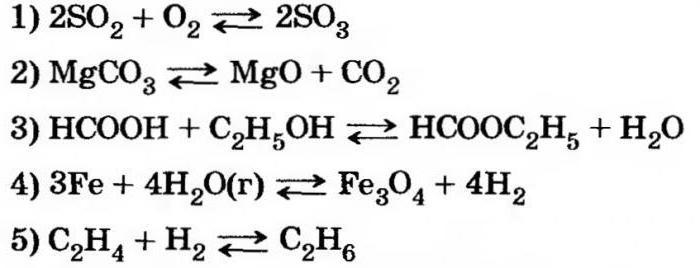
Kaj je bistvo ravnotežja
Reverzibilne kemijske reakcije ne proizvajajo določenih izdelkov. Na primer, med oksidacijo žveplovega oksida (4), istočasno s proizvodnjo žveplovega oksida (6), se ponovno tvorijo začetne komponente.
Nepovratni postopki vključujejo popolno transformacijo interakcijskih snovi, ki jo spremlja podobna reakcija, ki prejema en ali več reakcijskih produktov.
Primeri nepovratnih interakcij so reakcije razgradnje. Na primer pri ogrevanju kalijev permanganat nastane kovinski manganat, manganov oksid (4) in sprosti se tudi plinasti kisik.
Ad
Reverzibilna reakcija ne pomeni nastajanja padavin, razvijanje plina. To je ravno njena glavna razlika od nepovratne interakcije.
Kemijsko ravnovesje je takšno stanje interakcijskega sistema, v katerem se lahko ena ali več kemijskih reakcij pojavi reverzibilno pod pogojem, da so stopnje procesov enake.
Če je sistem v dinamičnem ravnovesju, ni spremembe temperature, koncentracije reagentov, drugih parametrov v danem časovnem obdobju.

Pogoji ravnotežnega premika
Reverzibilno reakcijsko ravnotežje je mogoče razložiti s pravilom Le Chatelier. Njegovo bistvo je v tem, da se pri zunanjem vplivu na sistem, ki je sprva v dinamičnem ravnovesju, spremeni reakcija v nasprotni smeri učinka. Vsaka reverzibilna reakcija s tem načelom se lahko premakne v pravo smer v primeru spremembe temperature, tlaka in koncentracije medsebojno učinkovitih snovi.
Ad
Načelo Le Chatelier "dela" samo za plinaste reagente, trdne in tekoče snovi se ne upoštevajo. Obstaja vzajemno razmerje med tlakom in volumnom, ki ga določa Mendelejeva - Clapeyronova enačba. Če je volumen začetnih plinastih sestavin večji od reakcijskih produktov, potem je za spremembo ravnovesja v desno pomembno povečati tlak mešanice.
Na primer, pri preoblikovanju ogljikov monoksid (2) v ogljikov dioksid 2 mol reagira ogljikov monoksid in 1 mol kisika. To tvori 2 mola ogljikovega monoksida (4).
Če je treba zaradi stanja problema to reverzibilno reakcijo premakniti v desno, je potrebno povečati pritisk.
Koncentracija reaktantov prav tako pomembno vpliva na postopek. V skladu z načelom Le Chatelierja se v primeru povečanja koncentracije začetnih komponent ravnotežje procesa premakne proti produktu njihove interakcije.
V tem primeru zmanjšanje (odstranitev iz reakcijske zmesi) nastalega proizvoda prispeva k pretoku neposrednega postopka.
Poleg pritiska, koncentracije, ima sprememba temperature pomemben vpliv na potek povratne ali neposredne reakcije. Ko se začetna zmes segreje, opazimo ravnotežni premik proti endotermnemu procesu.
Ad

Primeri reverzibilnih reakcij
Razmislite o specifičnih postopkih za premik ravnotežja proti nastajanju reakcijskih produktov.
2CO + 02-2C02
Ta reakcija je homogen postopek, saj so vse snovi v istem (plinskem) stanju.
V levem delu enačbe so 3 količine komponent, po interakciji se je ta kazalnik zmanjšal, oblikovali smo 2 volumna. Za pretok neposrednega postopka je potrebno povečati tlak reakcijske zmesi.
Glede na to, da je reakcija eksotermna, se temperatura zniža, da nastane ogljikov dioksid.
Ravnotežje procesa se bo premaknilo v smeri tvorbe reakcijskega produkta z naraščajočo koncentracijo enega od izhodnih snovi: kisika ali ogljikovega monoksida.
Zaključek
Reverzibilne in nepovratne reakcije imajo pomembno vlogo v človeškem življenju. Procesi izmenjave, ki se pojavljajo v našem telesu, so povezani s sistematičnim premikom v kemičnem ravnotežju. V kemijski proizvodnji se uporabljajo optimalni pogoji za usmerjanje reakcije v pravo smer.