Lastnosti soli: fizikalne in kemijske
Vsak dan smo soočeni s solmi in niti ne razmišljamo o vlogi, ki jo imajo v našem življenju. Ampak brez njih voda ne bi bila tako okusna in hrana ne bi prinesla užitka, rastline ne bi rasle in življenje na zemlji ne bi moglo obstajati, če v našem svetu ne bi bilo soli. Kakšne so torej te snovi in katere lastnosti soli so nujne?
Kaj je sol
V kompoziciji je najštevilčnejši razred, ki ga odlikuje raznolikost. это продукт реакции между кислотой и основанием, при которой водородный атом заменяется металлическим. Že v 19. stoletju je kemik J. Vercelius določil sol - to je produkt reakcije med kislino in bazo, v kateri je vodikov atom nadomeščen s kovinskim. V vodi so soli običajno disociirane v kovino ali amonij (kation) in kislinski ostanek (anion).

Sol lahko dobite na naslednje načine:
- z medsebojnim delovanjem kovine in nekovin, v tem primeru brez kisika;
- ko kovina sodeluje s kislino, dobimo sol in sprostimo vodik;
- kovina lahko premesti drugo kovino iz raztopine;
- кислотного и основного (еще их называют оксидом неметалла и оксидом металла соответственно); v medsebojnem delovanju dveh oksidov , kislih in bazičnih (imenujemo jih tudi nekovinski oksid oziroma kovinski oksid);
- reakcija kovinskega oksida in kisline proizvaja sol in vodo;
- reakcija med bazo in nekovinskim oksidom daje tudi sol in vodo;
- z reakcijo ionske izmenjave lahko reagirajo različne vodotopne snovi (baze, kisline, soli), reakcija pa se bo nadaljevala, če se v vodi tvorijo plin, voda ali rahlo topne (netopne) soli.
Lastnosti soli so odvisne samo od kemijske sestave. Najprej pa poglejmo njihove razrede.
Razvrstitev
Glede na sestavo se razlikujejo naslednji razredi soli: t
- o vsebnosti kisika (ki vsebuje kisik in kisik);
- pri interakciji z vodo (topna, slabo topna in netopna).
Takšna razvrstitev ne odraža v celoti raznolikosti snovi. Moderna in najbolj popolna klasifikacija, ki ne odraža le sestave, ampak tudi lastnosti soli, je predstavljena v naslednji tabeli.
| Sol | |||||
|---|---|---|---|---|---|
| Normalno | Kislo | Main | Dvoposteljna | Mešano | Kompleksno |
| Vodik se popolnoma zamenja | Vodikove atome ne nadomesti metal | Osnovne skupine se nadomestijo s kislinskim ostankom, ki ni v celoti | Sestavljen iz dveh kovin in enega kislega ostanka | Sestavljen je iz enega kovinskega in dveh kislih ostankov | Kompleksne snovi, ki so sestavljene iz kompleksnega kationa in aniona ali kationa in kompleksnega aniona |
| NaCl | KHSO 4 | FeOHSO 3 | KNaSO 4 | CaClBr | [Cu (NH3) 4 ] S04 |
Fizične lastnosti
Kljub širokemu razredu teh snovi je mogoče opredeliti splošne fizikalne lastnosti soli. To so snovi z ne-molekularno strukturo z ionsko kristalno mrežo.
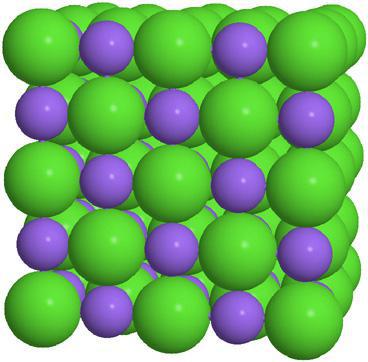
Zelo visoke točke taljenja in vrelišča. V normalnih pogojih vse soli ne izvajajo elektrike, vendar je večina od njih popolnoma prevodnih v raztopini.
Barva je lahko zelo različna, odvisna je od kovinskega iona, ki je njegov del. Železov sulfat (FeSO 4 ) je zelen, železov klorid (FeCl 3 ) je temno rdeč in kalijev kromat (K 2 CrO 4 ) je lepa svetlo rumena barva. Večina soli pa je še vedno brezbarvna ali bela.

Topnost v vodi se spreminja in je odvisna od sestave ionov. Načeloma imajo vse fizikalne lastnosti soli. Odvisni so od tega, kateri kovinski ion in kateri kislinski ostanek je vključen v sestavo. Še naprej razmišljamo o soli.
Kemijske lastnosti soli
Tudi tu je pomembna značilnost. Poleg fizikalnih, kemijskih lastnosti soli so odvisne od njihove sestave. In tudi, na kateri razred pripada.

Toda splošne lastnosti soli se še vedno lahko razlikujejo:
- mnogi od njih se pri segrevanju razgradijo v dva oksida: kisli in bazični, brez kisika - kovinski in nekovinski;
- soli medsebojno delujejo tudi z drugimi kislinami, toda reakcija poteka samo, če sol vsebuje kisli ostanek šibke ali hlapne kisline ali je rezultat netopna sol;
- interakcija z alkalijami je mogoča, če kation tvori netopno bazo;
- reakcija je mogoča med dvema različnima solema, vendar le, če se ena od na novo nastalih soli ne raztopi v vodi;
- lahko pride do reakcije s kovino, vendar je to mogoče le, če kovino, ki se nahaja desno od območja napetosti, vzamemo iz kovine v soli.
O kemijskih lastnostih normalnih soli govorimo zgoraj, medtem ko drugi razredi reagirajo s snovmi na nekoliko drugačen način. Razlika pa je le pri izdelkih na prodajnem mestu. V bistvu so ohranjene vse kemijske lastnosti soli in zahteve za reakcije.