Klasifikacija termodinamičnih sistemov
Razmislite o značilnostih termodinamičnih sistemov. Pod njimi se običajno razumejo fizične makroskopske oblike, sestavljene iz velikega števila delcev, ki niso namenjeni za opisovanje makroskopskih parametrov vsakega posameznega delca.
Ni omejitev v naravi materialnih delcev, ki so sestavni del takih sistemov. Lahko jih predstavimo v obliki molekul, atomov, ionov, elektronov, fotonov.
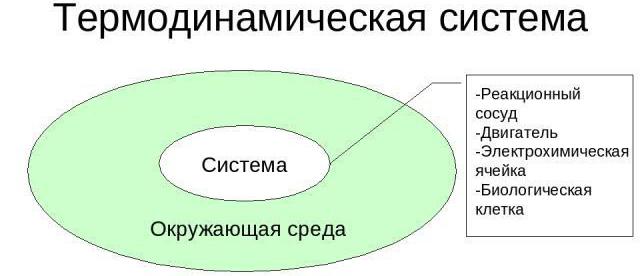
Posebne lastnosti
Analizirajmo značilne lastnosti termodinamičnih sistemov. Kot primer lahko vzamete kateri koli predmet, ki ga lahko opazite brez uporabe teleskopov, mikroskopov. Za popoln opis takega sistema so izbrane makroskopske podrobnosti, s katerimi lahko določimo volumen, tlak, temperaturo, električno polarizacijo, magnetno indukcijo, kemično sestavo in maso komponent.
Ad
Za vse termodinamične sisteme obstajajo pogojne ali realne meje, ki jih ločujejo od okolja. Namesto tega pogosto uporabljajo koncept termostata, za katerega je značilna tako visoka vrednost toplotne zmogljivosti, da v primeru izmenjave toplote s sistemom, ki ga analiziramo, temperaturni indeks ostane konstanten.
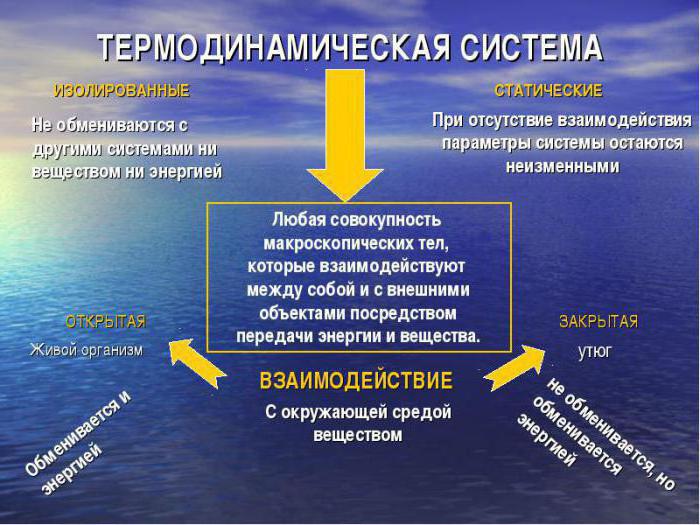
Klasifikacija sistemov
Razmislite, kaj je klasifikacija termodinamičnih sistemov. Glede na naravo njegove interakcije z okoljem je običajno navesti:
- izolirane vrste, ki ne izmenjujejo snovi ali energije z zunanjim okoljem;
- adiabatsko izolirana, ne izmenjava snovi z zunanjim okoljem, ampak vstopanje v izmenjavo dela ali energije;
- zaprti termodinamični sistemi nimajo izmenjave snovi, dovoljena je le sprememba energijske vrednosti;
- za odprte sisteme je značilen popoln prenos energije, snovi;
- delno odprte lahko imajo polprepustne stene, zato niso popolnoma vključene v izmenjavo materialov.
Glede na opis lahko parametre termodinamičnega sistema razdelimo na kompleksne in preproste.

Značilnosti enostavnih sistemov
Enostavne sisteme imenujemo ravnotežna stanja, katerih fizično stanje lahko določimo s specifičnim volumnom, temperaturo, tlakom. Primeri tovrstnih termodinamičnih sistemov so izotropna telesa, ki imajo enake značilnosti v različnih smereh in točkah. Torej, tekočine, plinaste snovi, trdne snovi, ki so v stanju termodinamičnega ravnovesja, niso izpostavljene elektromagnetnim in gravitacijskim silam, površinski napetosti, kemičnim transformacijam. Analiza enostavnih teles je v termodinamiki priznana kot pomembna in relevantna s praktičnega in teoretičnega vidika.
Ad
Notranja energija tovrstni termodinamični sistem je povezan z okoljem. Pri opisu uporabe števila delcev, mase snovi vsake posamezne komponente.
Kompleksni sistemi
Kompleks vključuje termodinamične sisteme, ki ne sodijo v preproste oblike. Na primer, to so magneti, dielektriki, trdna elastična telesa, superprevodniki, vmesne površine, toplotno sevanje, elektrokemijski sistemi. Kot parametre, uporabljene za njihovo opisovanje, ugotavljamo elastičnost vzmeti ali palice, površino faznega odseka, toplotno sevanje.
Fizični sistem se imenuje takšen sklop, v katerem ni kemijske interakcije med snovmi v mejah temperature, tlaka, izbranih za študijo. In kemijski sistemi imenujejo tiste možnosti, ki vključujejo interakcijo med njenimi posameznimi komponentami.
Ad
Notranja energija termodinamičnega sistema je odvisna od prisotnosti njene izolacije z zunanjim svetom. Na primer, kot varianta adiabatne lupine si lahko predstavljamo Dewarjevo plovilo. Homogenost se kaže v sistemu, v katerem imajo vse komponente podobne lastnosti. Primeri teh so plinske, trdne, tekoče raztopine. Tipičen primer homogene plinske faze je atmosfera Zemlje.
Značilnosti termodinamike
Ta del znanosti se ukvarja s preučevanjem osnovnih zakonov, ki urejajo procese, povezane z sproščanjem, absorpcijo energije. V kemijski termodinamiki je namenjena preučevanju medsebojnih transformacij sestavnih delov sistema, da se določijo zakoni, ki urejajo prehod ene vrste energije v drugo pod danimi pogoji (tlak, temperatura, volumen).
Sistem, ki je predmet termodinamičnih raziskav, lahko predstavimo kot vsak predmet narave, ki vključuje veliko število molekul, ki so ločene z vmesnikom z drugimi realnimi predmeti. Pod stanjem sistema izhaja kombinacija njenih lastnosti, ki omogočajo, da jo določimo s stališča termodinamike.
Ad
Zaključek
V vsakem sistemu je prehod ene vrste energije v drugo in vzpostavljeno je termodinamično ravnovesje. Oddelek za fiziko Posebej pomembni so tisti, ki se ukvarjajo s podrobno študijo transformacij, sprememb, ohranjanja energije. Na primer, v kemijski kinetiki je mogoče ne samo opisati stanje sistema, temveč tudi izračunati pogoje, ki vodijo do njegove premestitve v pravo smer.
Hessov zakon, ki povezuje entalpijo, entropijo obravnavane transformacije, omogoča identifikacijo možnosti spontane reakcije, da se izračuna količina toplote, ki jo sprosti (absorbira) termodinamični sistem.
Termokemija, ki temelji na temeljih termodinamike, je praktično pomembna. Zaradi tega področja kemije se pri proizvodnji izvajajo predhodni izračuni izkoristka goriva in izvedljivosti uvajanja določenih tehnologij v realno proizvodnjo. Podatki iz termodinamike omogočajo uporabo pojavov elastičnosti, termoelektričnosti, viskoznosti, magnetizacije za industrijsko proizvodnjo različnih materialov.