Aluminijev klorid v človeškem življenju
Ta članek se osredotoča na aluminijev klorid, snov, ki jo ljudje pogosto uporabljajo na številnih področjih svojega delovanja. Upoštevamo glavne kvalitativne značilnosti te spojine, metode njene proizvodnje in druge značilnosti.
Uvod v aluminijev klorid
Aluminijev klorid so aluminijeve soli in soli maslene kisline. Njegova kemijska formula je AlCl 3 . Postopek sublimacije se začne pri 183 ° C pod normalnim tlakom. Ko se tlak poveča, se postopek taljenja začne pri 192,6 ° C.
V vodi se ta spojina raztopi precej dobro - pri 25 ° C v sto gramih vode se raztopi v 44,38 g aluminijevega klorida. V zraku z visoko vlažnostjo začne kaditi zaradi reakcije hidrolize, ki sprošča HCl.
V vodnih raztopinah nastanejo beli kristalni hidrati z rumenim odtenkom. Aluminijev klorid je zelo topen v velikih količinah organskih spojin, kot so etanol, nitrobenzen, etilen glikol itd. Proces raztapljanja v raztopinah toluena in benzena praktično ni opazen.
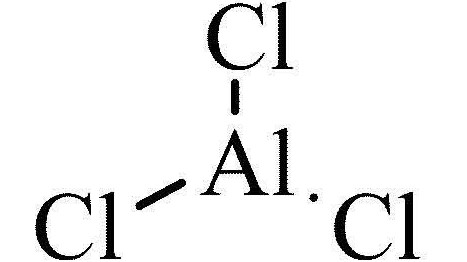
Načine, kako priti
Obstaja veliko načinov za pridobivanje AlCl 3 . Najpomembnejši med njimi je proces izpostavljanja Cl 2 in CO v gredni peči dehidriranemu boksitu ali kaolinu:
- Al203 + ZSO + 3Cl2 → 2AlCl3 + 3C02.
Druga pomembna metoda pridobivanja je interakcija borovega triklorida in aluminijevega fosfida pri temperaturi devetsto stopinj Celzija. Na izhodu iz te reakcije dobimo aluminijev klorid in borov fosfid:
- BCl3 + AlP → BP + AlCl3 .
Druge proizvodne metode vključujejo:
- Al + FeCl3 → AlCl3 + Fe;
- Al (OH) 3 + 3HCl → AlCl3 + 3H20;
- 3CuCl2 + 2Al → 2AlCl3 + 3Cu;
- 2Al + 6HCl → 2AlCl3 + 3H2.
Področja uporabe
Brezvodni AlCl 3 se uporablja v industriji, najpogosteje kot katalizator. S kombiniranjem z veliko količino anorganskih in organskih snovi lahko tvori različne izdelke. Pravzaprav je to osnova njegove glavne metode uporabe kot katalizatorja. Na primer, ko se olje razgradi v različne frakcije, uporabimo AlCl 3 kot destruktivni katalizator.

Uporaba alkilacije pri njegovi uporabi temelji na dejstvu, da se ogljikovodiki iz serije etilena začnejo polimerizirati in kondenzirati, pri čemer tvorijo kompleksnejše serije sistemov. Reakcija aciliranja in proces izomerizacije parafinskih ogljikovodikov se lahko pojavita tudi pod vplivom aluminijevega klorida kot katalizatorja v kemijski interakciji snovi.
Kozmetika in aluminijev klorid heksahidrat
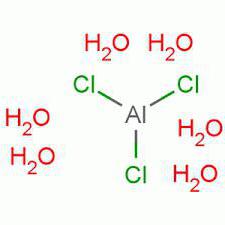
Heksahidrat je derivat aluminijevega klorida s kemijsko formulo - AlCl 3 -6H 2 O. Široko se uporablja v kozmetični industriji, vendar je zelo nevarna snov. Mimogrede, to je ena od mnogih pogosto uporabljenih komponent v proizvodnji deodorantov proti potenju. To je posledica dejstva, da je ta snov precej poceni, poleg tega pa resnično odlično opravlja vlogo borca s človeškim potenjem.

Številni regulatorji pogosto napadajo heksahidrat aluminijevega klorida, saj se šteje, da je to zelo strupena sestavina. In to je v resnici tako, a ker je zelo učinkovito, je v večini primerov zaprto za svojo pomanjkljivost. Znatno število študij in poskusov potrjuje učinkovitost spojine v boju proti potenju.
Največja koncentracija te snovi v proizvodnji izdelkov se še vedno preučuje, saj točen vzrok za izrazito sposobnost zmanjševanja znojenja še ni jasen. Če poskušate opisati njeno lastnost v smislu fizičnega učinka, AlCl 3 -6H 2 O tvori netopne kovinske spojine, ki blokirajo znojne kanale in tako nekaj časa preprečujejo znojenje.
Aluminijev klorid heksahidrat je ena od sestavin široke palete potrošniškega blaga. Najpogosteje ga najdemo v deodorantih, kot tudi zobne paste, šminke in koloidne barve.
Pri zobni pasti in šminki je količina AlCl 3 -6H 2 O običajno minimalna, v mejah od stotinke do deset, pri barvah pa 18%.
Kaj je etiaxil heksahidrat
Aluminijev klorid etiaxil heksahidrat je eno najpomembnejših orodij v boju proti hiperhidrozi (povečano potenje) pod pazduho. Ta težava se lahko pojavi pri mnogih ljudeh, še posebej pri najbolj občutljivem občutku udobja. In to je lahko posledica številnih razlogov:
- motnje v hormonskem sistemu;
- njeno prestrukturiranje;
- toplota na ulici;
- različne vrste bolezni;
- motnje v delovanju živčnega sistema itd.
Ta spojina je odlična pri reševanju težav prekomernega potenja in je zelo učinkovita snov. Priporočljivo je, da ga nanesete na suho in ne-razdraženo kožo, pred spanjem pa jo sperite z milom. Če se na mestu uporabe pojavi draženje, je treba uporabiti kortikoidne mazila. Dovolj je dvakrat nanesti aluminijev klorid heksahidrat, kar bo dalo zelo dobre rezultate, potem pa bo dovolj, da ga uporabimo približno enkrat na teden.
Aluminijev klorid heksahidrat je v obliki kristalov, ki nimajo barve, zlahka topen v raztopinah alkohola, vode, etrov in glicerina. Spojina je zelo higroskopična, zato jo je treba skladiščiti v suhih prostorih, brez dostopa vlage.
Zaključek
Upamo, da vam je naš članek pomagal razumeti, kaj je aluminijev klorid. Zdaj lahko navedete izčrpen opis, navedite načine pridobivanja v industriji in obseg uporabe te snovi. Z uporabo AlCl 3 in AlCl 3 -6H 2 O je pomembno vedeti, da te spojine spadajo med številne strupene snovi in zato morate biti pri njihovi uporabi previdni.