Nasičeni ogljikovodiki: lastnosti in uporaba
Najprej upoštevamo mejne ogljikovodike, zlasti njihovo strukturo, lastnosti, aplikacije.
Splošne informacije o alkanih
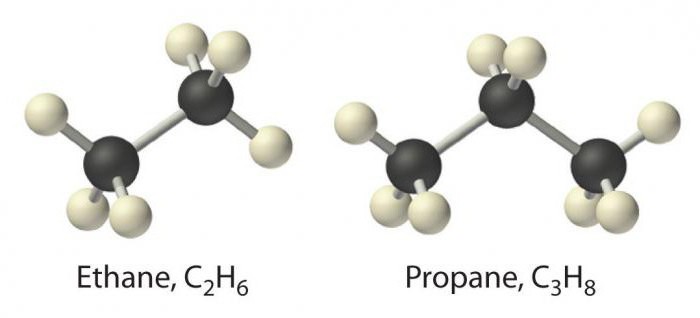
Ta razred vključuje spojine, ki ustrezajo splošni formuli CnH2n + 2. Njihove molekule so linearne, za njih je značilna le preprosta vez.
Mejne ogljikovodike predstavlja homologna serija metana. Med atomi ogljika v molekulah sp3 hibridizacija, za katero je značilen kot 109 stopinj.
Biti v naravi
Mejni ogljikovodiki so v naravi široko porazdeljeni. Na primer, metan, glava tega razreda ShNu, nastane z razgradnjo živalskih in rastlinskih organizmov na močvirnih območjih (brez dostopa do zraka).
Poleg tega je ta spojina prisotna v rudnikih premoga, kar pogosto vodi do resnih eksplozij in smrti rudarjev.
Mejni ogljikovodiki v velikih količinah so v trdni, tekoči in plinasti obliki v olju. Poleg metana olje vsebuje tudi propan, etan, butan in pentan.
Fizikalne lastnosti alkanov
Te snovi so v vodi slabo topne. Najnižji člani serije so plini. S povečanjem relativne molekulske mase spojin opazimo povečanje vrelišča in tališča, pride do prehoda iz plinastega stanja v tekočine.

Kemijske lastnosti
Upoštevajte osnovne kemijske lastnosti nasičenih ogljikovodikov. Zaradi nizke polarnosti C-C vezi so kemično neaktivne spojine.
Med značilnimi lastnostmi predstavnikov tega razreda opažamo radikalno halogeniranje. Kot posledica interakcije v prvi fazi nastane monohalogeno spojina in vodikov halid. Glede na to, da ima reakcija verižni mehanizem, se nadomeščanje nadaljuje, dokler se ne pojavijo atomi halogena namesto vodikov.
Poleg halogenacije so prisotni tudi nasičeni ogljikovodiki dušikove kisline. Nitracija vodi do tvorbe nitroalkanov.
Sulfuracija je povezana z substitucijo vodikovega atoma s sulfo skupino, med produkti reakcije bo alkansulfonska kislina in voda. Postopek izvedemo z rahlim segrevanjem reakcijske zmesi, žveplove kisline v koncentrirani obliki.
V normalnih pogojih imajo alkani odpornost na tako močna oksidacijska sredstva kot kalijev permanganat, kalijev dikromat.
Ko se temperatura dvigne, se opazuje njihovo oksidacijo s kisikom v zraku ogljikov monoksid (4) in vodne pare.
Nepopolna (katalitska) oksidacija vodi do tvorbe ketonov, aldehidov, karboksilnih kislin.
Ob prekinitvi C-C vezi nastane razpoka, zaradi česar so spojine z manjšim številom ogljikovih atomov oblikovane iz dolge ogljikove verige.
Med produkti dehidrogenacije nenasičenih ogljikovodikov in molekul vodika pride do reakcije pri visokih temperaturah.
Med dehidrociklizacijo nastanejo aromatski ogljikovodiki, ki imajo praktično uporabo.
Nenasičena ShNu
Mejni in nenasičeni ogljikovodiki imajo lahko ciklično ali alifatsko strukturo. Na primer, alken, ki imajo splošno formulo CnH2n, se razlikujejo po prisotnosti dvojnih vezi med ogljikovimi atomi.
Zato za predstavnike serije etilenskih karakterističnih reakcij dodamo dvojno vez. Hidrohalogeniranje in hidracija poteka za asimetrične alkene po Markovnikovem pravilu. Njegovo bistvo je, da pri spajanju z dvojno vezjo vodikovega halogenida ali vode, so atomi halogenov ali hidrokso skupine vezani na ogljik, ki ima manjše število H, in vodik gre na prvi atom C.
Poleg tega za predstavnike tega razreda organske spojine značilna reakcija polimerizacije. Našli so široko uporabo v sodobni kemični industriji. Na primer, za proizvodnjo polietilena, ki je povpraševanje v kmetijstvu, medicina, je etilen vzet kot začetni monomer. Med postopkom katalitične polimerizacije se dvojna vez razpade in sčasoma tvori polimerno spojino.
Kvalitativna reakcija nedoločenost (prisotnost dvojnih in trojnih vezi v molekulah) je beljenje bromove (jodove) vode, kakor tudi beljenje raztopine kalijevega permanganata.
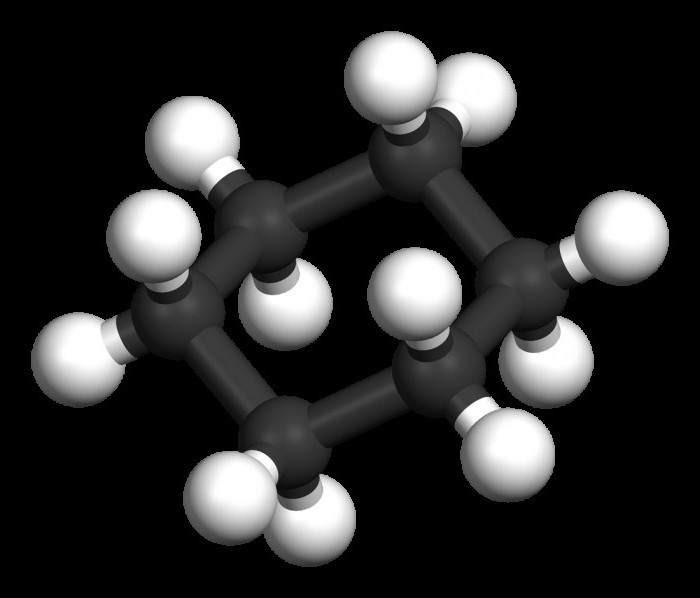
Med cikličnimi ogljikovodiki, ki se sedaj pogosto uporabljajo, je treba navesti benzen in toluen. Ti ShNu so značilni predstavniki številnih aromatskih ogljikovodikov, ki imajo splošno formulo CnH2n-6.
Benzen, v katerem je elektronska gostota enakomerno porazdeljena, velja za nizko aktivno spojino. Toluen, ki se uporablja za industrijsko proizvodnjo benzojske kisline, ki je odličen konzervans, ima večjo reaktivnost.

Zaključek
V organski kemiji se razlikuje več razredov ogljikovodikov, ki se razlikujejo v razporeditvi ogljikovih atomov in prisotnosti enojnih in dvojnih (trojnih) vezi. Kljub precejšnjim razlikam v strukturi, fizikalnih in kemijskih lastnostih so vse v povpraševanju v različnih panogah. Med nasičenimi ogljikovodiki je še posebej zanimiv metan in njegovi najbližji homologi.
Med dienskimi spojinami so vodilni kazalci v proizvodnji polimernih materialov 1,3-butadien in 2-metilbutadien-1,3. Posebej zanimivi so aromatski ogljikovodiki. So osnova za proizvodnjo organskih barvil, konzervansov.