Beljakovine: monomer, struktura in funkcija
Beljakovine so organske spojine z visoko molekulsko maso. Sestavljeni so iz aminokislinskih ostankov. Vključujejo tudi druge snovi: žveplo, kisik, dušik, vodik in ogljik. Nekatere beljakovine lahko tvorijo komplekse z molekulami, če vsebujejo cink, baker, železo in fosfor. Proteini imajo visoko molekulsko maso, zato se imenujejo makromolekule. Na primer, v jajčnih albumin - 36 tisoč, in hemoglobina (beljakovine v krvi) - 152 tisoč, in miozin ima molekulsko maso 500 tisoč. Primerjaj: molekulska masa benzena je 78, ocetna kislina pa 60.
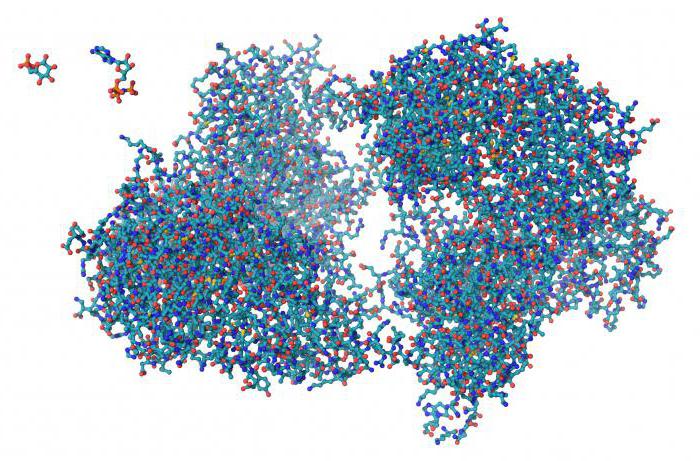
Struktura
Pogosto, zlasti med šolarji, lahko naletimo na trditev, da so proteinski monomeri nukleotidi. To je napačno prepričanje. Beljakovine ali beljakovine, ki so najbolj razširjene in številne organske spojine, so polimeri, ki so raznoliki in potrebni za delovanje telesa. Od 50 do 80% suhe mase celice pade na beljakovino. Monomeri, oziroma njihovo število in zaporedje, razlikujejo proteine drug od drugega.
Beljakovine so neperiodični polimeri, za njihovo delovanje je pomembna prisotnost več snovi. V splošni formuli morata biti prisotna karboksilna skupina (-COOH), amino skupina (-NH2) in radikal ali R-skupina (to je preostali del molekule), karboksilna in amino skupina. Kaj vsebuje protein? Njeni monomeri so aminokisline, in čeprav celice in tkiva vsebujejo več kot sto do sedemdeset vrst aminokislin, biologi kot monomere vključujejo le dva ducata vrst.
Obstaja razvrstitev aminokislin, po kateri so razdeljene v dve skupini, odvisno od tega, ali jih lahko sintetizirajo živali in ljudje. Organizem lahko proizvaja zamenljive aminokisline samostojno, vendar ga je mogoče pridobiti nenadomestljivo le od zunaj - s hrano, toda rastline jih lahko sintetizirajo vse.
Razvrstitev
Sami proteini so razvrščeni glede na aminokislinsko sestavo. Lahko so popolne, če vsebujejo celoten sklop aminokislin in imajo okvaro, če manjka ena ali več aminokislin. Če je protein sestavljen samo iz aminokislin, se imenuje preprosta. V primeru, da je prisotna protetična skupina, imenovana tudi ne-aminokislinska komponenta, se imenuje kompleksna. Skupino, ki ni aminokisline, lahko predstavimo kot metaloproteine, ogljikove hidrate (glikoproteine), lipide (lipoproteine) in nukleinske kisline (nukleoproteini).
Osnovni del
Sami aminokisline so sestavljene iz treh bistvenih delov. Tako lahko rečemo, da je proteinski monomer radikal, ki razlikuje med tipi aminokislin, pa tudi nespremenjenimi karboksilnimi in amino skupinami. Po številu sestavin karboksilne in amino skupine se aminokisline delijo na nevtralne, bazične in kisle. Nevtralne imajo eno karboksilno in eno amino skupino. Osnovna formula vsebuje več kot eno amino skupino, v kislih aminokislinah pa je več kot ena karboksilna skupina.
Aminokisline - beljakovinski monomeri - so amfoterne spojine, saj lahko zaradi prisotnosti karbonskih aminokislin v raztopini delujejo kot baze in kot kisline. V vodni raztopini so predstavljene kot ionske oblike.
Peptidna vez
Polipeptid - kot znanstveniki imenujejo protein: njegov monomer je vezan na lastno vrsto s peptidnimi vezmi. Peptidi so produkt reakcije kondenzacije aminokislin. Za interakcijo karboksilne in amino skupine dveh aminokislin je značilna tvorba kovalentne vezi dušik-ogljik, ki se imenuje peptid. Peptide razvrstimo glede na število aminokislinskih ostankov v svoji sestavi: dipeptide, tripeptide, tetrapeptide in tako naprej. S ponavljajočim se ponavljanjem tvorbe kovalentne vezi dušik-ogljik tvorijo polipeptidi. En konec peptida vsebuje prosto amino skupino in se imenuje N-terminus, druga je prosta karboksilna skupina in se imenuje C-terminal.

Druga razvrstitev
Kot je navedeno zgoraj, so proteinski monomeri sestavljeni iz amino in karboksilnih skupin in radikala, ki tvorijo močne vezi med seboj. Lahko so prisotne tudi druge snovi, vendar so lastnosti celotne molekule odvisne od skupine R in obstaja druga vrsta razvrstitve. Katero Za monomerni protein je običajno, da ima različne radikale, glede na njihovo vrsto in vse aminokisline lahko razdelimo na heterociklične, aromatske in alifatske. Alifatski radikal lahko vsebuje funkcionalne skupine, ki dajejo posebne lastnosti. To so amino, karboksilna, tiolna (-SH), hidroksilna (-OH), amidna (-C0-NH2) in gvanidinska skupina.
Različni radikali
Monomer proteinske molekule, ki vsebuje amino skupino, je aminokislinski prolin. Heterociklični radikali so vsebovani v triptofanu in histidinu. Aromatski radikal je prisoten v fenilalaninu in tirozinu. Dodatna hidroksilna skupina je v serinu in treoninu; karboksil - v aspartiku in glutaminska kislina. Druga amidna skupina v radikalu je v asparaginu in glutaminu (ne smemo zamenjati s kislinami). Dodatna amino skupina je v lizinu in gvanidin - v argininu. Žveplo je prisotno v radikalih cisteina in metionina.
Organizacija proteinskih molekul v prostoru
Vsak protein ima specifične funkcije, ki so odvisne od prostorske organizacije molekul. Poleg tega je podpora beljakovin v obliki verige, to je v razširjeni obliki, energetsko neugodna za celico, zato so, tako kot molekule DNK, polipeptidne verige zgoščene, s čimer pridobijo konformacijo - tridimenzionalno strukturo.
Prostorska organizacija proteinskih molekul ima štiri ravni.
Ker so monomeri proteinskih molekul aminokisline, je primarna struktura predstavljena kot polipeptidna veriga, ki sestoji iz aminokislinskih ostankov, ki so povezani s peptidno vezjo. Kljub navidezni enostavnosti je primarna struktura tista, ki določa, kakšno funkcijo lahko izvaja beljakovina. Monomer v verigi mora biti na mestu, zamenjava celo enega izmed njih pa bo spremenila namen celotne molekule. Na primer, če je šesti glutaminska kislina v hemoglobinu nadomeščena z valinom, bo celotna molekula prenehala delovati in prenos kisika bo moten. Takšna nadomestitev vodi do razvoja človeške anemije srpastih celic.
Če sestava poliproteina vsebuje deset aminokislinskih ostankov, potem bo veliko variacij izmenjav monomerov - 1020, če je prisotnih vseh 20, bodo kombinacije, ki jih je mogoče sestaviti, še večje. Človeško telo sintetizira več kot deset tisoč proteinov, ki se razlikujejo ne samo v primerjavi med seboj, ampak tudi z beljakovinami drugih živih organizmov.
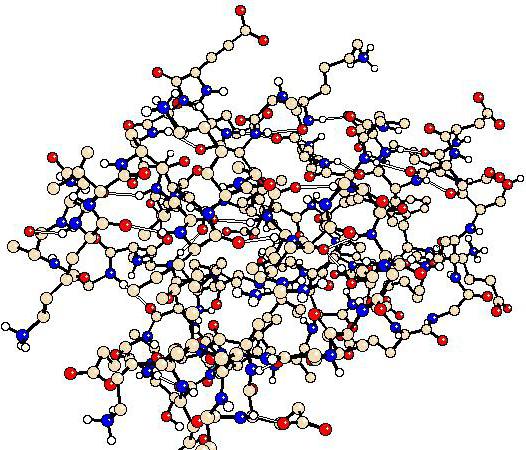
Za sekundarno strukturo je značilno pravilno zlaganje verige v spiralo, ki je podobna raztegnjeni vzmeti. Povezave med beljakovinskimi monomeri so vodik in krepijo strukturo. Te vezi se pojavijo med amino in karboksilnimi skupinami. Vodikove vezi so šibkejše od peptidnih vezi, vendar pa celotna konfiguracija zaradi večkratnih ponovitev postane bolj tog in stabilen. Za nekatere beljakovine, kot so fibroin (pajčevina, svila), keratin (nohti in lase) in kolagen, ne pride do nadaljnjega zbijanja.
Tretja raven
Na naslednjem nivoju so polipeptidne verige zložene v globule, ki nastanejo zaradi namestitve novih kemijskih vezi - disulfida, ionskega, vodika. Pomemben dejavnik je tudi vgradnja hidrofobne interakcije med R-skupinami aminokislinskih ostankov, in sicer hidrofilno-hidrofobne interakcije igrajo glavno vlogo pri oblikovanju terciarne strukture proteinske molekule.
Ko se vbrizgajo v vodno raztopino, poskušajo hidrofobni radikali pobegniti iz vode z združevanjem v globule, hidrofilne R-skupine pa medsebojno delujejo z vodnimi dipoli (hidracija), nasprotno pa se pojavijo na površini. Nekatere beljakovine imajo dodatno stabilizacijo terciarne strukture zaradi disulfidnih kovalentnih vezi, ki se pojavljajo med dvema cisteinskim ostankom zaradi prisotnosti atomov žvepla. Terciarna struktura se konča s kompaktiranjem protein-encimov, protiteles in določenih hormonov.

Kvartarna struktura
Slednja stopnja zbijanja je prisotna v kompleksnih beljakovinah, ki vsebujejo dve ali več globul. Zadrževanje podenot nastane zaradi ionskih, hidrofobnih in elektrostatičnih interakcij. Tudi tvorba disulfidnih vezi je možna. Kvartarna struktura ima protein hemoglobina, ki ga tvorita dve alfa podenoti, ki vsebujejo 141 aminokislinskih ostankov in beta podenote, ki vključujejo 146 ostankov. Vsaka podenota je povezana tudi z molekulo heme, ki vsebuje železo.
Lastnosti beljakovin
Ker je monomer beljakovinske molekule aminokislina, so od njih, skupaj s strukturno organizacijo, odvisne lastnosti. Proteini kažejo tako kisle kot osnovne lastnosti, ki jih določajo R-skupine aminokislin: če je v sestavi več bazičnih aminokislin, so osnovne lastnosti bolj izrazite. Lastnosti pufrov proteinov se določijo s sposobnostjo pripojitve in sproščanja protona (H +). Hemoglobin, ki ga vsebujejo rdeče krvne celice, je eden najmočnejših pufrov, poleg vezave kisika deluje tudi kot regulator pH-vrednosti krvi.
Obstajajo topne beljakovine, kot so fibrinogen, in netopne, ki opravljajo mehanske funkcije (npr. Kolagen, keratin, fibroin). Encimi so kemijsko aktivni proteini in v nasprotju z njimi obstajajo inertni polipeptidi. Razlikujemo tudi beljakovine, ki so odporne ali nestabilne na učinke zunanjih pogojev.
Denaturacija
Zunanji dejavniki, kot so ultravijolično sevanje, soli težkih kovin in same kovine, dehidracija, sevanje, segrevanje in spremembe pH, lahko povzročijo delno ali popolno uničenje strukturne organizacije proteinske molekule. Izguba tridimenzionalne strukture se imenuje denaturacija. Njegov vzrok je zlom vezav, ki je dal strukturo molekule stabilnost. Najprej se uničijo slabe vezi, nato pa v primeru še hujših pogojev raztrgajo tudi močni, zato se kvartarna struktura najprej zruši, šele nato - terciarna in sekundarna.
Ko se prostorska konfiguracija spremeni, beljakovina spremeni tudi njene lastnosti, zaradi česar ne more več opravljati svoje biološke naloge. Če denaturacija ni povzročila uničenja baze, primarne strukture, potem je reverzibilna in beljakovina bo sposobna izvesti postopek samozdravljenja - renaturacijo. V drugih primerih je denaturacija nepovratna.

Zaščita in presnova
Brez sodelovanja beljakovin v telesu se ne zgodi niti en sam proces. Njihova konstrukcijska funkcija je, da sodelujejo pri nastajanju zunajceličnih in celičnih struktur, prisotni so v sestavi celičnih membran, las, nohtov in kit. Opravljajo tudi transportno funkcijo: hemoglobin prenaša kisik in ogljikov dioksid, celični membranski proteini pa aktivno in selektivno izvajajo prenos potrebnih snovi v celico in iz nje v zunanje okolje.
Nekateri hormoni imajo beljakovinsko naravo in so vključeni v uredbo presnovo. Na primer, insulin uravnava glukozo v krvi in hkrati spodbuja tvorbo glikogena in optimizira sintezo maščob iz ogljikovih hidratov.
Zaščitna funkcijo beljakovin Sestavljen je iz tvorbe protiteles, če je telo napadeno s tujimi beljakovinami in mikroorganizmi. Protitelesa lahko najdejo in jih nevtralizirajo. Pri ranah in kosih iz fibrinogena nastane fibrin, ki pomaga ustaviti krvavitev.
Druge funkcije
Brez beljakovin je gibanje nemogoče: miozin in aktin sta kontraktilni proteini, zaradi katerih mišice delajo pri živalih.
Proteini vsebujejo tudi signalno funkcijo. V celične membrane vsebuje beljakovine, ki lahko spremenijo svojo terciarno strukturo glede na zunanje okolje. To je osnova za sprejem in prenos v celico signalov iz zunanjega okolja.
Niti ljudje niti živali ne morejo shranjevati beljakovin (izjema je kazeinsko mleko in albuminska jajca), vendar beljakovine prispevajo k kopičenju nekaterih snovi v telesu. Na primer, med razpadom hemoglobina, železo ne zapusti telesa, ampak tvori kompleks s feritinom. Razgradnja enega grama beljakovin daje telesu in 17,6 kJ energije, to je njihova energijska funkcija. Vendar pa praviloma organizem »skuša« ne porabiti tako pomembnega materiala za to, in najprej se maščobe in ogljikovi hidrati razgradijo.
Ena najpomembnejših funkcij je katalitična. Zagotavljajo ga encimi, ki lahko pospešijo biokemične reakcije v celicah.