Gorčični plin: ime, formula, značilnosti in zanimiva dejstva o snovi
Prvi kemični napad v zgodovini so 22. aprila 1915 izvedli nemški vojaki v bližini belgijskega mesta Ypres. V kakovosti strupene snovi Takrat je bil uporabljen klor, ki je postal prva vrsta kemičnega orožja. Prvi napad je sledil drugi, 31. maja istega leta, na vzhodni fronti, z uporabo fozgena. In 12. maja 1917, po več epizodah uspešne uporabe drugih strupenih snovi (agentov), je bil spet izveden kemijski napad v bližini Ypr - z gorčičnim plinom, pozneje imenovanim "gorčica" na bojišču.

Zgodovina
Domnevni gorčični plin se lahko šteje za Belgijo. Njen rojeni fizik Cesar Depre je prvič leta 1822 sintetiziral to snov. Prejel je gorčični plin, kadar je bil izpostavljen etilen žveplovemu kloridu (žveplov diklorid). Gorčico je dobil tudi Rich leta 1854 in Frederick Guthrie leta 1860 z istimi reagenti. Slednji je v svoji raziskavi že govoril o škodljivih učinkih plina.
Prvič je čisti gorčični plin pridobila nemški znanstvenik Viktor Meyer. Namesto neposredne sinteze je uporabil tiodiglikol in fosforjev triklorid. Meyer je podrobno opisal fizikalne in kemijske lastnosti te spojine.
Ad

Med prvo svetovno vojno in po njem sta Lommel in Steinkopf preučevala plin (takrat se je pojavilo prvotno ime te snovi, Lost). Zahvaljujoč njihovim raziskavam je Nemčija lahko uporabila Lost že leta 1917. Uporabljen postopek priprave je enak kot pri Meyerju, uporabili smo samo tionil klorid namesto ogljikovega triklorida.
Po plinskih napadih so države Antante spoznale učinkovitost gorčičnega plina in po določenem času začele s proizvodnjo.
V Nemčiji Guiller's je bila proizvodnja gorčičnega plina zelo pomembna: količina proizvedenega OM je bila izmerjena v več sto tisoč tonah. Uničenje po vojni je trajalo približno deset let.
Vrednost in koristi
Pred gorčičnim plinom so Nemci uporabljali strupeni klor in dušen fosgen / difosgen (kot tudi njihove mešanice v različnih razmerjih) - plinasto OM. Za njihovo učinkovitost so imeli tudi slabosti: odvisnost od meteoroloških razmer, težave pri dobavi in montaži plinskih jeklenk, slabo nadzorovan polmer škode. Z izumom strelnega orožja z agenti je bilo mogoče uporabiti strupene snovi v kakršnem koli agregatnem stanju: tekočem, trdnem, plinastem. Tu najdemo trdne spojine z arzenom. Vendar pa so države Antante hitro izboljšale plinske maske in ta sredstva so postala neučinkovita.
Ad

S prihodom gorčice se je začela nova faza razvoja organske snovi. Glavna značilnost izgubljenega plina je bila mehurjenje kože - razen dihal, je prizadelo tudi oči in telesa, prodrlo pod obleko in čevlje, medtem ko ni uporabljalo plinskih mask. Poleg tega je imel gorčični plin nizko hlapnost - dovolil je, da "ne okuži" žive sile, temveč celotne odseke terena.
Zaradi številnih prednosti pred drugimi prvimi generacijami kemičnih agensov je gorčični plin dolgo ostal "v uporabi", njegova proizvodnja v velikih količinah pa je potekala do sredine 20. stoletja.
Struktura
Sistematično ime gorčice je 2,2'-diklorodietilsulfid. V Angliji in Združenih državah Amerike se imenuje "gorčični plin" zaradi značilnega kavstičnega vonja česna. V Nemčiji je plin prejel kodna imena H (za tehnične), HS in pozneje HD - za destilirano snov.
Ad
Formula gorčičnega plina je relativno preprosta.
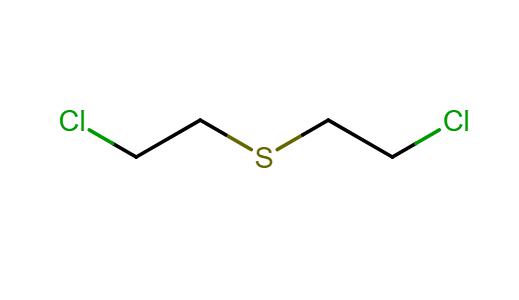
Fizične lastnosti
V normalnih pogojih (atmosferski tlak, temperatura 20 ° C) je gorčični plin hlapna oljna tekočina. Značilni vonj in rumenkasta barva dajejo nečistoče. Ne raztopi se v vodi, ampak hidrolizira (razpade), da nastane tiodiglikol. Omejeno je v alkoholu, v organskih topilih - eter, benzen, kloroform, živalska in rastlinska olja - zelo dobro. Prav tako je zelo topen v drugih kemičnih sredstvih, kar vam omogoča, da ustvarite mešanice več snovi.
Kemijske lastnosti in nevtralizacija
Čeprav je bilo v članku že omenjeno, da se v vodi hidrolizira strupeni gorčični plin, je bilo v praksi pogosto opaženo naslednje: gorčica, ki je bila nekaj let shranjena v neugodnih razmerah, v mokrih prostorih ali v poškodovanih cilindrih, je izgubila malo svoje dejavnosti. To ne ustreza laboratorijskim podatkom: če je snov hidrolizirana, preneha obstajati v svoji prvotni molekularni (za plin) obliki in izgubi svoje lastnosti. To protislovje je mogoče pojasniti z dejstvom, da voda in gorčični plin nista mešljivi tekočini: v laboratoriju med hidrolizo poteka intenzivno mešanje, reakcija gre skozi celoten volumen, v poljskih pogojih pa voda zajame gorčični plin s plastjo, reakcija pa poteka samo na vmesniku dveh medijev, in to je zelo počasno in reverzibilno.
Ad
Za razplinjevanje (nevtralizacija) gorčice v velikih količinah belila, je v skupnem "belilu" posebnega pomena. Nanesite ga v obliki koncentrirane vodne raztopine, v kateri so okuženi predmeti namočeni, temeljito premešajte. Hipokloriti so ekonomsko najugodnejši: poceni so in se proizvajajo v velikih količinah.

V zadnjih desetletjih so kloramini postali pomembni za odplinjevanje strupenega gorčičnega plina. Kloramin T je eden najpomembnejših v praktični uporabi, v primerjavi s kompleksnim učinkom belila na gorčico pa je reakcija z natrijevo soljo kloramina T preprosta: žveplo v diklorodietil sulfidu oksidira in nastaja produkt dodajanja kloramina. Na osnovi kloramina T v ZDA je nastala zmes, ki je primerna za razplinjevanje tudi instrumentov in avtomobilov.
Preostale zmesi za odplinjevanje, čeprav so lahko učinkovitejše, imajo v praksi le omejeno uporabo zaradi visokih stroškov surovin in proizvodne kompleksnosti.
Ena od kvalitativnih reakcij, ki omogočajo zaznavanje 10 mg gorčičnega plina v 1000 litrih zraka, je reakcija z zlatim (II) kloridom, za katerega je značilna pojava rumenkaste oborine v raztopini klorida in pri visokih koncentracijah gorčičnega plina, rdečkasto rumene oljne kapljice.
Pridobivanje
Obstajajo trije glavni načini za proizvodnjo gorčičnega plina v laboratoriju in v industrijskem obsegu.
Prvi je reakcija etilena z žveplovim dikloridom. To metodo je razvil Guthrie.
Drugo metodo je odkril Meyer in je vključevala delovanje na tiodiglikol s klorirnimi sredstvi: fosforjev klorid, hidroklorid, tionil klorid.
Tretjo metodo je leta 1942 razvil Lazier v ZDA. Temelji na interakciji vodikovega sulfida z vinilkloridom v prisotnosti organskih peroksidov kot katalizatorjev. Donos produkta lahko doseže 75% - to je visoka vrednost za organsko sintezo.
Ad
Ukrepanje na telesu
Gorčični plin je strupeno in mehurasto zastrupitveno sredstvo. Deluje na vse dele telesa, zato je za zaščito pred njim potrebna posebna oblačila, ki pokrivajo celotno površino telesa.
Gorčica mora imeti latentno obdobje delovanja, to je takoj po stiku s kožo, ne bo simptomov in šele po 2-6 urah se pojavi rdečina, vnetje - povrhnjica je zavrnjena. Epidermis ugasne in na njegovem mestu se pojavijo gnojilo in razjede, ki zahtevajo dolgotrajno zdravljenje. Če takšnega zdravljenja ni, se smrt zgodi med več urami in enim mesecem (odvisno od odmerka učinkovin).
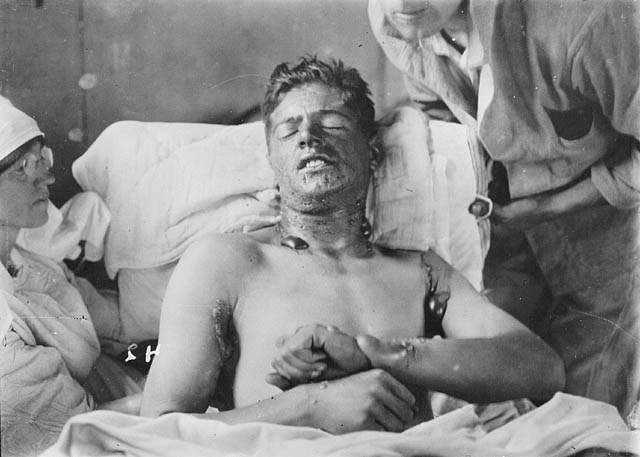
Ko gorčični plin pride v stik z očmi, se začne vnetje sprednjega dela očesa, zlasti roženice (zaradi zamuljenja je možna tudi izguba vida). Nato se razvijejo gnojni konjunktivitis in nekroza tkiva, ki zahteva dolgotrajno zdravljenje.

Vpliv gorčice na dihalni sistem je lokaliziran v zgornjem dihalnem sistemu. Pojavijo se notranje krvavitve, pojavijo se gnojne in gangrenske žarnice, pri visokih koncentracijah se lahko razvije pljučni edem.
Splošni zastrupitveni učinek gorčice je posledica dejstva, da ne vpliva samo na prizadeta območja, ampak se absorbira tudi v krvni obtok in se širi po vsem telesu, kar se kaže v motnjah cirkulacije, toksičnih ledvičnih, prebavnih in možganskih krvavitvah.
Spremembe na osnovi gorčice
Znano je, da so se pred drugo svetovno vojno in v njem z vojaškimi kemijskimi laboratoriji v ZDA in Angliji ukvarjali z Levinsteinom yperitom, mešanico navadnega gorčičnega plina s polisulfidi, katerih struktura je vsebovala dolge verige atomov žvepla. Težko je oceniti vojaški pomen te snovi.
Po prvi svetovni vojni je že omenjeni Steinkopf pridobil dibrom- in dijodo-dietilsulfide (tako imenovani izgubljeni brom in jod). Niso deležni široke uporabe, saj ustrezajo konvencionalnemu gorčičnemu plinu z vidika učinkovitosti in so veliko dražji v proizvodnji.