Izotopi so ... radioaktivni izotopi, njihov razpad in razpolovni čas
Verjetno ne na zemlji taka oseba, ki ne bi slišala o izotopih. Ampak ne vsi vedo, kaj je to. Izraz »radioaktivni izotopi« zveni posebej zastrašujoče. Ti nerazumljivi kemijski elementi prestrašijo človeštvo, vendar v resnici niso tako grozni, kot se zdi na prvi pogled.
Opredelitev
Razumeti koncept radioaktivnih elementov najprej je treba povedati, da so izotopi vzorci istega kemičnega elementa, vendar z različno maso. Kaj to pomeni? Vprašanja bodo izginila, če se najprej spomnimo strukturo atoma. Sestavljen je iz elektronov, protonov in nevtronov. Število prvih dveh osnovnih delcev v jedru atoma je vedno konstantno, medtem ko se lahko nevtroni, ki imajo svojo lastno maso, pojavijo v isti snovi v različnih količinah. Ta okoliščina ustvarja različne kemijske elemente z različnimi fizikalnimi lastnostmi. 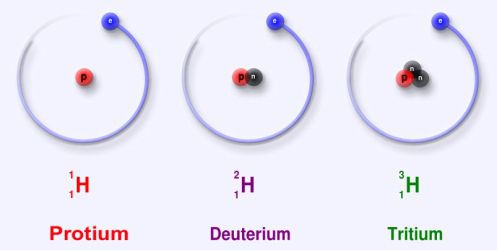
Zdaj lahko podamo znanstveno definicijo obravnavanega koncepta. Izotopi so torej kumulativni sklop kemičnih elementov s podobnimi lastnostmi, vendar z različnimi masnimi in fizikalnimi lastnostmi. Po sodobnejši terminologiji se imenujejo pleiad nukleotidov kemičnega elementa.
Ad
Malo zgodovine
V začetku prejšnjega stoletja so znanstveniki odkrili, da lahko ista kemična spojina pod različnimi pogoji pokaže različne mase elektronskih jeder. S čisto teoretičnega vidika bi se takšni elementi lahko šteli za nove in začeli z njimi zapolniti prazne celice v periodnem sistemu D. Mendelejeva. Vendar je v njej le devet prostih celic in znanstveniki so odkrili na desetine novih elementov. Poleg tega so matematični izračuni pokazali, da zaznanih spojin ni mogoče šteti za prej neznane, ker so njihove kemijske lastnosti v celoti ustrezale značilnostim obstoječih.
Po dolgotrajnih razpravah so se odločili, da te elemente imenujemo izotope in jih postavimo v isto celico kot tiste, katerih jedra vsebujejo enako število elektronov z njimi. Znanstveniki so uspeli ugotoviti, da so izotopi le nekatere variacije kemijskih elementov. Vendar pa so njihove vzroke in dolgoživost preučevali že skoraj stoletje. Že na začetku 21. stoletja je nemogoče trditi, da človeštvo popolnoma pozna vse izotope.
Ad
Vztrajne in nestabilne variacije
Vsak kemični element ima več izotopov. Ker v svojih jedrih obstajajo prosti nevtroni, ne vstopajo vedno v stabilne vezi z drugimi komponentami atoma. Po določenem času prosti delci zapustijo jedro, zaradi česar se njegova masa in fizikalne lastnosti spremenijo. Tako nastanejo drugi izotopi, ki sčasoma vodijo v tvorbo snovi z enakim številom protonov, nevtronov in elektronov.
Te snovi, ki se zelo hitro razgradijo, se imenujejo radioaktivni izotopi. V prostor sproščajo veliko število nevtronov, ki tvorijo močno ionizirajoče gama sevanje, znano po svoji močni prodorni moči, ki negativno vpliva na žive organizme.
Ad
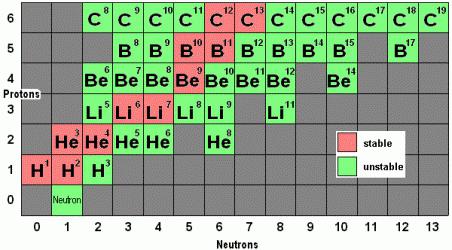
Stabilnejši izotopi niso radioaktivni, saj količina prostih nevtronov, ki jih oddajajo, ni sposobna generirati sevanja in bistveno vpliva na druge atome.
Znanstveniki že dolgo časa vzpostavljajo en pomemben vzorec: vsak kemijski element ima svoje izotope, obstojne ali radioaktivne. Zanimivo je, da jih je bilo veliko pridobljenih v laboratoriju, njihova prisotnost v naravni obliki pa je majhna in ni vedno določena z instrumenti.
Širjenje v naravi
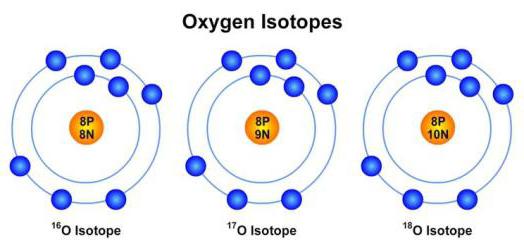
V naravnih pogojih so najpogosteje prisotne snovi, katerih masa izotopa je neposredno določena z njegovo vrstno številko v tabeli D. Mendelejeva. Na primer, vodik, označen s simbolom H, ima zaporedno številko 1 in njegova masa je enaka eni. Njegovi izotopi, 2H in 3H, so v naravi izjemno redki.
Tudi človeško telo ima določeno količino radioaktivnih izotopov. Skozi hrano vstopajo v obliki izotopov ogljika, ki jih rastline absorbirajo iz zemlje ali zraka in postanejo del organske snovi v procesu fotosinteze. Zato človek, živali in rastline oddajajo določeno sevanje. Samo on je tako nizek, da ne moti normalnega delovanja in rasti.
Viri, ki prispevajo k nastajanju izotopov, so notranje plasti Zemljinega jedra in sevanje iz vesolja.
Kot veste, je temperatura na planetu odvisna predvsem od njenega vročega jedra. Šele pred kratkim je postalo jasno, da je vir te toplote zapletena termonuklearna reakcija, v katero so vključeni radioaktivni izotopi.
Ad
Razpad izotopov
Ker so izotopi nestabilne formacije, lahko predpostavimo, da se sčasoma razpadejo v trajnejše jedre kemijskih elementov. Ta trditev je resnična, ker znanstveniki v naravi niso mogli zaznati velike količine radioaktivnih izotopov. Da, in večina tistih, ki so jih kopali v laboratorijih, je obstajala nekaj minut do nekaj dni, nato pa so se spet spremenili v običajne kemične elemente.
Toda v naravi so tudi izotopi, ki so zelo odporni na propad. Obstajajo lahko milijarde let. Takšni elementi so nastajali v tistih daljnih časih, ko se je zemlja še oblikovala in celo trdna skorja ni bila na njeni površini.
Radioaktivni izotopi se zelo hitro razpadajo in ponovno oblikujejo. Da bi olajšali oceno odpornosti izotopa, so se znanstveniki odločili, da preučijo kategorijo njegove razpolovne dobe.
Half life
Vsi bralci ne morejo takoj razumeti, kaj pomeni ta koncept. Definiramo ga. Razpolovna doba izotopa je čas, ko preneha obstajati pogojna polovica odvzete snovi.

To ne pomeni, da bo preostala povezava uničena v enakem času. Glede na to polovico je treba upoštevati drugo kategorijo - časovno obdobje, v katerem bo izginil drugi del, tj. Četrtina začetne količine snovi. In to razmišljanje se nadaljuje neomejeno. Domnevamo lahko, da je čas popolnega razpada začetne količine snovi nemogoče šteti, saj je ta proces skoraj neskončen.
Ad
Vendar pa lahko znanstveniki, ki poznajo razpolovno dobo, določijo, koliko snovi je obstajalo na začetku. Ti podatki se uspešno uporabljajo v sorodnih znanostih.
V sodobnem znanstvenem svetu se koncept popolnega razpada praktično ne uporablja. V zvezi z vsakim izotopom je običajno navesti njegovo razpolovno dobo, ki se giblje od nekaj sekund do več milijard let. Nižje kot je razpolovna doba, več je sevanja od snovi in višja je radioaktivnost.
Mineralna utrdba
V nekaterih vejah znanosti in tehnologije je uporaba sorazmerno velike količine radioaktivnih snovi obvezna. Hkrati pa je v naravnih pogojih zelo malo takšnih spojin.
Znano je, da izotopi niso običajne variante kemijskih elementov. Njihovo število se meri z nekaj odstotki najbolj odporne sorte. Zato morajo znanstveniki umetno obogatiti fosilne materiale.
V letih raziskav je bilo ugotovljeno, da razpad izotopa spremlja verižna reakcija. Sproščeni nevtroni ene snovi začnejo vplivati na drugo. Posledica tega je, da se težka jedra razgradijo v lažja in dobijo nove kemijske elemente.

Ta pojav se imenuje verižna reakcija, zaradi katere je mogoče pridobiti bolj obstojne, a manj pogoste izotope, ki se kasneje uporabljajo v nacionalnem gospodarstvu.
Uporaba energije upadanja
Prav tako so znanstveniki ugotovili, da se med razpadom radioaktivnega izotopa sprosti ogromna količina proste energije. Njegovo količino običajno merimo s Curiejevo enoto, ki je enaka času cepljenja 1 g radona-222 na 1 sekundo. Višja kot je ta indikator, več energije se sprosti.
To je bil razlog za razvoj načinov uporabe proste energije. Torej so obstajali atomski reaktorji, v katere je postavljen radioaktivni izotop. Večina energije, ki jo sprosti, se zbira in pretvarja v elektriko. Na podlagi teh reaktorjev se gradijo jedrske elektrarne, ki zagotavljajo najcenejšo električno energijo. Zmanjšane verzije takšnih reaktorjev se postavijo na samovozne mehanizme. Glede na tveganje za nesreče so najpogosteje takšne naprave podmornice. V primeru izpada reaktorja bo število žrtev na podmornici lažje zmanjšati.

Druga zelo strašljiva možnost za uporabo energije iz razpolovnega časa so atomske bombe. Med drugo svetovno vojno so bili preizkušeni na človeštvu Japonska mesta Hirošima in Nagasaki. Posledice so bile zelo žalostne. Zato ima svet dogovor o neuporabi tega nevarnega orožja. V kraju z velikimi državami, ki se osredotočajo na militarizacijo, in danes še naprej raziskovamo v tej industriji. Poleg tega mnogi izmed njih skrivoma proizvajajo atomske bombe iz svetovne skupnosti, ki so tisočkrat nevarnejše od tistih, ki se uporabljajo na Japonskem.
Izotopi v medicini
Za miroljubne namene se je razpad radioaktivnih izotopov naučil uporabljati v medicini. Če usmerite sevanje na prizadeto območje telesa, lahko prekinete potek bolezni ali pomagate bolniku, da se popolnoma okreva.
Pogosteje pa se radioaktivni izotopi uporabljajo za diagnostiko. Dejstvo je, da je njihovo gibanje in narava grozda najlažje zabeležiti s sevanjem, ki ga proizvajajo. Tako se v človeško telo vbrizga določena nenevarna količina radioaktivne snovi, zdravniki pa z instrumenti opazujejo, kako in kje gre.
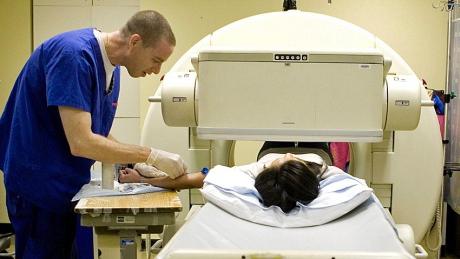
Tako je delo diagnosticirano možgani, naravo rakavih tumorjev, zlasti delovanje žlez notranjih in zunanjih izločkov.
Uporaba v arheologiji
Znano je, da v živih organizmih vedno obstaja radioaktivni ogljik-14, katerega razpolovni čas je 5570 let. Poleg tega znanstveniki vedo, koliko tega elementa vsebuje telo do smrti. To pomeni, da vsa rezana drevesa oddajajo enako količino sevanja. Sčasoma se intenzivnost sevanja zmanjša.
To pomaga arheologom ugotoviti, kako dolgo je drevo, iz katerega so zgradili kuhinjo ali katero koli drugo ladjo, in s tem čas gradnje, umrlo. Ta raziskovalna metoda se imenuje analiza radioaktivnega ogljika. Zahvaljujoč njemu so znanstveniki lažje vzpostavili kronologijo zgodovinskih dogodkov.