Izobarični proces, sorodne enačbe in izpeljava formule dela
Izobarični proces (imenovan tudi izobarični proces) je eden od termodinamičnih procesov, ki se pojavljajo pri indikatorju konstantnega tlaka. Masa plinskega sistema pa ostaja konstantna. Vizualni prikaz grafa, ki prikazuje izobarični proces, je podan s termodinamičnim diagramom v ustreznem koordinatnem sistemu.
Primeri
Najpreprostejši primer izobarnega procesa je segrevanje določene količine vode v odprti posodi. Kot drug primer lahko podamo razširitev idealnega plina v valjastem volumnu, kjer ima bat prosti tek. V vsakem od teh primerov bo pritisk konstanten. Je enak navadnemu atmosferskemu tlaku, kar je povsem očitno.
Ad
Reverzibilnost
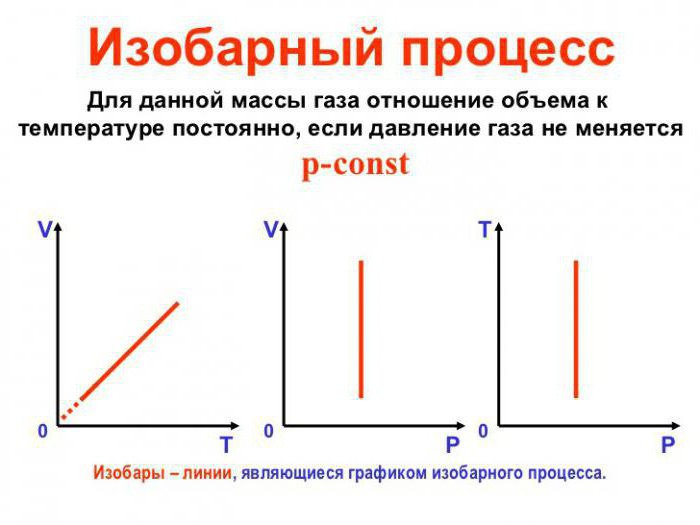
Izobarični proces lahko velja za reverzibilen, če tlak v sistemu sovpada z zunanjim tlakom in je enak na vseh točkah procesa (to je, je konstanten v vrednosti) in se temperatura zelo počasi spreminja. Tako se termodinamično ravnotežje v sistemu vzdržuje v vsakem trenutku. Kombinacija zgoraj navedenih dejavnikov nam daje možnost, da obravnavamo izobarični proces reverzibilen.
Da bi v sistemu izvedli izobarični postopek, mora biti toplota, ki jo je treba prenesti ali odstraniti. Hkrati pa je treba toploto porabiti za delo pri širjenju idealnega plina in njegovo spremembo. notranje energije. Formula, ki prikazuje medsebojno odvisnost količin med izobaričnim procesom, se imenuje Gay-Lussacov zakon. To kaže, da je volumen sorazmeren s temperaturo. Izvedimo to formulo, ki temelji na površnem znanju.
Ad
Sklenitev zakona Gay-Lussac (primarno razumevanje)
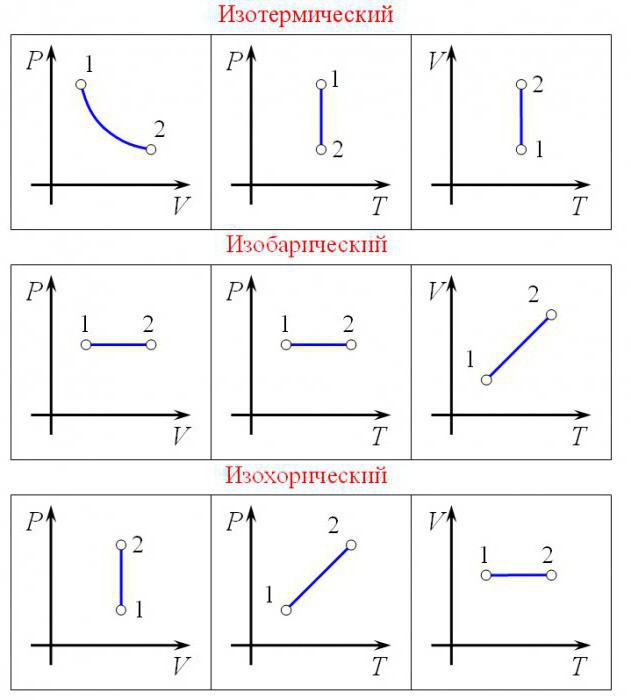
Oseba, vsaj malo poučena v molekularni fiziki, ve, da je veliko nalog povezanih z določenimi parametri. Njihovo ime je plinski tlak, količina plina in temperatura plina. V nekaterih primerih molekularna in molsko maso količino snovi, univerzalno plinsko konstanto in druge kazalnike. In obstaja jasna povezava. Spregovorimo o univerzalni plinski konstanti podrobneje. V primeru, da nekdo ne ve, kako ga dobiti.
Pridobitev univerzalne plinske konstante

Ta konstanta (konstantno število z določeno dimenzijo) se imenuje tudi Mendelejeva konstanta. Prisotna je tudi v enačbi Mendelejev-Clapeyron za idealen plin. Kako je naš slavni fizik dobil to konstanto?
Kot vemo, enačba idealnega plina ima naslednjo obliko: PV / T (ki je taka: »produkt tlaka in volumna deljena s temperaturo«). V zvezi z univerzalno plinsko konstanto, tako imenovano Avogadrov zakon. Pravi, da če vzamemo kateri koli plin, bo enako število molov pri enaki temperaturi in istem tlaku zasedlo enako količino.
Pravzaprav je to verbalna formulacija enačbe stanja idealnega plina, ki je bila napisana v obliki formule malo prej. Če vzamemo normalne pogoje (in to je, ko je temperatura plina 273,15 Kelvina, je tlak 1 atmosfera, oziroma 101325 paskalov, prostornina molov plina pa 22,4 litra) in jih nadomestimo v enačbo, pomnožimo in vse delimo, potem dobimo da nam kombinacija takih dejanj daje številčno vrednost, ki je enaka 8,31. Dimenzija je podana v džulih, ki jo delimo z zmnožkom na Kelvin (j / mol * k).
Ad
Mendelejev-Clapeyronova enačba
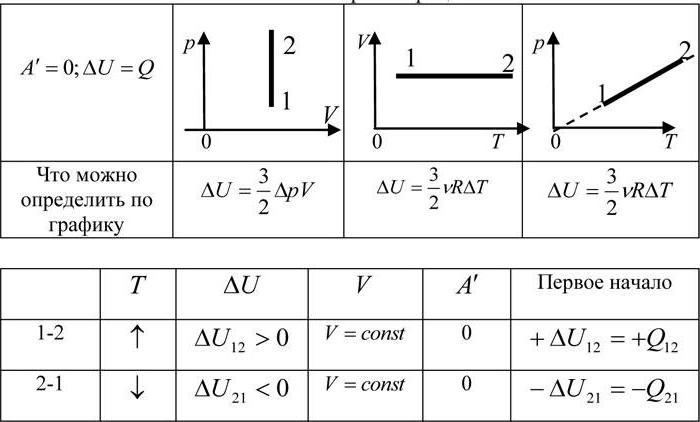
Vzemimo enačbo stanja idealnega plina in jo ponovno napišemo v novi obliki. Spomnimo, da ima prvotna enačba obliko PV / T = R. Zdaj pomnožimo oba dela s temperaturnim indeksom. Dobimo formulo PV (m) = RT. To pomeni, da je produkt tlaka po prostornini enak produktu univerzalne plinske konstante s temperaturo.
Zdaj pomnožite obe strani enačbe z enim ali drugim številom molov. Njihovo število označujemo s črko, npr. X. Tako dobimo naslednjo formulo: PV (m) X = XRT. Vemo pa, da produkt V z indeksom »m« povzroči le volumen V, število molov X pa se pokaže v obliki delitve določene mase z molsko maso, to je, da ima obliko m / M.
Tako bo končna formula izgledala takole: PV = MRT / m. To je ravno enačba Mendelejev-Clapeyrona, na katerega sta oba fizika prispela skoraj istočasno. Desno stran enačbe (in istočasno delimo) lahko pomnožimo s Avogadrojeva številka. Potem dobimo: PV = XN (a) RT / N (a). Toda zmnožek števila molov po Avogadrojevi številki, to je XN (a), nam ne daje nič več kot skupno število plinskih molekul, označenih s črko N.
Ad
Hkrati bo kvocient univerzalne plinske konstante in Avogadrojevega števila - R / N (a) dala Boltzmannovo konstanto (označeno s k). Zato dobimo še eno formulo, vendar v nekoliko drugačni obliki. Tukaj je: PV = NkT. Odprete lahko to formulo in dobite naslednji rezultat: NkT / V = P.
Obratovanje plina v izobaričnem procesu
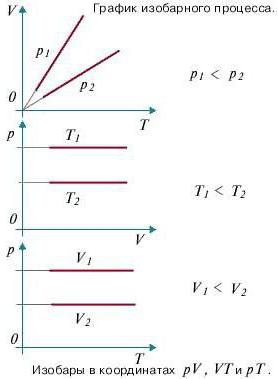
Kot smo ugotovili prej, je izobar proces termodinamični proces, v katerem tlak ostaja konstanten. Da bi ugotovili, kako se bo delo določilo med izobaričnim procesom, se bomo morali obrniti na prvi zakon termodinamike. Splošna formula je naslednja: dQ = dU + dA, kjer je dQ količina toplote, dU je sprememba notranje energije, dA pa delo, opravljeno med izvajanjem termodinamičnega procesa.
Še posebej upoštevajte izobarični proces. Upoštevajte faktor, da tlak ostane konstanten. Zdaj poskusite ponovno napisati prvi začetek termodinamike za izobarični proces: dQ = dU + pdV. Da bi dobili vizualno predstavitev procesa in dela, ga morate prikazati v koordinatnem sistemu. Naj bo abscisa os p, ordinata os V. Naj se volumen poveča. Na dveh točkah, ki se med seboj razlikujeta z ustrezno vrednostjo p (seveda, fiksno), upoštevajte stanja, ki predstavljajo V1 (začetni volumen) in V2 (končni volumen). Graf bo v tem primeru ravna črta, vzporedna z osjo x.
Iskanje dela je lažje kot kdajkoli prej. To bo preprosto območje slike, ki je na obeh straneh omejeno z projekcijami na absciso osi, na tretji strani pa je ravna črta, ki povezuje točke, ki ležijo na začetku in na koncu izobarične ravne črte. Poskusimo izračunati vrednost dela z uporabo integrala.
Ad
Izračuna se takole: A = p (integral med V1 in V2) dV. Odpiramo integral. Dosežemo, da bo delo enako zmnožku pritiska na razliko v volumnih. To pomeni, da bo formula izgledala takole: A = p (V2 - V1). Če odkrijemo nekaj količin, dobimo še eno formulo. Izgleda takole: A = xR (T2 - T2), kjer je x količina snovi.
Univerzalna plinska konstanta in njen pomen

Lahko rečemo, da bo zadnji izraz določil fizični pomen R - univerzalne plinske konstante. Da bi bilo bolj jasno, se obrnemo na določene številke. Za testiranje vzemite en mol snovi. Hkrati naj bo razlika v temperaturi 1 Kelvin. V tem primeru je enostavno videti, da bo delovanje plina enako univerzalni plinski konstanti (ali obratno).
Zaključek
To dejstvo lahko predstavimo v nekoliko drugačni luči, če parafraziramo besedilo. Na primer, univerzalna plinska konstanta bo numerično enaka delu, opravljenemu med izobarično ekspanzijo z enim molom idealnega plina, če se segreje z enim Kelvinom. Nekoliko težje bo izračunati delo z drugimi izoprocesi, a glavna stvar je uporabiti logiko. Potem bo vse hitro padlo na svoje mesto in izpeljava formule bo lažja, kot si misliš.