Kako narediti izomere: formule
Poskusite ugotoviti, kako narediti izomere. organske snovi. Na primer, vzemite nasičene in nenasičene ogljikovodike.
Opredelitev
Najprej ugotovite, kaj je izomerija. Glede na število ogljikovih atomov v molekuli je možno tvoriti spojine, ki se razlikujejo po strukturi, fizikalnih in kemijskih lastnostih. Izomerija je pojav, ki pojasnjuje raznolikost organskih snovi.
Izomerizem nasičenih ogljikovodikov
Kako narediti izomere, pokličite predstavnike tega razreda organske spojine? Za spopadanje z nalogo, za začetek izberemo posebne značilnosti tega razreda snovi. Nasičeni ogljikovodiki imajo splošno formulo SpN2n + 2, v molekulah so prisotne le preproste (posamezne) vezi. Izomerija za predstavnike številnih metanov kaže na obstoj različnih organskih snovi, ki imajo enako kvalitativno in kvantitativno sestavo, vendar se razlikujejo v zaporedju razporeditve atomov.
Ad
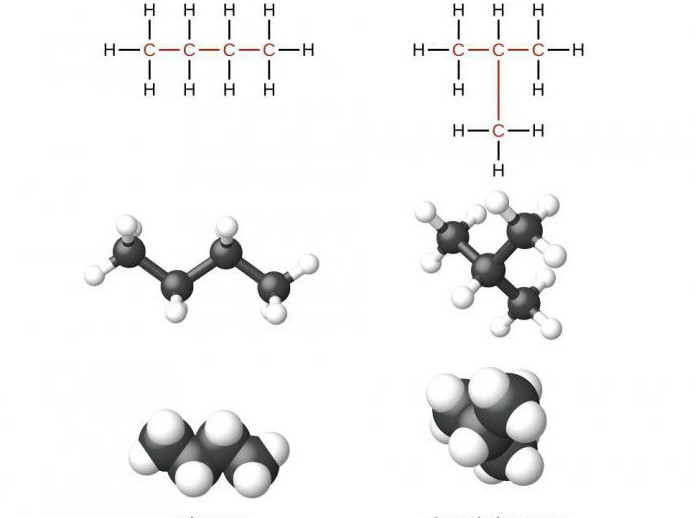
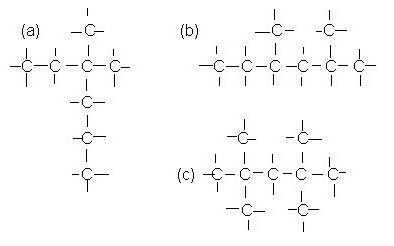
V prisotnosti nasičenih ogljikovodikov s štirimi ali več ogljikovimi atomi v sestavi opazimo izomerijo ogljikovega ogrodja za člane tega razreda. Na primer, možno je formulirati formulo snovi izomerov sestave C5H12 v obliki normalnega pentana, 2-metilbutana, 2,2-dimetilpropana.
Zaporedje
Strukturni izomeri, značilni za alkane, so sestavljeni z uporabo specifičnega algoritma delovanja. Da bi razumeli, kako sestaviti izomere nasičenih ogljikovodikov, se poglobimo o tem vprašanju. Najprej upoštevamo neposredno verigo ogljika, ki nima dodatnih vej. Na primer, v prisotnosti šestih atomov ogljika v molekuli je mogoče pripraviti formulo heksana. Ker imajo alkani vse enojne vezi, se lahko za njih zapišejo samo strukturni izomeri.
Ad
Strukturni izomeri
Za oblikovanje formul možnih izomerov se ogljikov skelet skrajša z enim atomom C, spremeni se v aktivni delček - radikal. Metilna skupina se lahko nahaja na vseh atomih v verigi, razen ekstremnih atomov, tako da tvorijo različne organske derivate alkanov.
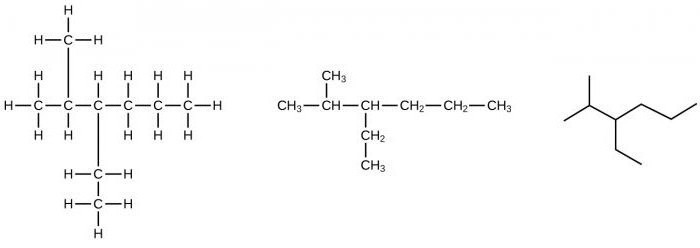
Na primer, lahko naredimo formulo 2-metilpentan, 3-metilpentan. Nato se število ogljikovih atomov v glavni (glavni) verigi zmanjša za še eno, zaradi česar se pojavita dve aktivni metilni skupini. Lahko se nahajajo na istih ali sosednjih atomih ogljika, pri čemer dobimo različne izomerne spojine.
Na primer, lahko ustvarite formule za dva izomera: 2,2-dimetilbutan, 2,3-dimetilbutan, ki se razlikujejo po fizikalnih lastnostih. Z naknadnim skrajšanjem osnovnega ogljikovega ogrodja lahko dobimo druge strukturne izomere. Torej, za ogljikovodike omejevalne serije, se pojav izomerizma pojasni s prisotnostjo posameznih (preprostih) vezi v njihovih molekulah.
Značilnosti izomerizma alkenov
Da bi razumeli, kako narediti izomere, je treba upoštevati posebne značilnosti tega razreda organskih snovi. Imamo splošno formulo SpN2p. V molekulah teh snovi je poleg enojne vezi tudi dvojna vez, ki vpliva na količino izomernih spojin. Poleg strukturne izomernosti, ki je značilna za alkane, lahko za ta razred izločimo tudi izomerijo položaja večkratne vezi, interklasno izomerijo.
Ad
Na primer, za C4H8 ogljikovodik lahko formuliramo dve formuli, ki se razlikujeta v razporeditvi dvojne vezi: buten-1 in buten-2.
Da bi razumeli, kako narediti izomere s splošno formulo C4H8, morate imeti idejo, da imajo poleg alkenov tudi ciklični ogljikovodiki isto splošno formulo. Kot izomeri, ki pripadajo cikličnim spojinam, lahko predstavimo ciklobutan kot tudi metilciklopropan.
Poleg tega lahko formuliramo geometrične izomere za nenasičene spojine etilenskih serij: cis in trans oblike. Za ogljikovodike, ki imajo dvojno vez med atomi ogljika, je značilnih več vrst izomerizma: strukturna, medklasična, geometrijska.
Alkine
Za spojine, ki spadajo v ta razred ogljikovodikov, je splošna formula SpN2p-2. Med razlikovalnimi značilnostmi tega razreda je mogoče omeniti prisotnost trojne vezi v molekuli. Eden od njih je preprost, ki ga tvorijo hibridni oblaki. Dve vezi nastanejo, ko se ne-hibridni oblaki prekrivajo, določajo značilnosti izomerizma tega razreda.
Na primer, za ogljikovodik C5H8 lahko pripravimo formule snovi, ki imajo nerazvejano ogljikovo verigo. Ker je v izvirni spojini večkratna vez, se lahko nahaja drugače in tvori penty-1, penty-2. Na primer, možno je napisati nerazvito in reducirano formulo spojine z dano kvalitativno in kvantitativno sestavo, v kateri bo ogljikova veriga zmanjšana za en atom, ki bo v spojini predstavljen kot radikal. Poleg tega obstajajo interklasni izomeri za alkine, ki so dienski ogljikovodiki.
Ad
Za ogljikovodike, ki imajo trojno vez, lahko sestavimo izomere ogljikovega skeleta, napišemo dienske formule in upoštevamo tudi spojine z drugačno razporeditvijo večkratne vezi.
Zaključek
Pri pripravi strukturnih formul organskih snovi se lahko atomi kisika in ogljikovi atomi uredijo na različne načine, pri čemer nastanejo snovi, ki se imenujejo izomeri. Glede na specifičnost razreda organskih spojin se lahko število izomerov spreminja. Na primer, za ogljikovodike omejevalnih serij, ki vključujejo spojine metanskih serij, je značilna samo strukturna izomerija.
Za homologe etilena, za katere je značilna prisotnost večkratne (dvojne) vezi, lahko poleg strukturnih izomerov upoštevamo tudi izomerijo položaja večkratne vezi. Poleg tega imajo druge spojine, ki spadajo v razred cikloalkanov, enako splošno formulo, to je možno medklasno izomerijo.
Za snovi, ki vsebujejo kisik, na primer za karboksilne kisline, se lahko zapišejo tudi formule optičnih izomerov.