Elektrokemična korozija in zaščita pred njo
Korozija se nanaša na proces spontanega uničenja površine materialov zaradi interakcije z okoljem. Njegov vzrok je termodinamična nestabilnost kemijskih elementov do določenih snovi. Formalno so polimeri, les, keramika, guma podvrženi koroziji, vendar se zanje pogosteje uporablja izraz „staranje“. Največjo škodo povzroča rjavenje kovin, za zaščito katere se razvijajo visokotehnološki protiukrepi. Toda o tem bomo govorili kasneje. Znanstveniki se razlikujejo po kemični in elektrokemični koroziji kovin.

Kemična korozija
Običajno se pojavi, ko je izpostavljen kovinski strukturi suhih plinov, tekočin ali raztopin, ki ne izvajajo električnega toka. Bistvo te vrste korozije je neposredna interakcija kovine z agresivnim okoljem. Elementi kemično korodirajo med toplotno obdelavo ali zaradi dolgotrajnega delovanja pri dovolj visokih temperaturah. To velja za rezila. plinske turbine, oprema za taljenje peči, deli motorjev z notranjim izgorevanjem in tako naprej. Posledično se na površini tvorijo nekatere spojine: oksidi, nitridi, sulfidi.
Ad
Elektrokemična korozija
Je rezultat stika kovin s tekočim medijem, ki lahko prenaša električni tok. Zaradi oksidacije se material spremeni v strukturne spremembe, kar povzroči nastanek rje (netopni produkt) ali pa se kovinski delci prenesejo v raztopino ionov.
Elektrokemična korozija: Primeri
Razdeljen je na:
- Atmosferski, ki se pojavi, ko se na kovinski površini nahaja tekočinski film, v katerem se plini, ki jih vsebuje atmosfera (npr. O 2 , CO 2 , SO 2 ), lahko raztopijo z nastajanjem elektrolitskih sistemov.
- Tekočina, ki teče v prevodnem tekočem mediju.
- Tla, ki teče pod vplivom podzemne vode.
Razlogi
Ker običajno nobena kovina, ki se uporablja za industrijske potrebe, ni popolnoma čista in vsebuje različne vrste vključkov, nastane elektrokemična korozija kovin zaradi nastajanja velikega števila kratkih stikov lokalnih galvanskih celic na površini železa.
Ad
Njihov videz je lahko povezan ne samo s prisotnostjo različnih (zlasti kovinskih) nečistoč (kontaktna korozija), ampak tudi s površinsko heterogenostjo, napakami. kristalne rešetke mehanske poškodbe in podobno.
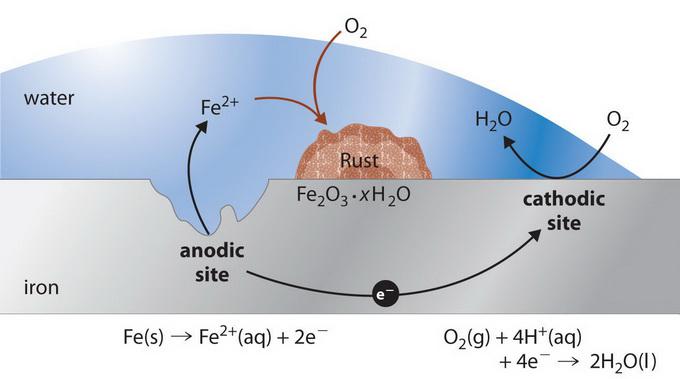
Mehanizem interakcije
Proces elektrokemične korozije je odvisen od kemijske sestave materialov in okoljskih značilnosti. Če je tako imenovana tehnična kovina prekrita z mokrim filmom, potem se v vsaki od teh galvanskih mikroelementov, ki se tvorijo na površini, pojavita dve neodvisni reakciji. Bolj aktivna komponenta korozivnega para daje elektrone (npr. Cink v paru Zn-Fe) in gre v tekoči medij kot hidratirani ioni (to je, korodira) z naslednjo reakcijo (anodni proces):
M + nH 2 O = M z + * nH 2 O + ze.
Ta del površine je negativni pol lokalnega elementa v sledovih, kjer se kovina raztopi elektrokemično.
Na manj aktivnem delu površine, ki je pozitiven pol mikroelementa (železo v paru Zn-Fe), so elektroni vezani zaradi redukcijske reakcije (katodni proces) po shemi:
Ad
Ox + ze = Rdeča.
Prisotnost oksidacijskih sredstev v vodnem filmu, ki lahko veže elektrone, omogoča nadaljevanje anodnega procesa. Tako se lahko elektrokemijska korozija razvije le, če se hkrati odvijajo anodni in katodni procesi. Zaradi zaviranja enega od njih se stopnja oksidacije zmanjša.

Proces polarizacije
Oba zgoraj omenjena procesa povzročata polarizacijo ustreznih polov (elektrod) elementa v sledovih. Kakšne so funkcije tukaj? Navadno je elektrokemijska korozija kovin bistveno upočasnjena zaradi polarizacije katode. Zato se bo ojačala pod vplivom faktorjev, ki preprečujejo to reakcijo, in jih spremlja tako imenovana depolarizacija pozitivne elektrode.
Pri mnogih korozijskih procesih se katodna depolarizacija izvaja z odvajanjem vodikovih ionov ali z redukcijo vodnih molekul in ustreza formulam:
- V kislem okolju: 2H + + 2e = H2.
- V alkalnem: 2H2O + 2e = H2 + 2OH - .
Potencialno območje
Potencial, ki ustreza tem procesom, odvisno od narave agresivnega okolja, se lahko spreminja od -0,83 do 0 V. Za nevtralno vodno raztopino pri temperaturah blizu standarda, je približno -0,41 V. Posledično, vodikovi ioni, v vodi in v nevtralnih vodnih sistemih, lahko oksidirajo samo kovine s potencialom, manjšim od -0,41 V (ki se nahaja v nizu napetosti za kadmij). Glede na to, da so nekateri elementi zaščiteni z oksidnim filmom, je število kovin, dovzetnih za oksidacijo v nevtralnih medijih z vodikovimi ioni, zanemarljivo.
Če vlažen film vsebuje raztopljeni kisik zraka, potem je lahko, odvisno od narave medija, vezan elektrone z učinkom depolarizacije kisika. V tem primeru je shema elektrokemične korozije naslednja:
Ad
- O2 + 4e + 2H2O = 4OH - ali
- 2 + 4e + 4H + = 2H20.
Potencial teh elektrodnih reakcij pri temperaturah, ki so blizu standardnemu, je od 0,4 V (alkalni medij) do 1,23 V (kisli medij). V nevtralnih okoljih potencial procesa redukcije kisika pri teh pogojih ustreza vrednosti 0,8 V. Zato je raztopljeni kisik sposoben oksidacije kovin s potencialom manjšim od 0,8 V (ki se nahaja v nizu napetosti za srebro).

Glavni oksidanti
Vrste elektrokemijske korozije so označene z oksidacijskimi elementi, med katerimi so najpomembnejši vodikovi ioni in kisik. Hkrati je film, ki vsebuje raztopljeni kisik, veliko bolj nevaren v smislu korozije kot vlaga, kjer ni kisika in je sposoben oksidirati kovine samo z vodikovimi ioni, saj je v zadnjem primeru število vrst materialov, ki lahko korodirajo, veliko manj.
Ad
V jeklu in v železu so na primer ogljikove nečistoče prisotne predvsem v obliki železovega karbida Fe 3 C. V tem primeru je mehanizem elektrokemijske korozije z depolarizacijo vodika za te kovine naslednji:
- (-) Fe - 2e + nH 2 O = Fe 2+ nH 2 O (lahko nastane rja);
- (+) 2H + + 2e = H2 (v nakisanem mediju);
- (+) 2H2O + 2e = H2 + 2OH - (v nevtralnem in alkalnem okolju).
Mehanizem korozije železa, ki vsebuje nečistoče bakra, v primeru depolarizacije kisika katode je opisan z enačbami:
- (-) Fe-2e + nH2O = Fe2 + nH2O;
- (+) 0,502 + H2O + 2e = 2OH - (v nakisanem mediju);
- (+) 0,5O2 + 2H + + 2e = H 2 O (v nevtralnem in alkalnem mediju).
Elektrokemična korozija poteka z različnimi hitrostmi. Ta kazalnik je odvisen od:
- potencialne razlike med poli elementa v galvanizaciji v sledovih;
- sestavo in lastnosti elektrolitskega medija (pH, prisotnost inhibitorjev in stimulansov korozije);
- koncentracija (hitrost pretoka) oksidacijskega sredstva;
- temperature
Metode zaščite
Elektrokemična zaščita kovin pred korozijo se doseže na naslednje načine:
- Ustvarjanje antikorozijskih zlitin (legiranje).
- Povečajte čistost posamezne kovine.
- Z nanosom na površino različnih zaščitnih premazov.
Ti premazi so:
- Nekovinski (barve, laki, t maziva emajla).
- Kovinski (anodni in katodni premazi).
- Oblikuje se s posebno površinsko obdelavo (pasiviranje železa v koncentrirani žveplovi kislini ali. T dušikova kislina; železo, nikelj, kobalt, magnezij v alkalnih raztopinah; tvorbo oksidnega filma, na primer na aluminiju).
Kovinske plošče
Najbolj zanimiva in obetavna je elektrokemična korozijska zaščita druge vrste kovine. Zaradi narave zaščitnega učinka se metalizirani premazi delijo na anodno in katodno. O tem se poglobimo bolj podrobno.
Anodna prevleka je prevleka, ki jo tvori bolj aktivna (manj plemenita) kovina kot tista, ki je zaščitena. To pomeni, da zaščito izvaja element, ki je v območju napetosti od osnovnega materiala (npr. Prevleka iz železa s cinkom ali kadmijem). V primeru lokalnega uničenja zaščitnega sloja bo korozija manj plemenita prevleka iz kovine. V območju prask in razpok se oblikuje lokalna galvanska celica, katere katoda je kovina, ki jo je treba ograjevati, anoda pa je oksidirana prevleka. Celovitost takega zaščitnega filma ni pomembna. Toda če je debelejša, se bo elektrokemijska korozija počasnejša, koristni učinek bo trajal dlje.
Katodna se imenuje premaz z visoko potencialno kovino, ki v nizu napetosti stoji za zaščitenim materialom (npr. Brizganje nizko legiranih jekel z bakrom, kositrom, nikljem, srebrom). Prevleka mora biti neprekinjena, saj se pri poškodbi tvorijo lokalne galvanske celice, v katerih je osnovna kovina anoda, zaščitna plast pa je katoda.

Kako zaščititi kovino pred oksidacijo
Elektrokemična korozijska zaščita je razdeljena na dve vrsti: tekalna plast in katodo. Podplat je podoben anodnemu premazu. Večja plošča bolj aktivne zlitine je pritrjena na material, ki ga je treba zaščititi. Oblikuje se galvanska celica, osnovna kovina, v kateri služi kot katoda, zaščitnik pa je anoda (korodira). Za to vrsto zaščite se običajno uporabljajo zlitine na osnovi cinka, aluminija ali magnezija. Ščitnik se postopoma raztopi, zato ga je treba redno menjati.
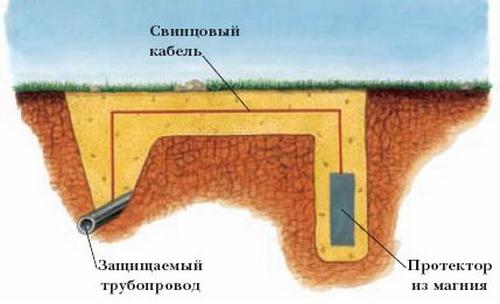
Elektrokemična korozija cevovodov povzroča veliko težav v sektorju gospodarskih javnih služb in industrije kot celote. V boju proti njej je najprimernejša metoda polarizacije katode. Pri tem je kovinska konstrukcija, ki je zaščitena pred destruktivnimi oksidacijskimi procesi, povezana z negativnim polom nekega zunanjega enosmernega vira (potem postane katoda, s tem se poveča hitrost nastajanja vodika in zmanjša korozijska stopnja), na pozitivni pol pa pritrdi nizko vrednost kovine. .
Metode elektrokemične zaščite so učinkovite v prevodnem mediju (morska voda je odličen primer). Zato se zaščitniki pogosto uporabljajo za zaščito podvodnih delov ladij.
Agresivno ravnanje
Ta metoda je učinkovita, kadar elektrokemijska korozija železa poteka v majhni količini prevodne tekočine. Obvladati destruktivne procese v tem primeru na dva načina:
- Odstranjevanje kisika iz tekočine (odzračevanje) zaradi izpiranja z inertnim plinom.
- Uvajanje inhibitorjev v okolje - tako imenovani inhibitorji korozije. Na primer, če je površina uničena z oksidacijo s kisikom, dodajte organske snovi molekul, ki vsebujejo določene aminokisline (imino, tio in druge skupine). Dobro se adsorbirajo na kovinsko površino in znatno zmanjšajo hitrost elektrokemijskih reakcij, ki vodijo do uničenja površinskega kontaktnega sloja.
Zaključek
Seveda kemična in elektrokemična korozija povzroča veliko škodo tako v industriji kot v vsakdanjem življenju. Če kovine ne korodira, bi se življenjska doba mnogih predmetov, delov, sklopov, mehanizmov znatno povečala. Zdaj znanstveniki aktivno razvijajo alternativne materiale, ki lahko zamenjajo kovine, ne pa slabše po zmogljivosti, vendar je verjetno nemogoče popolnoma opustiti njegovo uporabo v kratkem času. V tem primeru se pojavljajo napredne metode za zaščito kovinskih površin pred korozijo.