Kristalna in amorfna telesa: struktura in lastnosti
Obstaja več agregatnih stanj, v katerih se nahajajo vsa telesa in snovi. To je:
- plin;
- tekočina;
- plazma;
- trdno.
Če upoštevamo celotno populacijo planeta in prostora, je večina snovi in teles še vedno v stanju plina in plazme. Vendar pa je na Zemlji sama vsebnost trdnih delcev pomembna. Tu bomo govorili o njih, ugotovili, kaj so kristalne in amorfne trdne snovi.
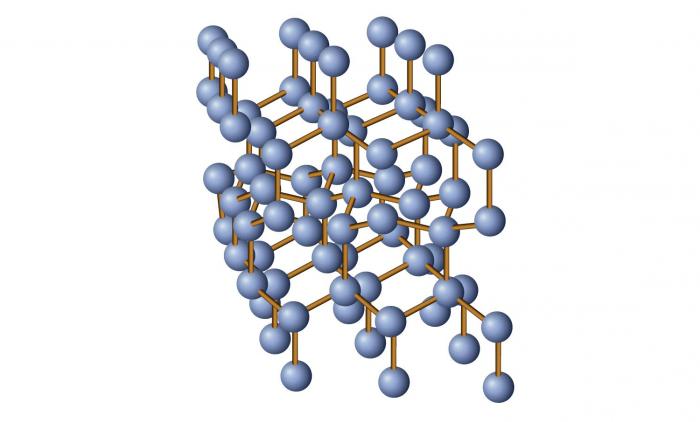
Kristalno in amorfna telesa: splošni koncept
Vse trdne snovi, telesa, predmeti so pogojno razdeljeni na:
- kristalinična;
- amorfen.
Razlika med njimi je ogromna, saj so osnova enote znaki strukture in izražene lastnosti. Na kratko, trdni kristali so tiste snovi in telesa, ki imajo določeno vrsto prostorskih kristalne rešetke to pomeni, da imajo sposobnost spreminjanja v določeni smeri, vendar ne v vseh (anizotropija).
Če pa so značilne amorfne spojine, potem je njihov prvi znak zmožnost hkratnega spreminjanja fizikalnih lastnosti v vseh smereh. To se imenuje izotropija.
Struktura, lastnosti kristaliničnih in amorfnih teles so popolnoma drugačne. Če imata prva jasno omejeno strukturo, ki je sestavljena iz urejenih delcev v prostoru, potem slednja nima reda.
Ad

Lastnosti trdnih snovi
Kristalna in amorfna telesa kljub temu spadajo v eno samo skupino trdnih snovi, zato imata vse značilnosti tega agregatnega stanja. To pomeni, da bodo splošne lastnosti za njih naslednje:
- Mehanska - elastičnost, trdota, sposobnost deformacije.
- Toplotno vrelišče in tališče, koeficient toplotnega raztezanja.
- Električna in magnetno - toplotna in električna prevodnost.
Tako obravnavane države imajo vse te značilnosti. Pojavijo se samo v amorfnih telesih in bodo nekoliko drugačne kot v kristalnih.
Pomembne lastnosti za industrijske namene so mehanske in električne. Pomembna značilnost je sposobnost okrevanja od deformacije ali, nasprotno, razpadanja in mletja. Veliko vlogo igra tudi dejstvo, da lahko snov prenaša električni tok ali je ni sposobna.
Ad

Kristalna struktura
Če opišemo strukturo kristalnih in amorfnih teles, moramo najprej navesti vrsto delcev, ki jih sestavljajo. V primeru. T kristali morda so ioni atomi, atomi, ioni (v kovinah) molekul (redko).
Na splošno so za te strukture značilna prisotnost strogo urejene prostorske mreže, ki se oblikuje kot posledica razporeditve delcev, ki tvorijo snov. Če si predstavljate strukturo kristala figurativno, dobite nekaj takega: atomi (ali drugi delci) so med seboj oddaljeni na določenih razdaljah, tako da dobimo idealno celico prihodnje kristalne rešetke. Nato se ta celica večkrat ponovi in tako se oblikuje celotna struktura.
Glavna značilnost je, da se fizikalne lastnosti takih struktur razlikujejo vzporedno, vendar ne v vseh smereh. Ta pojav se imenuje anizotropija. To pomeni, da če delujete na enem delu kristala, se druga stran morda ne bo odzvala nanj. Torej lahko zmelješ pol kosa soli, drugi pa ostane nedotaknjen.
Ad
Tipi kristalov
Običajno označujeta dve različici kristalov. Prva je monokristalna struktura, to je, ko je mreža sama 1. Kristalne in amorfne telesi so v tem primeru popolnoma drugačne lastnosti. Navsezadnje je za en kristal značilna anizotropija v čisti obliki. Je najmanjša elementarna struktura.
Če se posamezni kristali ponovijo večkrat in se združijo v eno, potem govorimo o polikristalu. Potem ne govorimo o anizotropiji, ker usmeritev elementarnih celic krši splošno urejeno strukturo. V zvezi s tem so polikristali in amorfna telesa blizu fizikalnih lastnosti.

Kovine in zlitine
Kristalinična in amorfna telesa sta zelo blizu drug drugemu. To je enostavno prepričati, pri čemer je treba vzeti kovine in njihove zlitine. Sami so pod normalnimi pogoji trdne snovi. Vendar se pri določeni temperaturi začnejo taliti in dokler ne pride do popolne kristalizacije, ostanejo v stanju raztezanja, debele, viskozne mase. In to je že amorfno stanje telesa.
Zato lahko strogo gledano skoraj vsaka kristalna snov pod določenimi pogoji postane amorfna. Tako kot slednji med strjevanjem postane trdna s urejeno prostorsko strukturo.
Ad
Kovine imajo lahko različne vrste prostorskih struktur, od katerih so najbolj znane in raziskane naslednje:
- Enostavna kubična.
- Zrnat.
- Z osredotočenim na glasnost.
Struktura kristala lahko temelji na prizmi ali piramidi, njen glavni del pa predstavlja:
- trikotnik;
- paralelogram;
- po kvadratu;
- šesterokotnik.
Snov, ki ima preprosto kubično mrežico, ima idealne izotropne lastnosti.

Koncept amorfnega
Kristalinična in amorfna telesa, navzven preprosta za razlikovanje. Navsezadnje jih je mogoče pogosto zamenjati z viskoznimi tekočinami. Struktura amorfne snovi temelji tudi na ionih, atomih, molekulah. Vendar pa ne tvorijo urejene stroge strukture, zato se njihove lastnosti spreminjajo v vseh smereh. To pomeni, da so izotropne.
Delci so razvrščeni naključno, naključno. Le včasih lahko tvorijo majhne lokuse, ki še vedno ne vplivajo na prikazane splošne lastnosti.
Lastnosti podobnih teles
So enake kristalom. Razlike so le pri kazalnikih za posamezno telo. Tako lahko na primer ločimo take karakteristične parametre amorfnih teles:
- elastičnost;
- gostota;
- viskoznost;
- žilavost;
- prevodnost in polprevodnost.
Pogosto lahko dosežete mejne pogoje spojin. Kristalinična in amorfna telesa lahko postanejo pol-amorfna.
Zanimiva je tudi značilnost zadevne države, ki se izraža z ostrim zunanjim vplivom. Torej, če je amorfno telo izpostavljeno močnemu udaru ali deformaciji, se lahko obnaša kot polikristal in se razcepi na majhne koščke. Vendar, če je čas za te dele, se bodo kmalu ponovno združili in spremenili v viskozno tekoče stanje.
Ad

To stanje spojin nima specifične temperature, pri kateri pride do faznega prehoda. Ta proces je močno razširjen, včasih celo desetletja (npr. Razgradnja polietilena nizkega tlaka).
Primeri amorfnih snovi
Obstaja veliko primerov takih snovi. Označimo nekaj najbolj očitnih in pogosto izpolnjenih.
- Čokolada je značilna amorfna snov.
- Smole, vključno s fenol-formaldehidom, vse plastike.
- Amber
- Steklo katere koli sestave.
- Bitumen
- Tar
- Vosek in drugi.
Amorfno telo nastane zaradi zelo počasne kristalizacije, to je povečanja viskoznosti raztopine pri znižanju temperature. Pogosto je te snovi težko imenovati trdne, temveč se nanašajo na viskozne debele tekočine.
Spojine, ki se pri kristalizaciji sploh ne kristalizirajo, imajo posebno stanje. Imenujejo se očala, država - steklasta.
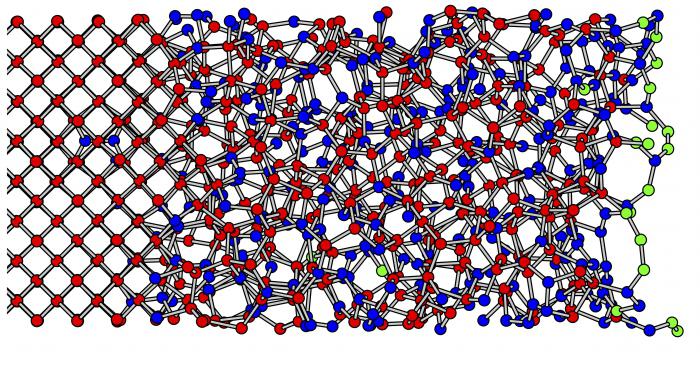
Steklene snovi
Lastnosti kristaliničnih in amorfnih teles so podobne, kot smo ugotovili, zaradi njihovega skupnega izvora in ene same notranje narave. Ampak včasih se ločeno šteje za posebno stanje snovi, ki se imenuje steklast. Gre za homogeno mineralno raztopino, ki kristalizira in strdi brez oblikovanja prostorskih mrež. To pomeni, da ostane vedno izotropen v smislu spreminjanja lastnosti.
Na primer, običajno okensko steklo nima točne vrednosti tališča. Samo s povečanjem tega indikatorja se počasi stopi, mehča in spremeni v tekoče stanje. Če se učinek ustavi, se bo zgodil obratni proces in strjevanje se bo začelo, vendar brez kristalizacije.
Takšne snovi so zelo cenjene, steklo je danes eno najpogostejših in najbolj iskanih gradbenih materialov po vsem svetu.