Kompleksne spojine in njihov pomen
Kompleksne spojine (CS) imajo pomembno vlogo pri aktivnosti živih organizmov. Prav tako se pogosto uporabljajo v industriji. Danes upoštevamo njihovo raznolikost vrst, uporabo in zgodovino študije.
Uvod v kompleksne spojine
Kompleksne spojine so snovi, ki nastanejo s kombinacijo liganda in kompleksirnega sredstva. Igrajte vlogo medsebojno delujočih delcev lahko atomov in ionov. A. Werner je leta 1893 uvedel teorijo kompleksnih spojin v svet, imenovano tudi teorija koordinacije.
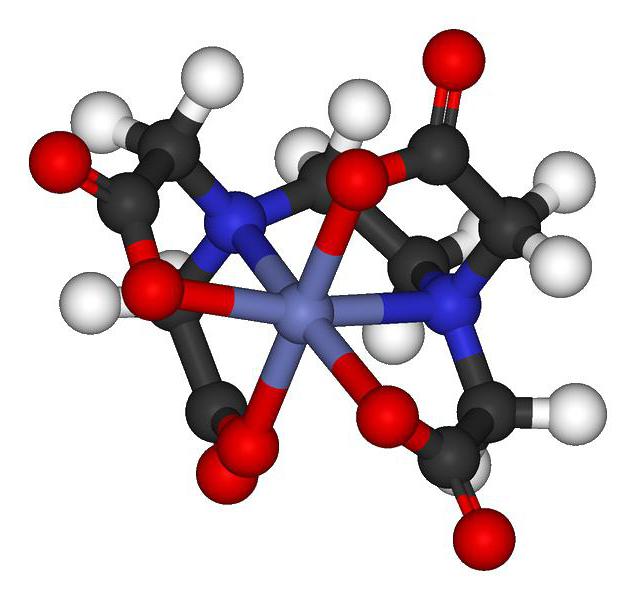
Za CS je značilna prisotnost zunanje krogle in popolna disociacija v raztopini vode v nizke disociacijske katione in anione. Vendar pa obstajajo nekatere vrste, ki nimajo zunanje sfere, ki jim ne omogoča, da bi se raztopile v vodi. Obstaja ogromna količina policaja.
Vrste spojin
Kompleksne spojine so razdeljene v tri glavne vrste:
- Prva vrsta, ki se razlikuje po kompleksnem naboju, vključuje kationske komplekse, v katerih so nevtralne molekule, ki obkrožajo pozitivni ion, usklajene. Drugi tip je anionski kompleks, v katerem pozitivno oksidiran atom deluje kot kompleksirno sredstvo in anioni enostavnega ali kompleksnega tipa so ligandi. Tretji tip se imenuje nevtralni kompleks, nastal je zaradi molekularne koordinacije okoli atoma z nevtralnim nabojem.
- Glede na naravo liganda so razdeljeni na amonijake (amoniak - ligand), akvakompleksi (ligand - voda), hidroksompleksi (ligandi - hidroksidni ioni), kislinski kompleksi (ligandi - kislinski ostanki), karbonili (ligandi - ogljikove molekule druge valence).
- V skladu z lokacijo ligandov sta monodentat, bidentat in polidentat QS.
Zgodovinske informacije
Leta 1893 je bil narejen prvi poskus, da se s pomočjo koordinacijske teorije Alfreda Wernerja izčrpno opiše struktura CS. Delo je bilo opravljeno pred pojavom teorije elektronske valence in običajno kemijske reakcije narave.

Werner je v svoji teoriji trdil, da imajo spojine anorganske narave jedra sestavljenih iz kompleksnih atomov. Atomi, ki obdajajo kompleks, se imenujejo koordinacija. Razporejeni so v skladu z obliko enostavnega poliedra. A. Werner je predvideval prisotnost veznega tipa v skupnem elektronskem paru, ki bi ga atomi ali molekule dali drugemu paru. Vendar pa odsotnost takšnih spojin povzroča nezaupanje med kemično skupnostjo. Kot rezultat, v naslednjih dveh desetletjih, znanstvenik poskušal ustvariti potrebne snovi, ki bi potrdili njegovo teorijo.
Werner je leta 1911 sintetiziral več kot štirideset molekul optičnega tipa, ki niso vsebovale ogljikovih atomov, kar je na koncu spremenilo mnenje kemijskih znanstvenikov o njegovi teoriji.
Alfred Werner je leta 1913 prejel Nobelovo nagrado za dosežke na področju kemije.
Nomenklatura
Kompleksne spojine imajo sistem za ustvarjanje lastnih imen, sestavljen iz petih točk:
- Prvi je izrazit anion, nato kation.
- Kompleksni del se začne z ligandom - anionom, ki se nahaja v notranji sferi, do konca pa se doda »o«.
- Monodentatni ligandi so označeni s pomočjo grškega: mono, di, tri, tetra, penta, hex (1, 2, 3, 4, 5, 6). Pri delu s polidentatnimi ligandi uporabljamo tris, bis, tetrakis in druge.
- Označevanje notranje sfere s svojimi komponentami, gre na zunanjo.
- Kompleksirno sredstvo delcev z nevtralnim kompleksom je navedeno v nominativnem primeru.
Informacije o strukturi
Kompleksne spojine imajo notranjo sfero, sestavljeno iz številnih ionov ali molekul nevtralne narave, ki so trdno povezani s kompleksirnim sredstvom. Imenujejo se ligandi. Notranja krogla lahko nosi tri vrste naboja: "+", "-" ali "0".
Zunanja koordinacijska sfera so ioni, ki se ne nahajajo v prostoru notranje sfere.
Povezavo med ligandom in centralnim ionom lahko povzroči bodisi elektrostatična privlačnost bodisi donorsko-akceptorski mehanizem.
Izomerija v koordinacijskih spojinah je pomemben statistični vidik. Ko govorimo o izomerizmu, pomenijo različne medsebojne položaje v prostoru atomov ali sestavin spojine, kar bo povzročilo spremembo fizikalnih in kemijskih lastnosti ustrezne spojine - izomera. CS izomerija je strukturna, optična in prostorska.
Stereokemija
Kompleksne spojine skupaj z organske snovi Visoko molekularne spojine sintetičnega ali naravnega izvora so glavni predmet stereokemijskih študij. A. Werner velja za enega tistih znanstvenikov, ki so razvili celotno področje raziskav in oživili nekatera področja kemijske dejavnosti. Stereokemija do danes ostaja referenčna točka za koordinacijske kemijske raziskave.
Nekatere lastnosti in metode pridobivanja
Pridobivanje kompleksnih spojin ima precej široko paleto izbir, vendar pa se takšne izbire pogosteje uporabljajo:
- Raztapljanje hidroksidov v vodnem amoniaku, ki se ne raztopi v vodi.
- Interakcija amoniaka s kovinskimi solmi s kompleksnimi lastnostmi; pogosteje so to kovine v sekundarni podskupini.
- Medsebojno delovanje cianidov ali rodanidov s kovinami ali solmi.
- Prostor je netopen v metali H 2 O amfoternega tipa, in sicer njihovi oksidi ali hidroksidi v alkalni raztopini.
- Kompleksne kisline lahko dobimo, na primer, z reagiranjem zlata in vodne kisline ali z hidroksilnim hidroksidom s HCl.
Številne kvalitativne lastnosti spojin so odvisne od njihovih elektronskih lastnosti, zato lahko barvo CS določimo s kompleksirnim sredstvom in ligandi. Energija, ki razcepi d-orbital, omogoča, da se elektroni gibljejo od njenih d xz , d xy , d zy nivojev na podravne z višjim energetskim indeksom d z 2 ali d z 2 - y 2 . Ta pojav spremlja absorpcija kvantov svetlobe. Velikost razlike med deljenimi ravnmi povzroča absorpcijo kvantov svetlobe z valovno dolžino različnih dolžin, ki daje določeno barvo.
Kompleksne spojine imajo tudi dve pomembni magnetni lastnosti, po katerih sta razvrščeni kot paramagnetni in diamagnetni. Paramagnetni kompleksi imajo svoje µ-momente in zato vstopajo v zunanja elektromagnetna polja v procesu interakcije. Diamagnetni kompleks nima magnetnega momenta, zato se magnetno polje mudi, da ga iztisne. Lastnosti paramagnetne narave določajo prisotnost elektronov, ki v svoji strukturi nimajo para.
Uporaba

Kompleksne spojine imajo eno od najpomembnejših vlog v vsakem organizmu, npr. Kisik, ki je v kombinaciji s hemoglobinom v krvi, preko telesa dovaja O2 v tkiva in celice; Klorofil v rastlinah je prav tako zapleten.
Uporaba kompleksnih spojin se pogosto uporablja v industriji. S pomočjo kemijskih metod, ki vključujejo tvorbo KS, se iz rude pridobivajo kovine. Primeri vključujejo čisto železo, nikelj in kobalt, ki jih dobimo s toplotno razgradnjo kovinskih karbonilov. Te kompleksne snovi, ki razpadajo, oddajajo potrebne kovine.

Analitična kemija lahko uporablja COP kot indikatorje. Zaradi njih lahko pospešimo organsko in anorgansko sintezo, saj so lastnosti katalizatorja neločljivo povezane z njihovo visoko aktivnostjo. Elektroformiranje tudi ne more biti brez kompleksnih spojin, kar je posledica nezmožnosti pridobivanja takšnih zanesljivih premazov iz preproste soli, v nasprotju s cianidnimi spojinami.