20 aminokislin: imena, formule, vrednost. Alanin, valin, serin, lizin, prolin, tirozin
Kemikalije, ki vsebujejo strukturne komponente molekule karboksilne kisline in amina, se imenujejo aminokisline. To je običajno ime skupine. organske spojine ki vsebuje ogljikovodično verigo, karboksilno skupino (-COOH) in amino skupino (-NH2). Njihovi predhodniki so karboksilne kisline in molekule, v katerih je vodik na prvem ogljikovem atomu nadomeščen z amino skupino, se imenujejo alfa-aminokisline.
Samo 20 aminokislin je dragocenih za encimske reakcije biosinteze, ki se pojavljajo v organizmu vseh živih bitij. Te snovi se imenujejo standardne aminokisline. Obstajajo tudi nestandardne aminokisline, ki so vključene v sestavo nekaterih posebnih beljakovinskih molekul. Ne najdemo jih povsod, čeprav v naravi opravljajo pomembno funkcijo. Verjetno so radikali teh kislin spremenjeni že po biosintezi.
Ad
Splošne informacije in seznam snovi
Obstajata dve veliki skupini aminokislin, ki sta bili izolirani zaradi zakonov njihove prisotnosti v naravi. Še posebej je na voljo 20 aminokislin standardnega tipa in 26 nestandardnih aminokislin. Prvi se nahajajo v sestavi beljakovin vseh živih organizmov, drugi pa so značilni za posamezne žive organizme.
20 standardnih aminokislin so razdeljene v 2 vrsti, odvisno od sposobnosti sintetiziranja v človeškem telesu. Te so zamenljive, ki se v človeških celicah lahko oblikujejo iz predhodnih sestavin in so nenadomestljive, za sintezo katerih ni encimskih sistemov ali substrata. Zamenljive aminokisline morda niso prisotne v hrani, saj lahko njihovo telo sintetizira in po potrebi dopolni njihovo količino. Eterične aminokisline telo ne more pridobiti samostojno, zato mora prihajati iz hrane.
Ad
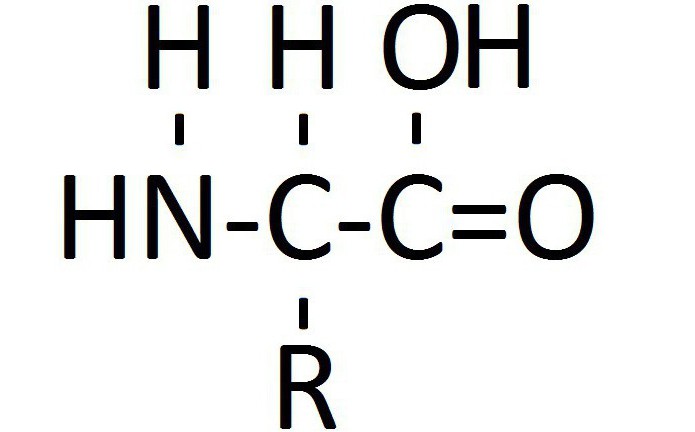
Biokemiki so definirali imena aminokislin iz skupine bistvenih. Znanih je skupno 8:
- metionin;
- treonin;
- izoleucina;
- levcin;
- fenilalanin;
- triptofan;
- valin;
- lizin;
- pogosto vključujejo tudi histidin.
To so snovi z različno strukturo ogljikovodikovih radikalov, vendar nujno s prisotnostjo karboksilne skupine in amino skupine na alfa-C-atomu.
V skupini zamenljivih aminokislin obstaja 11 snovi:
- alanin;
- glicin;
- arginin;
- asparagin;
- asparaginska kislina;
- cistein;
- glutaminska kislina;
- glutamin;
- prolin;
- serin;
- tirozina.
V bistvu je njihova kemijska struktura enostavnejša kot pri nenadomestljivih, zato je njihova sinteza za telo lažja. Večine esencialnih aminokislin ni mogoče dobiti le zaradi odsotnosti substrata, to je prekurzorske molekule prek reakcije transaminacije.
Glicin, alanin, valin
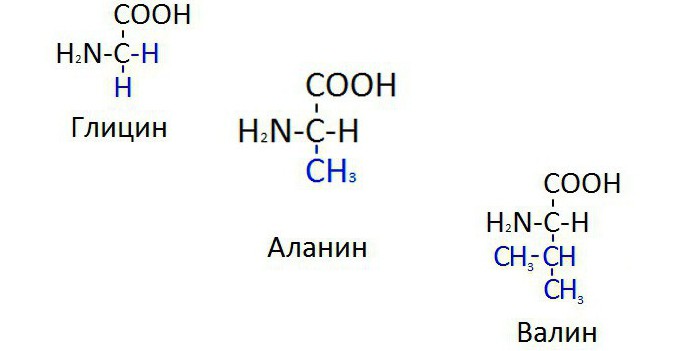
Pri biosintezi beljakovinskih molekul so najpogosteje uporabljeni glicin, valin in alanin (formula vsake snovi je prikazana spodaj na sliki). Te aminokisline so najenostavnejše v kemijski strukturi. Snov glicin je najpreprostejša v razredu aminokislin, to pomeni, da poleg alfa-ogljikovega atoma spojina nima radikalov. Toda tudi najpreprostejša struktura molekule ima pomembno vlogo pri podpori življenju. Še zlasti sintetiziramo hemoglobin porfirinski obroč in purinske baze iz glicina. Porfirni obroč je beljakovinski del hemoglobina, ki je zasnovan tako, da v sestavi celotne snovi vsebuje atome železa.
Ad
Glicin sodeluje pri zagotavljanju delovanja možganov, ki deluje kot zaviralni posrednik centralnega živčnega sistema. To pomeni, da je bolj vključen v delo možganske skorje - njeno najtežje organizirano tkivo. Še pomembneje je, da je glicin substrat za sintezo purinskih baz, ki je potreben za tvorbo nukleotidov, ki kodirajo dedne informacije. Poleg tega glicin služi kot vir za sintezo drugih 20 aminokislin, medtem ko lahko le-ta nastane iz serina.
Formula aminokisline alanin je nekoliko bolj zapletena od glicina, ker ima metil radikal, ki je nadomeščen z enim vodikovim atomom na alfa ogljikovem atomu snovi. Hkrati pa alanin ostaja ena izmed najpogosteje vpletenih molekul v biosintezi beljakovin. Je del vsake beljakovine v naravi.
Valin, ki ne more sintetizirati v človeškem telesu, je aminokislina z razvejeno ogljikovodično verigo, ki sestoji iz treh ogljikovih atomov. Izopropilni radikal daje molekuli večjo težo, toda zaradi tega je nemogoče najti substrat za biosintezo v celicah človeških organov. Zato mora valin nujno izhajati iz hrane. Prisoten je predvsem v strukturnih mišičnih beljakovinah.
Rezultati raziskave potrjujejo, da je valin potreben za delovanje centralnega živčnega sistema. Zlasti zaradi svoje sposobnosti za obnovitev mielinske ovojnice živčnih vlaken se lahko uporablja kot pomoč pri zdravljenju multiple skleroze, odvisnosti od drog in depresije. Najdemo ga v velikih količinah v mesnih izdelkih, rižu, posušenem grahu.
Ad
Tirozin, histidin, triptofan
V telesu se tirozin lahko sintetizira iz fenilalanina, čeprav prihaja iz velikih količin mlečnih izdelkov, predvsem iz skute in sirov. V kazein je vključena živalska beljakovina, ki je presežena v skuto in sirnih proizvodih. Ključna vrednost tirozina je, da njegova molekula postane substrat za sintezo kateholaminov. To so adrenalinski, norepinefrin, dopaminski mediatorji humoralnega sistema regulacije telesnih funkcij. Tirozin lahko hitro prodre skozi in skozi krvno-možganska pregrada, kjer se hitro spremeni v dopamin. Molekula tirozina sodeluje pri sintezi melanina, ki zagotavlja pigmentacijo kože, las in šarenice.
Hididinska amino kislina je del strukturnih in encimskih proteinov v telesu, je substrat za sintezo histamina. Slednji ureja izločanje želodca, sodeluje v imunskih reakcijah, uravnava celjenje poškodb. Histidin je esencialna aminokislina, telo pa svoje zaloge obnavlja samo iz hrane.
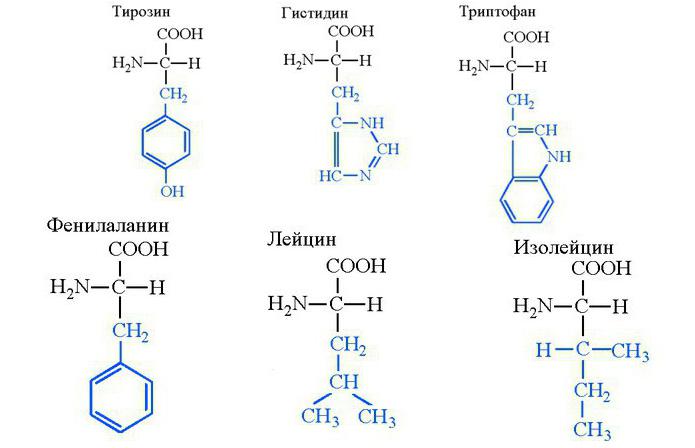
Telo ne more sintetizirati triptofana zaradi kompleksnosti ogljikovodikove verige. Je del proteina in je substrat za sintezo serotonina. Slednji je posrednik živčnega sistema, ki je namenjen uravnavanju ciklov budnosti in spanja. Triptofan in tirozin - ta imena aminokislin je treba zapomniti s strani nevrofiziologov, saj se iz njih sintetizirajo glavni mediatorji limbični sistem (serotonin in dopamin), ki zagotavljajo prisotnost čustev. Hkrati pa ni molekularne oblike, ki bi zagotavljala kopičenje esencialnih aminokislin v tkivih, zato morajo biti v hrani prisotni vsak dan. Proteinska hrana v višini 70 gramov na dan v celoti zadovolji te potrebe telesa.
Ad
Fenilalanin, levcin in izolevcin
Fenilalanin je izjemen, ker sintetizira aminokislinski tirozin s pomanjkanjem. Fenilalanin je strukturna sestavina vseh beljakovin v naravi. Je presnovni prekurzor nevrotransmiterja feniletilamina, ki zagotavlja duševno koncentracijo, dvig razpoloženja in psihostimulacijo. V Ruski federaciji v koncentraciji več kot 15% je promet s to snovjo prepovedan. Učinek feniletilamina je podoben učinkom amfetamina, vendar se prvi ne razlikuje po škodljivih učinkih na telo in se razlikuje le v razvoju psihološke odvisnosti.
Ena glavnih snovi aminokislinske skupine je levcin, iz katerega se sintetizirajo peptidne verige vseh človeških beljakovin, vključno z encimi. Spojina, ki se uporablja v svoji čisti obliki, lahko uravnava delovanje jeter, pospešuje regeneracijo celic in zagotavlja pomlajevanje telesa. Zato je levcin aminokislina, ki je na voljo kot zdravilo. Je zelo učinkovit pri pomožnem zdravljenju jetrne ciroze, anemije in levkemije. Leucin je aminokislina, ki močno olajša rehabilitacijo bolnikov po kemoterapiji.

Izoleucin, tako kot levcin, telo ne more sintetizirati neodvisno in spada v skupino bistvenih. Vendar pa ta snov ni droga, saj ima telo majhno potrebo po njem. V bistvu je v biosintezo vključen le eden od njegovih stereoizomerov (2S, 3S) -2-amino-3-metilpentanojske kisline.
Prolin, serin, cistein
Snov prolin je aminokislina s cikličnim ogljikovodičnim radikalom. Njegova glavna vrednost je prisotnost ketonske skupine v verigi, zaradi katere se snov aktivno uporablja pri sintezi strukturnih proteinov. Zmanjšanje ketona heterocikla v hidroksilno skupino, da se tvori hidroksiprolin, tvori več vodikovih vezi med verigami kolagena. Posledično so niti tega proteina skupaj tkane in zagotavljajo močno medmolekularno strukturo.
Prolin - aminokislina, ki zagotavlja mehansko trdnost človeškega tkiva in njegovega okostja. Najpogosteje ga najdemo v kolagenu, ki je del kosti, hrustanca in vezivnega tkiva. Tako kot prolin je cistein tudi aminokislina, iz katere se sintetizira strukturni protein. Vendar to ni kolagen, ampak skupina alfa-keratinskih snovi. Oblikujejo stratum corneum kože, nohti, so vključeni v sestavo lestvice lase.
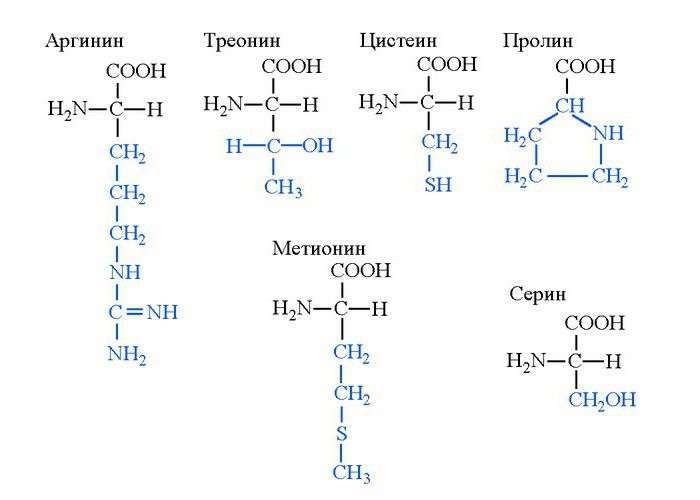
Snov serin je aminokislina, ki obstaja kot optični L in D-izomeri. To je nadomestljiva snov, ki se sintetizira iz fosfoglicerata. Serin lahko nastane med encimsko reakcijo iz glicina. Ta interakcija je reverzibilna, zato se glicin lahko tvori iz serina. Glavna vrednost slednjega je, da se encimi proteini, natančneje njihovi aktivni centri, sintetizirajo iz serina. Široko serin je prisoten v sestavi strukturnih proteinov.
Arginin, metionin, treonin
Biokemiki so ugotovili, da prekomerno uživanje arginina izzove razvoj Alzheimerjeve bolezni. Vendar pa so poleg negativne vrednosti snovi prisotne in vitalne funkcije za razmnoževanje. Zlasti zaradi prisotnosti gvanidinske skupine, ki prebiva v celici v kationski obliki, lahko spojina tvori veliko količino vodikovih medmolekularnih vezi. Zaradi tega arginin v obliki zwitteriona pridobi sposobnost vezanja s fosfatnimi regijami molekul DNA. Rezultat interakcije je nastajanje več nukleoproteinov - oblika pakiranja DNA. Arginin se lahko med spremembo pH jedrskega matriksa celice loči od nukleoproteina, kar zagotavlja odvijanje verige DNA in začetek prevajanja za biosintezo beljakovin.
V svoji strukturi aminokislinski metionin vsebuje atom žvepla, zato ima čista snov v kristalni obliki neprijeten gnilo vonj zaradi oddaje vodikovega sulfida. Pri ljudeh metionin opravlja regenerativno funkcijo in spodbuja celjenje membran jetrnih celic. Zato se proizvaja v obliki aminokislinskega zdravila. Metionin se sintetizira in drugo zdravilo je namenjeno za diagnozo tumorjev. Sintetizira se z zamenjavo enega ogljikovega atoma s C11 izotopom. V tej obliki se aktivno kopiči v tumorskih celicah, kar omogoča določitev velikosti možganskih neoplazem.
Za razliko od zgoraj omenjenih aminokislin je treonin manj pomemben: iz njega se ne sintetizirajo aminokisline, njegova vsebnost v tkivih pa je majhna. Glavna vrednost treonina - vključitev beljakovin. Ta amino kislina nima posebnih funkcij.
Asparagin, lizin, glutamin
Asparagin je običajna, zamenljiva aminokislina, ki je prisotna kot L-izomer sladkega okusa in grenki D-izomer. Beljakovine v telesu nastajajo iz asparagina, oksaloacetat pa se sintetizira z glukoneogenezo. Ta snov lahko oksidira v ciklu trikarboksilne kisline in proizvaja energijo. To pomeni, da asparagin poleg strukturne funkcije opravlja tudi energetsko funkcijo.
Ni moč sintetizirati v človeškem telesu lizin je aminokislina z alkalnimi lastnostmi. Večinoma so sintetizirani imunski proteini, encimi in hormoni. Hkrati je lizin aminokislina, ki neodvisno razvije protivirusna sredstva proti virusu herpesa. Vendar se snov ne uporablja kot zdravilo.
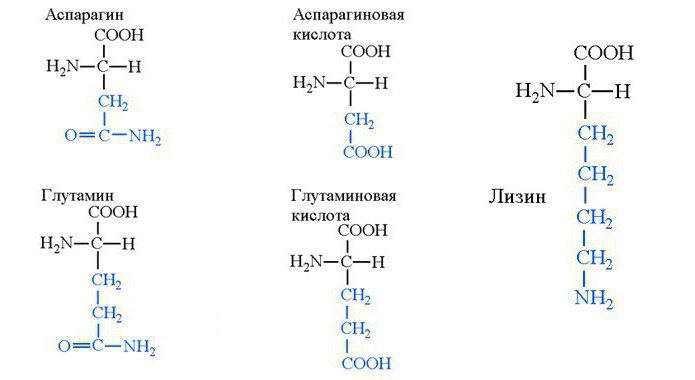
Aminokislinski glutamin je v krvi prisoten v koncentracijah, ki daleč presegajo vsebnost drugih aminokislin. Ima pomembno vlogo pri biokemičnih mehanizmih dušikove presnove in izločanja metabolitov, sodeluje pri sintezi nukleinske kisline encimi, hormoni, lahko okrepijo imunski sistem, čeprav se ne uporablja kot zdravilo. Toda glutamin se pogosto uporablja pri športnikih, saj pomaga pri okrevanju od vadbe, odstranjuje metabolite dušika in butira iz krvi in mišic. Ta mehanizem za pospešitev okrevanja športnika se ne šteje za umetnega in ni pravilno priznan kot doping. Poleg tega ni nobenih laboratorijskih metod za odkrivanje športnikov pri takem dopingu. Glutamin je prisoten tudi v znatnih količinah v hrani.
Asparaginska in glutaminska kislina
Aspartinske in glutaminske aminokisline so izjemno koristne za človeško telo zaradi svojih lastnosti, ki aktivirajo nevrotransmiterje. Pospešujejo prenos informacij med nevroni, kar zagotavlja ohranjanje učinkovitosti možganskih struktur, ki ležijo pod korteksom. V takih strukturah je pomembna zanesljivost in doslednost, saj ti centri uravnavajo dihanje in krvni obtok. Zato je v krvi ogromna količina aspartinske kisline in aminokisline glutamina. Prostorska strukturna formula aminokislin je prikazana na spodnji sliki.
Aspartinska kislina sodeluje pri sintezi sečnine, saj izločanje amoniaka iz možganov. Je pomembna snov za vzdrževanje visoke stopnje razmnoževanja in obnove krvnih celic. Seveda je pri levkemiji ta mehanizem škodljiv, zato so za doseganje remisije uporabljeni pripravki encimov, ki uničujejo aspartno amino kislino.
Četrtina vseh aminokislin v telesu je glutaminska kislina. Je nevrotransmiter postsinaptičnih receptorjev, potrebnih za sinaptični prenos impulza med procesi nevronov. Za glutaminsko kislino pa je značilen ekstra-sinaptični način prenosa informacij - volumetrična nevrotransmisija. Ta metoda je osnova spomina in je nevrofiziološka uganka, ker še ni jasno, katere receptorje določajo količino glutamata zunaj celice in zunaj sinaps. Predvidevamo pa, da je za množično nevrotransmisijo pomembna količina snovi zunaj sinapse.
Kemijska struktura
Vse nestandardne in 20 standardnih aminokislin imajo skupen načrt strukture. Vključuje ciklično ali alifatsko ogljikovodično verigo z ali brez radikalov, amino skupino na alfa ogljikovem atomu in karboksilno skupino. Ogljikovodikova veriga je lahko katera koli, tako da ima snov reaktivnost aminokislin, pomembno je mesto glavnih radikalov.
Amino skupino in karboksilno skupino moramo vezati na prvi ogljikov atom v verigi. V skladu z nomenklaturo, sprejeto v biokemiji, se imenuje alfa atom. Pomemben je za tvorbo peptidne skupine - najpomembnejše kemijske vezi, zaradi katere obstaja beljakovina. Z vidika biološke kemije se življenje imenuje način obstoja beljakovinskih molekul. Glavna vrednost aminokislin je tvorba peptidne vezi. V članku je predstavljena splošna strukturna formula aminokislin.
Fizične lastnosti
Kljub podobni strukturi ogljikovodikove verige so aminokisline bistveno drugačne po fizikalnih lastnostih od karboksilnih kislin. Pri sobni temperaturi so hidrofilne kristalinične snovi, ki se dobro raztopijo v vodi. V organskem topilu zaradi disociacije pri odstranitvi karboksilne skupine in protonov se aminokisline slabo raztopijo in tvorijo zmesi snovi, ne pa tudi resnične raztopine. Številne aminokisline so sladkega okusa, karboksilne kisline pa kisle.
Te fizikalne lastnosti so posledica prisotnosti dveh funkcionalnih kemijskih skupin, zaradi katerih se snov v vodi obnaša kot raztopljena sol. Pod delovanjem vodnih molekul se proton cepi iz karboksilne skupine, katere akceptor je amino skupina. Zaradi premestitve elektronske gostote molekule in odsotnosti prostega gibanja protonov pH (indeks kislosti), raztopina ostane dokaj stabilna pri dodajanju kislin ali alkalij z visoko disociacijsko konstanto. To pomeni, da lahko aminokisline tvorijo šibke puferske sisteme, ki ohranjajo homeostazo telesa.
Pomembno je, da je modul polnjenja disociirane aminokislinske molekule nič, ker proton, ločen od hidroksilne skupine, prevzame dušikov atom. Na dušiku v raztopini pa se tvori pozitivni naboj in na karboksilni skupini se tvori negativni naboj. Sposobnost disociacije je neposredno odvisna od kislosti, zato je za raztopine aminokislin prisotna izoelektrična točka. To je pH (indeks kislosti), pri katerem največje število molekul nima ničelnega naboja. V tem stanju so stacionarni na električnem polju in ne delujejo toka.